מטריקס מטאלו-פרוטאינאז Matrix metalloproteinase 9 - 9
| מדריך בדיקות מעבדה | |
| מטריקס מטאלו-פרוטאינאז 9 | |
|---|---|
| Matrix metalloproteinase 9 | |
| שמות אחרים | MMP-9, matrix metallopeptidase 9,.B gelatinase, GELB |
| מעבדה | כימיה בדם |
| תחום | מטלופרוטאינאז מתכתי המשתתף במגוון של תהליכים פתולוגיים, כגון סרטן, מצבי דלקת ומחלות אימונולוגיות וקרדיו-וסקולריות. |
| טווח ערכים תקין | 0-983 ננוגרם/מיליליטר. |
| יוצר הערך | פרופ' בן-עמי סלע |
הגן המקודד ל-MMP-9 ממוקם על הזרוע הארוכה של כרומוזום 20 בעמדה 20q11.2-q13.1, והוא מכיל 13 אקסונים. האנזים MMP-9 מסונתז כ-pre-pro-enzyme המכיל 707 חומצות אמינו כולל signal peptide בן 19 חומצות אמינו, והוא מופרש כ-pro-MMP בלתי פעיל. באדם, pro-MMP-9 enzyme מורכב מ-5 מקטעים (domains), מתוכם הפרו-פפטיד בקצה ה-N-טרמינאלי, המקטע הקטליטי הקושר אבץ, והמקטע ה-C-טרמינאלי דמוי ה-hemopexin הם מקטעים שמורים. המקטע הפרו-פפטידי מאופיין על ידי רצף שמור של 7 ח' האמינו - PRCGVPD. הציסטאין (C) בתוך רצף זה ידוע בתור ה-"cysteine switch", הקושר את האבץ הקטליטי לשמור את האנזים בצורתו הלא פעילה (Nagase ו-Woessner ב-J Biol Chem משנת 1999).
השפעול של האנזים מושג על ידי רצף (cascade) של פעילויות פרוטאוליטיות בה משתתף פלזמין ו-stromelysin 1 (הידוע גם כ-MMP-3), שבו פלזמין משפעל ויוצר MMP-3 פעיל מהזימוגן שלו. ה-MMP-3 הפעיל מבקע את הפרו-פפטיד מ-pro-MMP-9 שגודלו 92,000 דלטון, ליצירת אנזים פעיל שמשקלו המולקולארי 82,000 דלטון (Ramos-DeSimone וחב' ב-J Biol Chem משנת 1999). המקטע הקטליטי של MMP-9 מכיל שני אטומי אבץ ושלושה אטומי סידן. האבץ הקטליטי עובר קואורדינציה על ידי שלושה שיירי היסטידין של motif הקישור המשומר למצע המכיל 13 חומצות אמינו - HEXXHXXGXXH. אטום האבץ השני ושלושת אטומי הסידן תורמים למבנה התלת ממדי של המקטע הקטליטי. בנוסף, שייר מתיונין משומר היוצר במבנה מה שמכונה "Met-turn" ייחודי, אחראי לקטלוג של MMP-9 כ-metzincin (על פי Bode וחב' ב-FEBS Lett משנת 1993).
שלושה מקטעים חוזרים (repeats) של פיברונקטין-type II מוחדרים לתוך המקטע הקטליטי, כאשר הצורה הפעילה של MMP-9 מכילה גם בקצה ה-C טרמינלי שלה מקטע דמוי-hemopexin המכיל שני יוני סידן ושני יוני כלוריד ( Gomis-Rüth וחב' ב-J Mol Biol משנת 1996). מקטע ה-hemopexin חיוני לאפשר את ביקוע הקולאגנים התלת-גדיליים האינטרסטיציאליים.
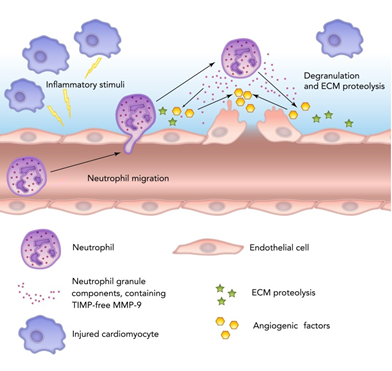
פעילות נויטרופילים: MMP-9 בשילוב עם elastase מהווה גורם רגולטורי בנדידה של נויטרופילים החודרים דרך ה-basement membrane (Boyer וחב' ב-Am J Respir Cell Mol Biol משנת 1996). ל-MMP-9 יש כמה תפקידים חשובים בתפקוד של נויטרופילים כמו הרס של המשתית החוץ-תאית (ECM), שפעול של IL-1β, וביקוע של מספר כימוקינים (Opdenakker וחב' ב-J Leukoc Biol משנת 2001). במודל של עכברים, חסר של MMP-9 גרם לעמידות להלם הנגרם על ידי אנדוטוקסין, מה שמצביע על החשיבות של MMP-9 בספסיס (Dubois וחב' ב-Eur J Immunol משנת 2002).
אנגיוגניות: MMP-9 עשוי לשחק תפקיד חשוב בתהליך האנגיוגניות ויצירה מחודשת של כלי-דם. לדוגמה, נראה ש-MMP-9 מעורב בתהליך ה-remodeling הקשור לרה-וסקולריזציה של גליומה (Forsyth וחב' ב-Br J Cancer משנת 1999). נראה ש-MMP-9 הוא רגולטור חיוני של יצירת growth plate והיצירה של כונדרוציטים היפרטרופיים. במודל של עכבר knockout ללא MMP-9, נמצא עיכוב בתהליך האפופטוזיס, בתהליך וסקולריזציה, ובהתגָּרְמוּת של כונדרוציטים (Vu וחב' ב-Cell משנת 1998). כן מתברר ש-MMP-9 שהוא למעשה gelatinase B נדרש לגיוס של תאי-גזע אנדותליאליים, שהוא מרכיב קריטי באנגיוגניות (Heissig וחב' ב-Cell משנת 2002).
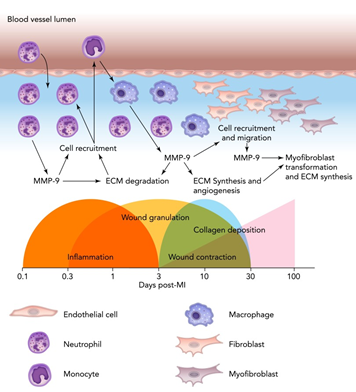
ריפוי פצעים: MMP-9 מבוטא באופן ניכר במהלך ריפוי של אפיתל מערכת הנשימה (Buisson וחב' ב-J Cell Physiol משנת 1996). במודל של עכברים מחוסרי MMP-9, נמצא שעכברים אלה לא היו מסוגלים להרחיק את משתית הפיברינוגן בעת ריפוי פצעים (Mohan וחב' ב-J Biol Chem משנת 2002). כאשר gelatinase B מגיב עם TGF-β1, הוא מעודד את הכיווץ של קולאגן, מה שמסייע לסגירת הפצע (Kobayashi וחב' ב-Lung Cell Mol Physiol משנת 2014).
MMP-9 וסרטן
אחת הפתולוגיות של MMP-9 קשורה למעורבותו בתהליך הסרטני כתוצאה מתפקידו ב-remodeling של ה-ECM ובאנגיוגניות. לדוגמה, MMP-9 מבוטא ביתר בתאי סרטן שד ממאירים (Morint וחב' ב-Int J Cancer משנת 2000). האנזים Gelatinase B משחק תפקיד מרכזי בהתקדמות הגידול משלב האנגיוגניות, לשלב ההתפשטות הגרורתית (Na וחב' ב-Cancer משנת 2014). קומפלקסים של gelatinase B ו-TIMPs (שהם המעכבים הרקמתיים של MMPs) מוגברים בסרטן מערכת העיכול ובממאירויות גינקולוגיות (Zucker ב-Cancer משנת 1995). המעורבות של MMP-9 בהתפתחות ממאירויות באדם, קשורה לביקוע של קולאגן type IV ב-basement membrane וב-ECM מה שמסייע לתאי הסרטן לנוע, לחדור לרקמות סמוכות ולשלוח גרורות (Groblewska וחב' ב-Folia Histochem & Cytobiol משנת 2012, Gress וחב' ב-Int J Cancer משנת 1995, ו-John ו-Tuszynski ב-Pathol Oncol Res משנת 2001).
באופן כללי MMPs כרוכים בשלבים הראשונים של התפתחות סרטן על ידי שהם הורסים את ה-ECM ופוגעים ב-basement membrane באופן שמאפשר לתאי הסרטן להתפשט מאזור הגידול הראשוני. בשלבים מאוחרים יותר MMPs יכולים לסייע לגרורות על ידי שינוי ב-integrins של תאי הסרטן (Ranuncolo וחב' ב-Cancer משנת 2002). במקור, נחקרה היצירה הישירה של פרוטאינזות על ידי תאי הסרטן. חלבונים אונקוגניים, פקטורי גדילה והורמונים עשויים לתרום לוויסות יצירת MMP-9 על ידי תאי סרטן שונים (Van den Steen וחב' ב-Crit Rev Biochem Mol Biol משנת 2002). היבט נוסף הוא יצירה של MMP-9 על ידי תאים סביב תאי הסרטן, כמו תאים פיברובלסטים סמוכים בהם יצירת MMP-9 מושרית על ידי התאים הסרטניים (Stuelten וחב' ב-J Cell Sci משנת 2005). אגב, לפרוטאוליזה על ידי MMP-9 יכולות להיות גם השפעות חיוביות: לדוגמה, tumastatin ו-endostatin הם פרגמנטים של קולאגן, עם פעילות אנטי-טומורוגנית (O'Reilly וחב' ב-Cell משנת 1997, ו- Maeshima וחב' ב-Science משנת 2002). במיקרו-סביבה של הגידול, ה-MMP-9 מופיע לרוב כתוצר הפרשה של תאים דלקתיים מגויסים, בעיקר נויטרופילים ומקרופאגים (Bergers וחב' ב-Nat Cell Biol משנת 2000, Coussens וחב' ב-Cell משנת 2000, ו-Nielsen וחב' ב-Int J Cancer משנת 1996).
MMP-9 המופרש במיקרו-סביבה של הגידול על ידי תאי סטרומה של מח העצם, מגביר את ההפרשה של VEGF, מה שמעלה את ריכוזו בנסיוב, ומהווה גירוי נוסף של תאי מח עצם. ההשערה היא שהרחקת MMP-9 מהמיקרו-סביבה של הגידול, קוטעת את הלולאה VEGF ממח עצם/MMP-9, מה שמפחית את האנגיוגניות ואת המייאלו-פויאזה. השערה זו נבחנה בהצלחה עם מעכב של amino-biphosphonate (Melani וחב' ב-Cancer Res משנת 2007). נויטרופילים ומקרופאגים מבטאים MMP-9 באופן דיפרנציאלי ויש להם גם השפעה דיפרנציאלית על אנגיוגניות ווסקולוגנזה. כמו שהודגם בעכברי knockout מחוסרי MMP-9, נמצא שאכן MMP-9 חיוני לוסקולוריזציה על ידי השתלת מח עצם מעכברי wild type המכילים MMP-9 ששחזרה את הווסקולוריזציה. לפיכך, נראה שהאנזים MMP-9 עשוי לשמש יעד לתרפיה של תהליך הסרטני (Ahn ו-Brown ב-Cancer Cell משנת 2008). גידול קטן-ממדים זקוק לצורך גידולו לאנגיוגניות כדי שכלי-דם חדשים יוצרו ויזינו את הגידול, כאשר תהליך זה ידוע כ-angiogenic switch (Folkman ב-Seminars cancer Biol משנת 1992), ו-MMP-9 מסתמן כגורם התומך באנגיוגניות (Giraudo וחב' ב-J Clin Invest משנת 2004).
MMP-9 וסרטן שלפוחית השתן: MMP9 נכרך עם סרטן שלפוחית השתן (Sier וחב' ב-Clin Cancer Res משנת 2000), ורמות MMP-9, MMP-2 ו-TIMP משמשות סמנים לאבחון לא-חודרני של סרטן השלפוחית (Eissa וחב' ב-Eur Urol משנת 2007).
MMP-9 וסרטן פי-הרחם: במודל קדם-קליני בעכברים לגבי סרטן פי הרחם המושרה על ידי HPV, נמצא שרק הביטוי של MMP-9 שנקבע בשיטות RT-PCR, אימונוהיסטוכימיה ו-gelatin zymography, עלה בצורה משמעותית בעת התקדמות המהלך הסרטני. באנליזה קלינית, ביטוי מוגבר של MMP-9 היה כרוך עם פרוגנוזה גרועה של המטופלות (Sheu וחב' ב-Cancer Res משנת 2003).
MMP-9 וסרטן העור והאפיתל האוראלי: מחקר בחיפוש אחר סמן אמין לנבא גרורות של קרצינומת תאי הקשקש, מצא שקרצינומה לא-חודרנית של הפה חסרה MMP9, בהשוואה לקרצינומה אוראלית לא-חודרנית. לפיכך השימוש של MMP9 כסמן פרוגנוסטי (Inmpola וחב' ב-J Pathol משנת 2004). מאפיין חשוב של סרטני עור ידוע כ-epithelial-to-mesenchymal transition (להלן EMT) של קרטינוציטים, כאשר מעבר זה לפנוטיפ חודרני דורש איתות על ידיTGF-β . בעוד ש- TGF-βהוא בעל השפעה שלילת בשלבים מאוחרים של התפתחות תאי הסרטן, יש לו תפקיד הגנתי בשלבים המוקדמים (Wang ב-Microsc Res Tech משנת 2001).
MMP-9 וסרטן הערמונית: MMP-9 מבוטא ומופרש על ידי תאי סרטן הערמונית, מה שגורם לשגשוג מופחת של תאי סרטן אלה. המסלול של β3-integrin-ERK כרוך בביטוי ובהפרשה של MMP-9 (Biswas וחב' ב-Cancer Res משנת 2010). ביטוי גבוה של MEK5 נכרך עם שגשוג וגרורות של סרטן הערמונית, והוא גם נכרך עם רמות מוגברות יותר של MMP-9 mRNA על ידי סטימולציה של ה-promoter של הגן המקודד ל-MMP-9 דרך AP-1 (Mehta וחב' ב-Oncogene משנת 2003). ברקמת קרצינומה של הערמונית, הביטוי משותף של matrilysine-2 ושל MMP-9 נמצא בעל חשיבות בהתקדמות סרטן זה, כיוון ש-matrilysine-2 הוא המשפעל של proMMP-9 (zhao וחב' ב-J Biol Chem משנת 2003).
MMP-9 וסרטן השחלות: תאי סרטן השחלות יכולים להיות מגורים על ידי ההורמון GnRH, לייצר MMP-9 על ידי איתות דרך האונקוגן c-jun, מה שמגביר גם את התנועתיות של תאים אלה ואת כושר החודרנות שלהם (Cheung וחב' ב-Cancer Res משנת 2006).
MMP-9 וגידולים סרטניים במוח: עיכוב של יצירת MMP-9 עם siRNA עיכב בהצלחה גידול של medulloblastoma במודל של הזרקת תאי סרטן זה למוח. טרנספקציה של MMP9 siRNA הביא לעצירה של מעגל חיי תאים אלה (Rao וחב' ב-Mol Cancer Ther משנת 2007). במחקר על תאי מנינגיומה באדם, ביטוי מוגבר של Ets-1 ושל MMP-9 היה כרוך בהישנות המנינגיומה. נראה ש-Ets-1 כרוך בהישנות של מנינגיומה על ידי השדרוג שלMMP-9 (Okuducu וחב' ב-Cancer משנת 2006). בעכברים, השגשוג של glioma עוכב בהצלחה על ידי העברה דרך נגיף adeno של רצף antisense-MMP-9 gene (על פי Lakka וחב' ב-Oncogene משנת 2002). מסלול התלוי ב-ERK מווסת את החודרנות של תאי glioma בתיווך של MMP-9 . תאים עם RRK חסום מכילים פחות ,MMP-9 mRNA פחות MMP-9 וממילא פחות פעילות של .MMP-9
MMP-9 וסרטן השד: קומפלקסים של neutrophil gelatinase-associated lipocalin (NGAL)/MMP9, נמצאו בערך ב-90% מדגימות השתן של מטופלות עם סרטן השד, אך לא נמצאו בשתן של נשים בריאות (Bolignano וחב' ב-Cancer Lett משנת 2010). יתרה מכך, ביטוי גבוה של MMP-9 נכרך עם הישרדות קצרה יותר של נשים עם סרטן שד (Dufour וחב' ב-Cancer Res משנת 2011). רמות של MMP-9, של NGAL ושל הקומפלקס של שני אלה, שנמדדו בנסיוב של מטופלות עם ductal carcinoma חודרנית, היו במתאם טוב עם חומרת המחלה (Provatopoulou וחב' ב-BMC Cancer משנת 2009). הביטוי של MMP-9 בסרטן השד קשור חלקית לביטוי של גורם השעתוק AP-2 ולאונקוגן.HER2 הפוטנציאל החודרני של תאי סרטן השד יכול להיות מוגבר בהוספה של IL-1β, מה שמעלה את הרמות של MMP-9 (Wang וחב' ב-Breast Cancer Res Treat משנת 2005). ביטוי-יתר של MMP-9 הביא להפרשה של החלבון האנטי-אנגיוגני endostatin (Bendrik וחב' ב-Cancer Res משנת 2008). הקולטן αvβ3 הקשור לספיחה, מעודד את הגרורתיות של סרטן שד באדם, תוך שיתוף פעולה עם MMP-9. רק תאים עם integrin αvβ3 משופעל, מכילים MMP-9 משופעל בתאי סרטן השד.
MMP-9 וסרטן מערכת העיכול: בקרצינומה של תאי הקשקש בוושט, הביטוי של MMP-9 בציטופלזמה של התאים סרטניים בולט בעיקר בתאים הנמצאים בחזית של התאים הגרורתיים, בהם הביטוי המשולב של matrilysin-2 ושל MMP-9 היה כרוך בפרוגנוזה גרועה (Yamamoto וחב' ב-carcinogenesis משנת 2004). בסרטן הלבלב, MMP-9 ממקור של נויטרופילים, פועל כגורם אנגיגני פוטנטי וישיר שאינו תלוי ב-VEGF (על פי Bausch וחב' ב-Angiogenesis משנת 2014). חודרנות של תאי קרצינומה הפאטו-צלולרית המוגברת על ידי קרינה, נחקרה בהקשר של ביטוי MMP-9. קרינה נמצאה מגבירה את רמות MMP-9 mRNA, את רמת MMP-9 ואת פעילותו (Cheng וחב' ב-Oncogene משנת 2006). בשלבים המאוחרים של סרטן המעי הגס, חסר הביטוי של גורם השעתוק AP2α, מה שמביא לביטוי גבוה של רמות MMP-9 (על פי Schwartz וחב' ב-Oncogene משנת 2007).
MMP-9 וסרטן גְּרוֹנִי, ואפי-לועי: רקמת סרטן הגרון מכילה רמות גבוהות של MMP-9 בהשוואה לרקמת גרון בריאה. תאי קרצינומה אפית-לועית היו חודרניים יותר לאחר גירוי עם הורמון העקה norepinephrine, במקביל לשדרוג ההפרשה של MMP-9 (על פי Yang וחב' ב-Cancer Res משנת 2006).
MMP-9 בלויקצמיה, לימפומה ו-multiple myeloma
הביטוי של MMP-9 התגלה גם בלימפומות של תאי T ובתאי הסטרומה שלהן (Ganor וחב' ב-leukemia Lymphoma משנת 2009). מטופלים עם לימפומה המבטאת MMP-9 הם בעלי הישרדות נמוכה (Sakata וחב' ב-Cancer משנת 2004). הקומפלקס MMP-9/Ku נמצא בתת-קבוצה של תאי לויקמיה באדם. הועלתה השערה שקומפלקס זה על פני תאי לויקמיה מגביר את התפשטותם (Monferran וחב' ב-EMBO J משנת 2004, ו-Paupert וחב' ב-Cell Cycle משנת 2008). Galectin-7 המבוטא על ידי תאי לימפומה, מגביר את התהליך הסרטני ומחיש חודרנות. Galectin-7 משרה סינתזה de novo שלMMP-9 mRNA (Demers וחב' ב-Cancer Res משנת 2005). בעזרת מגע קרוב עם תאי לימפומה, תאי סטרומה משרים את הביטוי של EGR-1 דרך איתות של EGF, תהליך בו יש ביטוי מופחת של MMP-9, וכתוצאה מכך מפחית את השגשוג של לימפומה ממקור התימוס (Bouchard וחב' ב-Blood משנת 2010). במטופלים עם לימפומה של ה-CNS, הרמות בנסיוב של MMP-9 כרוכות בסטאטוס של מחלה רדיוגרפית. רמה מוגברת בנסיוב של MMP-9 אינה מנבאת הישרדות (Hottinger וחב' ב-Ann Neurol משנת 2011).
ההתקדמות של multiple myeloma (להלן MM) כרוך בנדידה של תאי MM ממח העצם לדם. במהלך תהליך זה. התאים חייבים לעבור דרך שכבות של תאי אנדותל ושל basement membranes. מסיבה זו MMP-9 יכול להיות חיוני במיוחד לנדידה של תאי MM. בבחינה in vitro, תאי MM ראשוניים שבודדו מחולים, נמצאו בעלי יכולת לנדוד דרך matrigel רק אם הם מפרישים MMP-9 (Vande-Broek וחב' ב-Leukemia משנת 2004). בנוסף, האנדותל של מח העצם ותאי סטרומה יכולים לעודד הפרשה של MMP-9 על ידי תאי MM על ידי יצירת הכימוקיןCXCL1/SDF-1 על פי Parmo-Cabanas וחב' ב-J Pathol משנת 2006).
התפקידים הפתולוגיים של MMP-9
רמות מוגברות של MMP-9 נכרכו עם מחלות דלקתיות, אוטו-אימוניות, ניווניות וסרטניות רבות. להלן מספר דוגמאות למעורבות של MMP-9 בתחלואה במערכות שונות:
- תחלואות ריאה: מחקר רב נסוב על תפקיד MMP-9 בדלקת של דרכי האוויר ותהליכי remodeling בריאות. תחלואות ריאה שכיחות והם עלולות להתבטא החל מרגישות-יתר חריפה כמו אסתמה ו-acute respiratory distress syndrome (להלן ARDS) וכלה במחלות כרוניות כגון COPD או במחלות גנטיות כגון cystic fibrosis, סרטן ריאות או פיברוזיס אינטרסטיציאלי של הריאה. קיים איזון עדין בין מרכיבי ECM ותוצרי הפירוק שלהם בריאות, כאשר הפרה של איזון זה, עלולה לגרום לדוגמה לפיברוזיס ריאתי. כיוון ש-MMP-9 כרוך בדגרדציה של ECM, תפקידו נחקר במספר מחלות ריאה (Profita וחב' ב-Allergy משנת 2004). תאי אפיתל של הסימפונות מבטאים MMP-9 כתוצאה מגירוי על ידי TNF-α דרך שפעול של גורם השעתוק הגרעיני NF-κ B (Hozumi וחב' ב-Am J Physiol Lung Cell Mol Physiol משנת 2001). בנוסף, במחלות ריאה דלקתיות לויקוציטים תורמים לעודף של MMP-9 בריאה. בסרטן ריאות, תאי הסרטן והלויקוציטים המסתננים, מייצרים אף הם MMP-9. אסתמה ו-ARDS הן מחלות ריאה חריפות בהן התגלה ביטוי של MMP-9 (Kong וחב' ב-PLoS One משנת 2011, ו-Fligiel וחב' ב-Hum Pathol משנת 2006). היחס בין MMP-9 לבין המעכב שלו TIMP-1, הוא גורם חשוב בפתוגניות של ARDS (Lanchou וחב' ב-Crit Care Med משנת 2003).
- רמות מוגברות של MMP-9 ושל פעילותו, ברקמת ריאות היקפית של חולים עם COPD יוחסו לחומרת המחלה. רמות מוגברות של MMP-9 התגלו בפאזת הדחיסה (condensate) של האוויר הנשאף על ידי ילדים עם ברונכיאקטזיס (או רחבת הסמפונות) שהיא מחלה חסימתית של הריאה המאופיינת בהתרחבות בלתי הפיכה של הסימפונות. על פי רוב מדובר במחלה נרכשת, אולם במקרים נדירים תיתכן הופעה מולדת שלה. עשן סיגריות מכיל מספר רכיבים קרצינוגניים כגון benzo[a]pyrene העלולים להשרות ממאירות בריאות. טוקסינים אלה יכולים לשפעל איתות של NF-κB ולהביא לייצור של MMP-9 (Nakamaru וחב' ב-FASEB J משנת 2009). אכן, עשן סיגריות יכול להשרות הופעת אמפיזמה על ידי גירוי של הסננת תאי חיסון המפרישים פרוטאזות הגורמות להרס של ה-ECM ולאמפיזמה (Churg וחב' ב-Thorax משנת 2007). אף על פי ש- MMP-9 נמצא בריאות אמפיזמטיות, לא ניתן למצוא קורלציה בין התפתחות אמפיזמה על ידי MMP-9 שכן לא ניתן היה ליישם אסטרטגיות של עיכוב MMP-9 באמפיזמה (Atkinson וחב' ב-Am J Respir Crit Care Med משנת 2011). MMP-9 הוא יעד פוטנציאלי לטיפול ב-COPD (Muroski וחב' ב-Curr Pharm Biotechnol משנת 2008).
MMP ב-cystic fibrosis (להלן CF) מדובר בתהליך דלקתי ו-remodeling של דרכי האוויר. לפיכך, פעילות של פרוטאזות היא בעלת חשיבות משמעותית בפתוגנזה של CF. רמות מוגברות של MMP-9 ורמות מופחתות של המעכב TIMP-1 נמצאו בריאותיהם של חולי CF. בנוסף, hydroxynonenal-4 (להלן HNE) נתגלו בדגימות ליחה של חולי CF, ורמות אלו נמצאות במתאם טוב עם הרמות של MMP-9 משופעל (Gaggar וחב' ב-Am J Physiol Lung Cell Mol Physiol משנת 2007).
MMP-9 בסוכרת: אחת המחלות האוטו-אימוניות השכיחות ביותר היא סוכרת type 1. הועלתה השערה ש-MMP-9 הוא גורם דיאבטוגני, בכך שהוא מבקע פרוטאוליטית אינסולין, הופך את האינסולין המבוקע למוליקולה אימונוגנית, ומעורר תגובה אוטו-אימונית (Descamps וחב' ב-FASEB J משנת 2003, ו-Opdenakker ו-Van Damme ב-Immunol Today משנת 1994). במודל של סוכרת type 1 בעכברים, proMMP-9 משודרג וכרוך בפעילות המחלה. עם זאת, MMP-9 אינו גורם למחלה במודל חיה זה, אך כאשר הוא משופעל על ידי טריפסין, הוא מסייע לדגרדציה של אינסולין ולסוכרת (Descamps וחב' ב-J Pathol משנת 2004).
יש גם ראיות לכך שרמות MMP-9 מוגברות גם בחולים עם סוכרת type 2 ועם מחלת עורקים כליליים. התכשיר האנטי-סוכרתי rosiglitazone מפחית משמעותית את רמות MMP-9 בנסיוב (Marx וחב' ב-Arterioscler Thromb Vasc Biol Thromb משנת 2003). נמצא גם שרמות גבוהות של גלוקוז, מאיצות את האיתות על ידי TGF-β ועל ידי Smad, מגבירות את הביטוי של קולטנים ל-TGF-β ומשרות שפעול של TGF-β לטנטי, בתיווך של MMP-9. רמות מוגברות של MMP-9 נכרכו עם סיבוכים וסקולריים של סוכרת הבאים לביטוי בנוירופתיה, נפרופתיה ורטינופתיה, ועשויות להיות סמנים של מצב מחלת הסוכרת (Kowluru וחב' ב-Expert Opin Investig Drugs משנת 2012, Lauhio וחב' ב-Ann Med משנת 2008, ו-Bhatt ו-Veeranjaneyulu ב-Neurol Sci משנת 2010).
MMP-9 ומחלת שריר שלד: ארבע קבוצות של פרוטאזות קשורות לפתולוגיה של מחלת שריר השלד: מערכת ה-ubiquitin-proteasome, פרוטאזות ליזוזומליות, פרוטאזות התלויות בסידן, ומטלו-פרואזות. אך רק MMPs קשורים לדגרדציה של ECM (Liu וחב' ב-Muscle Nerve משנת 2010). עם זאת MMP-9 אינו מסוגל לעכל קולאגן type 1 שהוא הקולאגן הדומיננטי ב-ECM השרירי.
MMP-9 ותחלואות עור: MMP-9 כרוך בשחרור של desmoglein-3 מקרטינוציטים מה שיכול לגרום לשינויים בארכיטקטורה הרקמתית ולגרום לבועות אפיתליאליות (Cirillo וחב' ב-Oral Dis משנת 2007). הביטוי של MMP-9 מושרה בקרטינוציטים של העור על ידי IL-13, והביטוי של MMP-9 בולט בעיקר בנגעי אקזמה (Purwar וחב' ב-J Invest Dermatol משנת 2008). קרינת infrared המופיעה בקרני-שמש, מעלה את טמפרטורת עור האדם, ומשרה בעור יצירה של MMP-9 בקרטינוציטים (Shin וחב' ב-Free Radic Biol Med משנת 2008). בשורות תאים של קרטינוציטים, TGF-β משרה את הביטוי של MMP-9 (Salo וחב' ב-J Biol Chem משנת 1991). יתרה מכך, integrin α3β1 מסוגל לשפעל את MMP-9 בעזרת TGF-β (Lamar וחב' ב-J Invest Dermatol משנת 2008). אימורטליזציה של קרטינוציטים על ידי מוטציית p53-null משנה את התפקוד של α3β1 ומשרה את הביטוי של MMP-9 ומאידך את החודרנות של תאי הסרטן (Lamar וחב' ב-Cancer Res משנת 2008). הנדידה של קרטינוציטים במהלך התקדמות התהליך הסרטני מווסתת גם על ידי TNF-α דרך מסלול בו MMP-9 תלוי ב-αvβ6. במחקר על קרטינוציטים ממאירים בעכברי knockout החסרים MMP-9 נבלם התהליך הסרטני. בשורת תאי קרטינוציטים MK בעכבר, רמות MMP-9 המופרש היו מוגברות על ידי ביטוי מוגבר של האונקוגן ERK, תהליך שהיה תלוי ב- α1β3 integrin. בנוסף, נמצא ש-integrin זה מסוגל לייצב את MMP-9 mRNA ולהגדיל ריכוזיMMP-9 (Iyer וחב' ב-J Cell Sci משנת 2005).
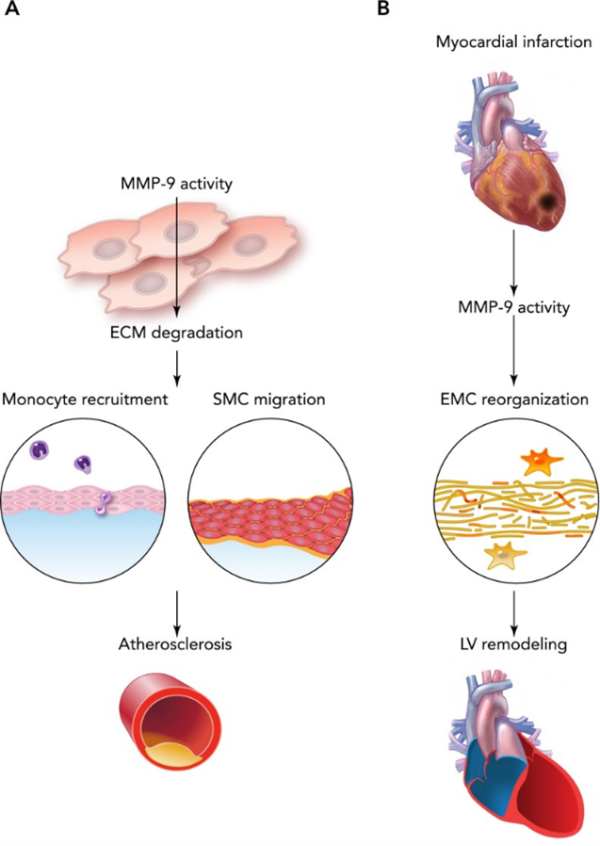
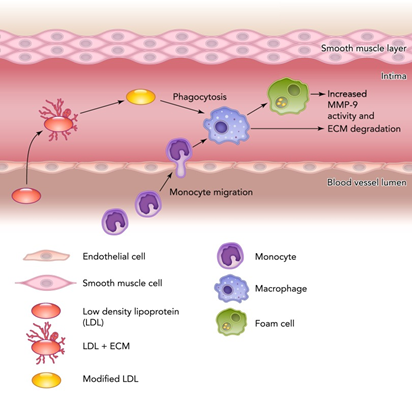
MMP-9 וטרשת עורקים: טרשת עורקים כרוכה ב-remodeling ממוקם של ה-ECM, ובנדידה ובשגשוג של תאי שריר חלק. מסיבה זו ה-remodeling של אנזימי המשתית כגון MMPs ובפרט gelatinases המסוגלים לפרק ג'לטין, נכרכו בתהליך הטרשתי (Whatling וחב' ב-Arterioscler Thromb Vasc Biol משנת 2004). התלישה של רובד טרשתי מתרחשת באופן תדיר יותר באזורי טרשת המכילים כמויות גדולות של מקרופאגים ותאי קצף (Speidl וחב' ב-FASEB J משנת 2004). לכן המחשבה הייתה שמקרופאגים מסוגלים להשרות תלישת רבדים על ידי הפרשת פרוטאזות המעכלות את המשתית. אכן, מקרופאגים של עכבר מבטאים ביתר MMP-9 פעיל, המחיש משמעותית את תלישת הרבדים (Gough וחב' ב-J Clin Invest משנת 2006). יש גורסים ש-MMP-9 מתפקד כסמן להערכת אי היציבות של הרובד הטרשתי (Robertson וחב' ב-J Intern Med משנת 2007). MMP-9 מסוגל לבקע N-cadherin ולגרום לשגשוג של VSMCs דרך איתות של β-catenin (Dwivedi וחב' ב-Cardiovasc Res משנת 2009). שגשוג של VSMC תורם לעיבוי של שכבת ה-intima בדופן העורקים. ל-MMP-9 יש תפקיד מפתח בנדידה של תאי שריר חלק וסקולריים (Mason וחב' ב-Circ Res משנת 1999). MMP-9 ועוד MMPs אחדים, מבוטאים ברקמה הטרשתית. מתברר ש-LDL מחומצן משדרג את הביטוי של MMP-9 ומפחית את הביטוי של TIMP-1 במקרופאגים ממקור מונוציטים, מה שיכול לתרום לדגרדציה של המשתית ברבדים טרשתיים (Lijnen ב-Thromb Haemost משנת 2001). בנוסף נמצא שיצירת MMP-9 במונוציטים משודרגת על ידי גורמים כגון אפינפרין, נור-אפינפרין ו-LPS.
MMP-9 ומפרצות (aneurysms)
מפרצת של עורק בטני (להלן מע"ב) מופיעה כהתרחבות קבועה של העורק הבטני, וכרוכים בה מסלולים פרוטאוליטיים, הרס ה-ECM של הדופן העורקי, תהליכי דלקת, עקה חמצונית ואפופטוזיס (Nordon וחב' ב-Nat Rev Cardiol משנת 2011), כאשר MMP-9 נכרך בתרחיש משמעותי זה. בנוסף, נמצא שמע"ב והקרע הדרמטי שעלול להתרחש בעורק, יכול להימנע על ידי מעכבים של MMPs כגון נגזרות סינתטיות של טטרה-ציקלינים, או על ידי ביטוי יתר של TIMP-1 במודל של חולדה (Lijnen ב-Thromb Haemost משנת 2001). בנוסף, עכברי knockout עם שפעול ירוד ביותר של MMP-9 היו מוגנים מפני מע"ב, והשפעה זו התבטלה על ידי הוספה של MMP-9 פעיל. בסוכרת, השרייה של MMP-9 מתרחשת על ידי שפעול של ERK, חלבון המשופעל על ידי p53, וכן על ידי NF-κB והיא נבלמת על ידי TGF-β. התכשיר Doxycycline מדכא את הגידול בממדי מפרצות עורקיות על ידי שהוא מעכב פעילות MMP-9 (Lindeman וחב' ב-Circulation משנת 2009, ו-Newman וחב' ב-Arterioscler Thromb משנת 1994).
MMP-9 והיפרטרופיה של החדר השמאלי: מצב זה מהווה הִסְתַּגְּלוּת של הלב ללחץ-דם גבוה שעלול להתפתח לאי-ספיקת לב. תהליך לבבי זה כורך remodeling של ה-ECM של שריר הלב, ולכן את הפעילות של MMPs כדוגמת MMP-9, ולפיכך עיכוב של ה-MMPs עשוי לסייע בטיפול במצב (Heymans וחב' ב-Am J Pathol משנת 2005).
MMP-9 ושבץ-מוחי: רמות מוגברות של MMP-9 נכרכו עם נזק מוחי בנפגעי שבץ (Rosell וחב' ב-Stroke משנת 2005). באזורי מוח של אוטם או של דימום, מוצאים הסננה חזקה של נויטרופילים המכילים MMP-9 בהתאמה לדגרדציה של קולאגן type IV ב-basal lamina. התכשיר edaravone הלוכד רדיקלים חופשיים והמשמש להתאוששות נוירולוגית לאחר אוטם מוחי, מדכא את הביטוי של MMP-9 mRNA ואת רמת MMP-9 ומעכב את השפעול שלNF-κB (Yagi וחב' ב-Stroke משנת 2009).
MMP-9 ופקקת: יצירת פקקת מבטאת איזון לקוי בין קרישת דם ופיברינוליזה, כאשר MMP-9 תורם כנראה יותר לתהליך הפיברינוליזה. אינטרפרון-γ משחק תפקיד מַזִּיק בהתפוגגות של DVT, בכך שהוא מדכא את הביטוי של MMP-9 ושל VEGF (Tai וחב' ב-J Pineal Res משנת 2010).
MMP-9 ופתולוגיה של העצם: מוטציות בגן המקודד ל-MMP-9 נכרכו עם מחלת עצם גנטית הידועה כ-metaphysical anadysplasia (Lausch וחב' ב-Am J Hum Genet משנת 2009). בנוסף, פולימורפיזם בנוקלאוטיד בודד (SNP) בגן של MMP-9 באדם, קשור לבקע בדיסקית של אזור המותן (Hirose וחב' באותו כתב עת משנת 2008). כמו כן, אובחנה ירידה בביטוי של הגן של MMP-9 בנגעים הידועים כ-tibial ,dyschondroplasia כאשר במחלה זו חלה ירידה בווסקולריזציה המיוחסת לביטוי של MMP-9 (Valeda וחב' ב- J Comp Pathol משנת 2011). נתונים אלה תואמים מאפיינים פנוטיפיים בעכברי knockout החסרים MMP-9 והלוקים גם כן ב-chondrodysplasia (Vu וחב' ב-Cell משנת 1998). מצטברות ראיות תפקודיות על פעילות MMP-9 לאחר שברי-עצם, בתהליכי ההתמיינות והוויסות של יצירת עצם פריוסטילית ואכונדרלית. ההשפעות של מעכבי פעילות של MMP-9 ב-remodeling של עצם במצבים נורמליים ופתולוגיים נחקרים כעת ( Ortega וחב' ב-Dis Model Mech משנת 2010, ו-Wang וחב' ב-Bone משנת 2012).
הוראות לביצוע הבדיקה
יש ליטול דם למבחנה כימית (פקק צהוב או אדום) ולסרכז בצנטריפוגה מקוררת, ויש להעביר את הנסיוב המופרד למבחנת פלסטיק ולהקפיא. יציבות הדגימה בטמפרטורת החדר- 4 שעות; יציבות הדגימה בקירור - 24 שעות; יציבות הדגימה בהקפאה - 30 יום. יש לפסול דגימה המגיעה למעבדה בטמפרטורת החדר, או נסיוב מאוד המוליטי. הבדיקה מתבצעת בשיטת ELISA.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק