הבדלים בין גרסאות בדף "מלנומה - טיפול - Melanoma - therapy"
| שורה 12: | שורה 12: | ||
}} | }} | ||
{{הרחבה|מלנומה}} | {{הרחבה|מלנומה}} | ||
| − | '''[[מלנומה]]''' (Melanoma) היא הסוג החמור ביותר של סרטן עור ממאיר. זיהוי מוקדם של הנגעים הוא חשוב ביותר היות והפרוגנוזה משתנה באופן משמעותי בהתאם לשלב גילוי המחלה - כמעט 100 | + | '''[[מלנומה]]''' (Melanoma) היא הסוג החמור ביותר של סרטן עור ממאיר. זיהוי מוקדם של הנגעים הוא חשוב ביותר היות והפרוגנוזה (Prognosis) משתנה באופן משמעותי בהתאם לשלב גילוי המחלה - כמעט 100 אחוזים שורדים את המחלה כאשר היא מתגלה בשלבים מוקדמים, לעומת פחות מ- 10 אחוזי שרידות כאשר קיימות גרורות בעת האבחנה. הסימן הקליני המחשיד ביותר לממאירות הוא הופעת שומה חדשה בעלת צורה וצבע חריגים, או שינוי במאפייני שומה קיימת. |
| − | לאחר שנים רבות בהם הטיפול הניתן לחולי מלנומה גרורתית היה מוגבל ביותר, | + | לאחר שנים רבות בהם הטיפול הניתן לחולי מלנומה גרורתית היה מוגבל ביותר, בשנות האלפיים חלה התקדמות רבה בטיפול המערכתי במלנומה. זאת בעקבות גילוי של מוטציות (Mutations) בגנים (Genes) שונים אשר אפשר טיפול ממוקד (Targeted) ומותאם לכל חולה. |
==אפידמיולוגיה== | ==אפידמיולוגיה== | ||
| − | בעולם מתגלים קרוב ל- 200,000 מקרים חדשים של מלנומה בשנה. בישראל מאובחנים מדי שנה כ- 200 חולים עם מלנומה בשלב הגרורתי. | + | בעולם מתגלים קרוב ל-200,000 מקרים חדשים של מלנומה בשנה. בישראל מאובחנים מדי שנה כ-200 חולים עם מלנומה בשלב הגרורתי. |
| − | 87 | + | 87 אחוזים מהחולים מאובחנים בשלב של מחלה מקומית (שלבים 2-1){{כ}}, 8 אחוזים בשלב בו המחלה מערבת בלוטות לימפה (Lymph nodes) אזוריות (שלב 3) ו-4 אחוזים בשלב בו קיימות גרורות (שלב 4). |
==אטיולוגיה== | ==אטיולוגיה== | ||
| שורה 28: | שורה 28: | ||
==קליניקה== | ==קליניקה== | ||
קיימים חמישה קריטריונים בסיסיים לזיהוי שומה החשודה כמלנומה: | קיימים חמישה קריטריונים בסיסיים לזיהוי שומה החשודה כמלנומה: | ||
| − | *'''א-סימטריה (Asymmetry)''': שומות רגילות הן בדרך כלל סימטריות, בעוד מלנומה עלולה להיות בעלת צורה לא סדירה או א-סימטרית | + | *'''א-סימטריה (Asymmetry)''': שומות רגילות הן בדרך כלל סימטריות, בעוד מלנומה עלולה להיות בעלת צורה לא סדירה או א-סימטרית |
:[[קובץ:Melanoma-01.png|מרכז|320 פיקסלים]] | :[[קובץ:Melanoma-01.png|מרכז|320 פיקסלים]] | ||
| − | *'''גבול (Border)''': לשומות רגילות יש בדרך כלל גבול חלק ומוגדר. במלנומה גבולות השומה לא סדירים, מטושטשים או מחוספסים | + | *'''גבול (Border)''': לשומות רגילות יש בדרך כלל גבול חלק ומוגדר. במלנומה גבולות השומה לא סדירים, מטושטשים או מחוספסים |
:[[קובץ:Melanoma-02.png|מרכז|320 פיקסלים]] | :[[קובץ:Melanoma-02.png|מרכז|320 פיקסלים]] | ||
| − | *'''גוון (Color)''': שומות רגילות הן בדרך כלל בצבע אחיד - חום. הגוון של מלנומה אינו אחיד, ושומה חשודה יכולה להופיע בשילוב של צבעים שונים - שחור, חום או חום-צהבהב, אדום, כחול ועוד | + | *'''גוון (Color)''': שומות רגילות הן בדרך כלל בצבע אחיד - חום. הגוון של מלנומה אינו אחיד, ושומה חשודה יכולה להופיע בשילוב של צבעים שונים - שחור, חום או חום-צהבהב, אדום, כחול ועוד |
:[[קובץ:Melanoma-03.png|מרכז|320 פיקסלים]] | :[[קובץ:Melanoma-03.png|מרכז|320 פיקסלים]] | ||
| − | *'''גודל או קוטר (Diameter)''': שומות בקוטר של 5 מילימטרים ומעלה חשודות יותר כמלנומות | + | *'''גודל או קוטר (Diameter)''': שומות בקוטר של 5 מילימטרים ומעלה חשודות יותר כמלנומות |
:[[קובץ:Melanoma-04.png|מרכז|320 פיקסלים]] | :[[קובץ:Melanoma-04.png|מרכז|320 פיקסלים]] | ||
| − | *'''שינוי (Evolution):''' הסימן החשוב ביותר. חשד למלנומה מתעורר כאשר מופיעה שומה חדשה וחריגה בצבע שחור, כאשר יש שינוי בגודלה, בצורתה, או בצבעה של שומה קיימת, או כאשר מופיע דימום או גרד בשומה, במיוחד אצל אנשים מעל גיל 40. לכן מעקב אחר שומות הוא הכרחי לאבחון מוקדם ולטיפול יעיל במחלה | + | *'''שינוי (Evolution):''' הסימן החשוב ביותר. חשד למלנומה מתעורר כאשר מופיעה שומה חדשה וחריגה בצבע שחור, כאשר יש שינוי בגודלה, בצורתה, או בצבעה של שומה קיימת, או כאשר מופיע דימום או גרד בשומה, במיוחד אצל אנשים מעל גיל 40. לכן מעקב אחר שומות הוא הכרחי לאבחון מוקדם ולטיפול יעיל במחלה |
:[[קובץ:Melanoma-05.png|מרכז|320 פיקסלים]] | :[[קובץ:Melanoma-05.png|מרכז|320 פיקסלים]] | ||
==אבחנה== | ==אבחנה== | ||
| − | האבחנה הסופית של מלנומה נעשית באמצעות ביופסיה של הנגע החשוד. | + | האבחנה הסופית של מלנומה נעשית באמצעות ביופסיה (Biopsy) של הנגע החשוד. |
==טיפול== | ==טיפול== | ||
הטיפול במלנומה הוא בהתאם לשלב המחלה: | הטיפול במלנומה הוא בהתאם לשלב המחלה: | ||
| − | *'''שלבים 1 | + | *'''שלבים 2-1:''' כריתה מקומית ודגימת בלוטת זקיף (Sentinel). במידה ומדובר בגידול באתר (In situ) ללא חדירה עמוקה וללא מאפיינים אגרסיביים, אין חובה לבצע דגימה של בלוטת הזקיף |
| − | *'''שלב 3:''' כריתה מקומית, כריתת בלוטות לימפה אזוריות וטיפול משלים | + | *'''שלב 3:''' כריתה מקומית, כריתת בלוטות לימפה אזוריות וטיפול משלים |
| − | *'''שלב 4:''' טיפול מערכתי- עד לאחרונה הטיפולים במלנומה היו מוגבלים מאוד ולא ממוקדים או מותאמים אישית. בשנים האחרונות התגלה כי כ- 50 | + | *'''שלב 4:''' טיפול מערכתי- עד לאחרונה הטיפולים במלנומה היו מוגבלים מאוד ולא ממוקדים או מותאמים אישית. בשנים האחרונות התגלה כי כ-50 אחוזים מהמלנומות הגרורתיות הן בעלות מוטציה בגן BRAF, הגורמת להיווצרות חלבון המעודד שגשוג בלתי-מבוקר של התאים הממאירים. נוכחות המוטציה BRAF מסתמנת כגורם פרוגנוסטי (Prognostic) שלילי להישרדות החולים |
===טיפול ממוקד במלנומה גרורתית- Zelboraf {{כ}}(Vemurafenib)=== | ===טיפול ממוקד במלנומה גרורתית- Zelboraf {{כ}}(Vemurafenib)=== | ||
| − | [[Zelboraf]] {{כ}}(Vemurafenib) הוא מעכב בררני של החלבון המוטנטי BRAF. מנגנון הפעולה של החלבון BRAF קשור לשפעול קולטן מסוג | + | [[Zelboraf]] {{כ}}(Vemurafenib) הוא מעכב בררני של החלבון המוטנטי BRAF. מנגנון הפעולה של החלבון BRAF קשור לשפעול קולטן מסוג Tyrosine kinase, המתחיל שרשרת של אירועים תוך-תאיים במסלול RAF-RAS אשר מובילים לשגשוג של התאים ולהישרדותם. |
| − | בכ- 50 | + | בכ-50 אחוזים מחולי המלנומה הגרורתית קיימת מוטציה בגן BRAF. המוטציה גורמת לשפעול בלתי מבוקר של שרשרת האירועים וכתוצאה מכך מובילה לחלוקת תאים בלתי מבוקרת. |
| − | Zelboraf היא מולקולה | + | Zelboraf היא מולקולה (Molecule) קטנה המעכבת את הגן הפגום BRAF. עיכוב זה מונע מעבר של אותות להתחלקות התא ובכך מעכב את שגשוג התאים ומוביל לנסיגת הגידול. |
| − | יעילותה של Zelboraf בטיפול בחולי מלנומה מתקדמת בעלי מוטציה בגן BRAF הוכחה במחקר שלב III גדול, שכלל 675 חולים אשר טופלו בתכשיר כקו ראשון, מחקר | + | יעילותה של Zelboraf בטיפול בחולי מלנומה מתקדמת בעלי מוטציה בגן BRAF הוכחה במחקר שלב III גדול, שכלל 675 חולים אשר טופלו בתכשיר כקו ראשון, מחקר BRIM-3{{כ}} (BRAF Inhibitor in Melanoma 3){{כ}}{{הערה|שם=הערה1|Paul B. Chapman et al: Improved Survival with Vemurafenib in Melanoma with BRAF V600E Mutation. N Engl J Med. 2011 Jun 30;364(26):2507-16.}}. בנוסף הוכחה היעילות במחקרים נוספים בשלבים I/II גם עבור קווי טיפול מתקדמים {{כ}}{{הערה|שם=הערה2|Sosman JA et al: Survival in BRAF V600-mutant advanced melanoma treated with vemurafenib. N Engl J Med. 2012 Feb 23;366(8):707-14.}}{{הערה|שם=הערה3|Flaherty KT et al: Inhibition of mutated, activated BRAF in metastatic melanoma. N Engl J Med. 2010 Aug 26; 363(9):809-19.}}. |
| − | במחקר | + | במחקר BRIM-3 נבדקה יעילות Zelboraf לעומת הטיפול המקובל, [[Dacarbazine]]. התוצאות הדגימו שיפור מובהק בכל המדדים הקליניים: |
| − | *Zelboraf האריכה משמעותית את תוחלת החיים של החולים והפחיתה את הסיכון לתמותה ב- 56 | + | *Zelboraf האריכה משמעותית את תוחלת החיים של החולים והפחיתה את הסיכון לתמותה ב-56 אחוזים (יחס סיכונים=0.44{{כ}}, 0.001>p) |
| − | *לאחר 6 חודשים, 83 | + | *לאחר 6 חודשים, 83 חודשים מהמטופלים ב-Zelboraf נשארו בחיים, לעומת 63 אחוזים בזרוע הביקורת |
| − | *הסיכון להתקדמות המחלה במטופלי Zelboraf היה נמוך ב- 74 | + | *הסיכון להתקדמות המחלה במטופלי Zelboraf היה נמוך ב-74 אחוזים (יחס סיכונים=0.26{{כ}}, 0.001>p) לעומת זרוע הביקורת {{הערה|שם=הערה1}} |
| − | *הזמן החציוני עד להתקדמות המחלה (Progression-free survival) היה ארוך יותר פי 3 לעומת זרוע הביקורת: 5.3 לעומת 1.6 חודשים | + | *הזמן החציוני עד להתקדמות המחלה (Progression-free survival) היה ארוך יותר פי 3 לעומת זרוע הביקורת: 5.3 לעומת 1.6 חודשים |
| − | *תגובה כללית לטיפול ( | + | *תגובה כללית לטיפול (Overall response rate) ב-Zelboraf הודגמה ב-48 אחוזים מהמטופלים, לעומת 5 אחוזים בזרוע הביקורת (0.001>{{כ}}p{{כ}}). שיעור שליטה במחלה (Disease control rate) עמד על 85 אחוזים בזרוע Zelboraf לעומת 30 אחוזים בזרוע הביקורת |
| − | תוצאות אלה נתמכות בתוצאות מחקרי שלב I ו- II {{כ}}{{הערה|שם=הערה2}}{{הערה|שם=הערה3}}, אשר הדגימו הישרדות של 50 | + | תוצאות אלה נתמכות בתוצאות מחקרי שלב I ו- II {{כ}}{{הערה|שם=הערה2}}{{הערה|שם=הערה3}}, אשר הדגימו הישרדות של 58-50 אחוזים מהחולים לאחר שנה ו- 38 אחוזים לאחר שנתיים. |
| − | ניתן לייחס את אחוזי התגובה הגבוהים והירידה המשמעותית בתמותה (ירידה של 56 | + | ניתן לייחס את אחוזי התגובה הגבוהים והירידה המשמעותית בתמותה (ירידה של 56 אחוזים בסיכון לתמותה), שלא נצפו כמותם לפני כן, לעובדה שמדובר בטיפול ממוקד לחולים בעלי מוטציה בגן BRAF. תוצאות אלה מדגימות כי הבנת המנגנון הביולוגי של המחלה מאפשרת את התאמת הטיפול הנכון לחולה הנכון. |
[[קובץ:Melanoma-06.png|מרכז|320 פיקסלים]] | [[קובץ:Melanoma-06.png|מרכז|320 פיקסלים]] | ||
| + | |||
| + | חולים עם מחלה גרורתית מוגבלת (Oligometastatic; אתר אחד או מספר מוגבל של אתרים), יש להעריך האם ניתן לנתח ולהסיר את הגרורות. הסרה מלאה של הגרורות מיוחסת לשרידות גבוהה יותר בחלק מהמקרים. | ||
| + | |||
| + | טיפול סיסטמי (Systemic) מיועד לחולים אשר הסרה ניתוחית של הגרורות אינה מתאימה. | ||
| + | |||
| + | הטיפול העיקרי לחולים עם מלנומה גרורתית הוא: Checkpoint inhibitor immunotherapy, בעיקר הנוגדן Anti-Programmed cell Death 1{{כ}} (PD-1){{כ}} Pembrolizumab{{כ}}, Nivolumab לבד או בשילוב עם הנוגדן Anti-Cytotoxic T-Lymphocyte-Associated protein 4{{כ}} (CTLA-4){{כ}} Ipilimumab וכן טיפול ממוקד נגד במסלול ה-Mitogen-Activated Protein Kinase {{כ}}(MAPK). | ||
| + | |||
| + | נבון לתחילת שנת 2018, בחירת וסדר הטיפול לכל חולה וחולה חסר מידע תומך פרוספקטיבי (Prospective) וניתן בעיקר אמפירית (Empiric), כאשר הוא מבוסס על גורמים כגון מידת התפשטות המחלה, המאפיינים המולקולריים (Molecular) של הגידול (נוכחות Driver mutation ב- BRAF או KIT), מצבו התפקודי של החולה ומחלות נלוות. | ||
| + | |||
| + | לצורך בחירת הטיפול הסיסטמי, יש לבדוק חולים עם מלנומה גרורתית מתקדמת צריכים לנוכחות מוטציית V600 ''BRAF''. מלנומות Acral (של קצוות הגוף) או של הריריות אשר אינן מכילות את המוטציה V600 ''BRAF'' צריכות להיבדק גם לנוכחות מוטציית KIT כשניתן. | ||
| + | |||
| + | לחולים ללא מוטציית V600 BRAF, ההמלצה היא לטיפול אימונותרפי (Immunotherapy) עם Nivolumab, {{כ}} Pembrolizumab או שילוב של Nivolumab עם Ipilimumab. נכון לתחילת שנת 2018, לא ידוע איזו תת קבוצה תרוויח יותר משילוב או טיפול מונותרפי (Monotherapy) של שתי תרופות ברצף, כמו גם המינון ולוח הזמנים בטיפול המשולב, ישנו צורך בעבודות מחקר נוספות. טיפול ממוקד אינו מומלץ לחולים ללא המוטציה V600 ''BRAF.'' | ||
| + | |||
| + | כאשר ההתוויה היא לטיפול אימונותרפי, השילוב המועדף הוא של עיכוב Checkpoint על ידי Nivolumab יחד עם Ipilimumab, יותר מאשר טיפול בודד בנוגדן anti-PD-1, בחולים המסוגלים לעמוד בטיפול עם שילוב בעל רעילות אפשרית. | ||
| + | |||
| + | חולים עם המוטציה V600 ''BRAF'' אשר טופלו תחילה בטיפול מבוסס נוגדן anti-PD-1 ואשר מחלתם אינה ניתנת יותר לשליטה על ידי אימונותרפיה, ההמלצה היא לטיפול נוגד דרך MAPK {{כ}}(Mitogen-Activated Protein Kinase) יחד עם השילוב של דיכוי BRAF ו-MEK{{כ}} (Dabrafenib יחד עם Trametinib או Vemurafenib יחד עם Cobimetinib) ופחות לטיפול כימותרפי. | ||
| + | |||
| + | חולים עם המוטציה V600 ''BRAF'' ויכולת תפקודית ירודה, ההמלצה היא לטפל בטיפול ממוקד של דרך ה-MAPK{{כ}} (נוגד BRAF יחד עם נוגד MEK) יותר מאשר אימותרפיה. טיפול ממוקד קשור לתגובה מהירה ואמינה יותר במצב זה. אפשרות נוספת היא טיפול באימונותרפיה של מעכבי ה-Checkpoint; אימונותרפיה יכולה להיות אפשרות טיפולית כקו שני כאשר ישנה התקדמות המחלה או לאחר תגובה מירבית לטיפול ממוקד. | ||
| + | |||
| + | לחולים עם מוטציית KIT ומחלה אסימפטומטית, הטיפול במעכבי KIT{{כ}} (Imatinib) חשוב לחולים עם מחלה סימפטומטית או אשר אינם מועמדים לטיפול אימונותרפי, עם העדפה לטיפול כחלק ממחקר קליני. | ||
==פרוגנוזה== | ==פרוגנוזה== | ||
| − | הפרוגנוזה משתנה בהתאם לשלב המחלה. במידה ומדובר במחלה מקומית (שלבים 1 | + | הפרוגנוזה משתנה בהתאם לשלב המחלה. במידה ומדובר במחלה מקומית (שלבים 2-1), הפרוגנוזה היא מצוינת ועומדת על 98.2 אחוזי הישרדות לחמש שנים. ההישרדות לחמש שנים עבור מחלה אזורית (שלב 3) היא 61.7 אחוזים. מלנומה גרורתית (שלב 4) הינה מחלה תוקפנית וקטלנית המתקדמת במהירות ובעלת פרוגנוזה קשה במיוחד - פחות מ-10 אחוזים שורדים למשך 5 שנים, ורובם אינם שורדים 12 חודשים לאחר האבחנה. |
==דגלים אדומים== | ==דגלים אדומים== | ||
גרסה מ־12:47, 19 במאי 2018
| מלנומה | ||
|---|---|---|
| Melanoma | ||

| ||
| ICD-10 | Chapter C 43. | |
| ICD-9 | 172.9 | |
| MeSH | D008545 | |
| יוצר הערך | ||
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – מלנומה
מלנומה (Melanoma) היא הסוג החמור ביותר של סרטן עור ממאיר. זיהוי מוקדם של הנגעים הוא חשוב ביותר היות והפרוגנוזה (Prognosis) משתנה באופן משמעותי בהתאם לשלב גילוי המחלה - כמעט 100 אחוזים שורדים את המחלה כאשר היא מתגלה בשלבים מוקדמים, לעומת פחות מ- 10 אחוזי שרידות כאשר קיימות גרורות בעת האבחנה. הסימן הקליני המחשיד ביותר לממאירות הוא הופעת שומה חדשה בעלת צורה וצבע חריגים, או שינוי במאפייני שומה קיימת.
לאחר שנים רבות בהם הטיפול הניתן לחולי מלנומה גרורתית היה מוגבל ביותר, בשנות האלפיים חלה התקדמות רבה בטיפול המערכתי במלנומה. זאת בעקבות גילוי של מוטציות (Mutations) בגנים (Genes) שונים אשר אפשר טיפול ממוקד (Targeted) ומותאם לכל חולה.
אפידמיולוגיה
בעולם מתגלים קרוב ל-200,000 מקרים חדשים של מלנומה בשנה. בישראל מאובחנים מדי שנה כ-200 חולים עם מלנומה בשלב הגרורתי.
87 אחוזים מהחולים מאובחנים בשלב של מחלה מקומית (שלבים 2-1), 8 אחוזים בשלב בו המחלה מערבת בלוטות לימפה (Lymph nodes) אזוריות (שלב 3) ו-4 אחוזים בשלב בו קיימות גרורות (שלב 4).
אטיולוגיה
גורם הסיכון העיקרי למחלה הוא חשיפה לשמש, ובעיקר חשיפה שאינה קבועה ונעשית לפרקים. בנוסף, הסיכוי למלנומה גבוה יותר אצל בהירי שיער, עור ועיניים.
נוכחות של שומות שונות מעלה אף היא את הסיכוי להתפתחות מלנומה, בעיקר במצבים בהם קיימת שומה מולדת.
קליניקה
קיימים חמישה קריטריונים בסיסיים לזיהוי שומה החשודה כמלנומה:
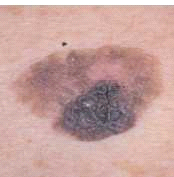
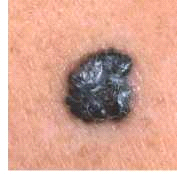
- א-סימטריה (Asymmetry): שומות רגילות הן בדרך כלל סימטריות, בעוד מלנומה עלולה להיות בעלת צורה לא סדירה או א-סימטרית
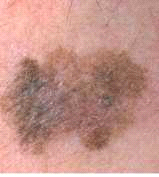
- גבול (Border): לשומות רגילות יש בדרך כלל גבול חלק ומוגדר. במלנומה גבולות השומה לא סדירים, מטושטשים או מחוספסים
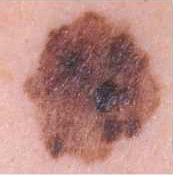
- גוון (Color): שומות רגילות הן בדרך כלל בצבע אחיד - חום. הגוון של מלנומה אינו אחיד, ושומה חשודה יכולה להופיע בשילוב של צבעים שונים - שחור, חום או חום-צהבהב, אדום, כחול ועוד
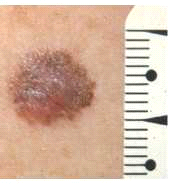
- גודל או קוטר (Diameter): שומות בקוטר של 5 מילימטרים ומעלה חשודות יותר כמלנומות
- שינוי (Evolution): הסימן החשוב ביותר. חשד למלנומה מתעורר כאשר מופיעה שומה חדשה וחריגה בצבע שחור, כאשר יש שינוי בגודלה, בצורתה, או בצבעה של שומה קיימת, או כאשר מופיע דימום או גרד בשומה, במיוחד אצל אנשים מעל גיל 40. לכן מעקב אחר שומות הוא הכרחי לאבחון מוקדם ולטיפול יעיל במחלה
אבחנה
האבחנה הסופית של מלנומה נעשית באמצעות ביופסיה (Biopsy) של הנגע החשוד.
טיפול
הטיפול במלנומה הוא בהתאם לשלב המחלה:
- שלבים 2-1: כריתה מקומית ודגימת בלוטת זקיף (Sentinel). במידה ומדובר בגידול באתר (In situ) ללא חדירה עמוקה וללא מאפיינים אגרסיביים, אין חובה לבצע דגימה של בלוטת הזקיף
- שלב 3: כריתה מקומית, כריתת בלוטות לימפה אזוריות וטיפול משלים
- שלב 4: טיפול מערכתי- עד לאחרונה הטיפולים במלנומה היו מוגבלים מאוד ולא ממוקדים או מותאמים אישית. בשנים האחרונות התגלה כי כ-50 אחוזים מהמלנומות הגרורתיות הן בעלות מוטציה בגן BRAF, הגורמת להיווצרות חלבון המעודד שגשוג בלתי-מבוקר של התאים הממאירים. נוכחות המוטציה BRAF מסתמנת כגורם פרוגנוסטי (Prognostic) שלילי להישרדות החולים
טיפול ממוקד במלנומה גרורתית- Zelboraf (Vemurafenib)
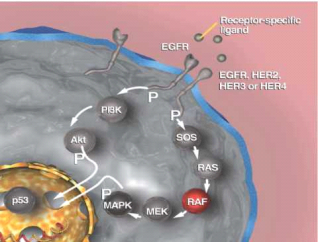
Zelboraf (Vemurafenib) הוא מעכב בררני של החלבון המוטנטי BRAF. מנגנון הפעולה של החלבון BRAF קשור לשפעול קולטן מסוג Tyrosine kinase, המתחיל שרשרת של אירועים תוך-תאיים במסלול RAF-RAS אשר מובילים לשגשוג של התאים ולהישרדותם.
בכ-50 אחוזים מחולי המלנומה הגרורתית קיימת מוטציה בגן BRAF. המוטציה גורמת לשפעול בלתי מבוקר של שרשרת האירועים וכתוצאה מכך מובילה לחלוקת תאים בלתי מבוקרת.
Zelboraf היא מולקולה (Molecule) קטנה המעכבת את הגן הפגום BRAF. עיכוב זה מונע מעבר של אותות להתחלקות התא ובכך מעכב את שגשוג התאים ומוביל לנסיגת הגידול.
יעילותה של Zelboraf בטיפול בחולי מלנומה מתקדמת בעלי מוטציה בגן BRAF הוכחה במחקר שלב III גדול, שכלל 675 חולים אשר טופלו בתכשיר כקו ראשון, מחקר BRIM-3 (BRAF Inhibitor in Melanoma 3)[1]. בנוסף הוכחה היעילות במחקרים נוספים בשלבים I/II גם עבור קווי טיפול מתקדמים [2][3].
במחקר BRIM-3 נבדקה יעילות Zelboraf לעומת הטיפול המקובל, Dacarbazine. התוצאות הדגימו שיפור מובהק בכל המדדים הקליניים:
- Zelboraf האריכה משמעותית את תוחלת החיים של החולים והפחיתה את הסיכון לתמותה ב-56 אחוזים (יחס סיכונים=0.44, 0.001>p)
- לאחר 6 חודשים, 83 חודשים מהמטופלים ב-Zelboraf נשארו בחיים, לעומת 63 אחוזים בזרוע הביקורת
- הסיכון להתקדמות המחלה במטופלי Zelboraf היה נמוך ב-74 אחוזים (יחס סיכונים=0.26, 0.001>p) לעומת זרוע הביקורת [1]
- הזמן החציוני עד להתקדמות המחלה (Progression-free survival) היה ארוך יותר פי 3 לעומת זרוע הביקורת: 5.3 לעומת 1.6 חודשים
- תגובה כללית לטיפול (Overall response rate) ב-Zelboraf הודגמה ב-48 אחוזים מהמטופלים, לעומת 5 אחוזים בזרוע הביקורת (0.001>p). שיעור שליטה במחלה (Disease control rate) עמד על 85 אחוזים בזרוע Zelboraf לעומת 30 אחוזים בזרוע הביקורת
תוצאות אלה נתמכות בתוצאות מחקרי שלב I ו- II [2][3], אשר הדגימו הישרדות של 58-50 אחוזים מהחולים לאחר שנה ו- 38 אחוזים לאחר שנתיים.
ניתן לייחס את אחוזי התגובה הגבוהים והירידה המשמעותית בתמותה (ירידה של 56 אחוזים בסיכון לתמותה), שלא נצפו כמותם לפני כן, לעובדה שמדובר בטיפול ממוקד לחולים בעלי מוטציה בגן BRAF. תוצאות אלה מדגימות כי הבנת המנגנון הביולוגי של המחלה מאפשרת את התאמת הטיפול הנכון לחולה הנכון.
חולים עם מחלה גרורתית מוגבלת (Oligometastatic; אתר אחד או מספר מוגבל של אתרים), יש להעריך האם ניתן לנתח ולהסיר את הגרורות. הסרה מלאה של הגרורות מיוחסת לשרידות גבוהה יותר בחלק מהמקרים.
טיפול סיסטמי (Systemic) מיועד לחולים אשר הסרה ניתוחית של הגרורות אינה מתאימה.
הטיפול העיקרי לחולים עם מלנומה גרורתית הוא: Checkpoint inhibitor immunotherapy, בעיקר הנוגדן Anti-Programmed cell Death 1 (PD-1) Pembrolizumab, Nivolumab לבד או בשילוב עם הנוגדן Anti-Cytotoxic T-Lymphocyte-Associated protein 4 (CTLA-4) Ipilimumab וכן טיפול ממוקד נגד במסלול ה-Mitogen-Activated Protein Kinase (MAPK).
נבון לתחילת שנת 2018, בחירת וסדר הטיפול לכל חולה וחולה חסר מידע תומך פרוספקטיבי (Prospective) וניתן בעיקר אמפירית (Empiric), כאשר הוא מבוסס על גורמים כגון מידת התפשטות המחלה, המאפיינים המולקולריים (Molecular) של הגידול (נוכחות Driver mutation ב- BRAF או KIT), מצבו התפקודי של החולה ומחלות נלוות.
לצורך בחירת הטיפול הסיסטמי, יש לבדוק חולים עם מלנומה גרורתית מתקדמת צריכים לנוכחות מוטציית V600 BRAF. מלנומות Acral (של קצוות הגוף) או של הריריות אשר אינן מכילות את המוטציה V600 BRAF צריכות להיבדק גם לנוכחות מוטציית KIT כשניתן.
לחולים ללא מוטציית V600 BRAF, ההמלצה היא לטיפול אימונותרפי (Immunotherapy) עם Nivolumab, Pembrolizumab או שילוב של Nivolumab עם Ipilimumab. נכון לתחילת שנת 2018, לא ידוע איזו תת קבוצה תרוויח יותר משילוב או טיפול מונותרפי (Monotherapy) של שתי תרופות ברצף, כמו גם המינון ולוח הזמנים בטיפול המשולב, ישנו צורך בעבודות מחקר נוספות. טיפול ממוקד אינו מומלץ לחולים ללא המוטציה V600 BRAF.
כאשר ההתוויה היא לטיפול אימונותרפי, השילוב המועדף הוא של עיכוב Checkpoint על ידי Nivolumab יחד עם Ipilimumab, יותר מאשר טיפול בודד בנוגדן anti-PD-1, בחולים המסוגלים לעמוד בטיפול עם שילוב בעל רעילות אפשרית.
חולים עם המוטציה V600 BRAF אשר טופלו תחילה בטיפול מבוסס נוגדן anti-PD-1 ואשר מחלתם אינה ניתנת יותר לשליטה על ידי אימונותרפיה, ההמלצה היא לטיפול נוגד דרך MAPK (Mitogen-Activated Protein Kinase) יחד עם השילוב של דיכוי BRAF ו-MEK (Dabrafenib יחד עם Trametinib או Vemurafenib יחד עם Cobimetinib) ופחות לטיפול כימותרפי.
חולים עם המוטציה V600 BRAF ויכולת תפקודית ירודה, ההמלצה היא לטפל בטיפול ממוקד של דרך ה-MAPK (נוגד BRAF יחד עם נוגד MEK) יותר מאשר אימותרפיה. טיפול ממוקד קשור לתגובה מהירה ואמינה יותר במצב זה. אפשרות נוספת היא טיפול באימונותרפיה של מעכבי ה-Checkpoint; אימונותרפיה יכולה להיות אפשרות טיפולית כקו שני כאשר ישנה התקדמות המחלה או לאחר תגובה מירבית לטיפול ממוקד.
לחולים עם מוטציית KIT ומחלה אסימפטומטית, הטיפול במעכבי KIT (Imatinib) חשוב לחולים עם מחלה סימפטומטית או אשר אינם מועמדים לטיפול אימונותרפי, עם העדפה לטיפול כחלק ממחקר קליני.
פרוגנוזה
הפרוגנוזה משתנה בהתאם לשלב המחלה. במידה ומדובר במחלה מקומית (שלבים 2-1), הפרוגנוזה היא מצוינת ועומדת על 98.2 אחוזי הישרדות לחמש שנים. ההישרדות לחמש שנים עבור מחלה אזורית (שלב 3) היא 61.7 אחוזים. מלנומה גרורתית (שלב 4) הינה מחלה תוקפנית וקטלנית המתקדמת במהירות ובעלת פרוגנוזה קשה במיוחד - פחות מ-10 אחוזים שורדים למשך 5 שנים, ורובם אינם שורדים 12 חודשים לאחר האבחנה.
דגלים אדומים
ביבליוגרפיה
- ↑ 1.0 1.1 Paul B. Chapman et al: Improved Survival with Vemurafenib in Melanoma with BRAF V600E Mutation. N Engl J Med. 2011 Jun 30;364(26):2507-16.
- ↑ 2.0 2.1 Sosman JA et al: Survival in BRAF V600-mutant advanced melanoma treated with vemurafenib. N Engl J Med. 2012 Feb 23;366(8):707-14.
- ↑ 3.0 3.1 Flaherty KT et al: Inhibition of mutated, activated BRAF in metastatic melanoma. N Engl J Med. 2010 Aug 26; 363(9):809-19.
- Zelboraf Israeli MoH approved prescribing information.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק