נוירופתיה מוטורית מולטיפוקאלית - Multifocal motor neuropathy
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – נוירופתיה
אלון אברהם
גבר בן 38 סבל מהופעת חולשה ביישור כף רגל ימין ובכפות הידיים, שהתפתחה בהדרגה במשך 6 השנים האחרונות. בבדיקתו נצפו דלדול בולט של שרירי כפות הידיים והרגליים, פסציקולציות בזרוע ובאמה מימין, חולשה קשה בכיפוף מרפק ימין וכן חולשה דיסטלית קשה בכפות הידיים, חולשת יישור כף רגל שמאל וחוסר מוחלט ביכולת ליישר את כף רגל ימין. בנוסף, לא הופקו החזרים, בעוד שבדיקת התחושה נמצאה תקינה על כל מרכיביה.
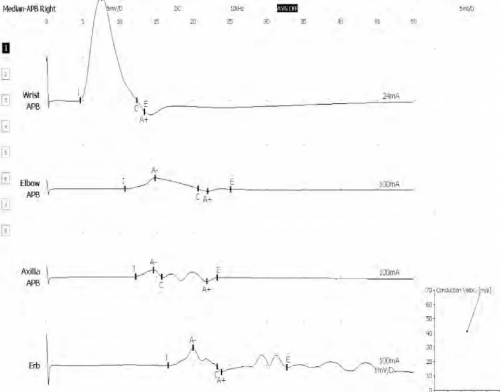
תמונה קלינית זו מכוונת למחלה מוטורית אסימטרית (מסוג Lower motor neuron - LMN) ללא מעורבות תחושתית. בבדיקה האלקטרודיאגנוסטית נצפו חסמי הולכה מוטורית חלקית (תמונה 1), ברובם הגדול של העצבים המוטורים בגפיים, בעוד שההולכות התחושתיות היו תקינות.
הקדמה
במסגרת הכינוס השנתי של האקדמיה האמריקאית לרפואה אלקטרודיאגנוסטית ב-1985 הציגו Parry ו- clark 3 חולים שסבלו מנוירופתיה מוטורית טהורה (ללא מעורבות סיבים תחושתיים), שפגעה בגפיים העליונות. חולים אלה אובחנו כסובלים ממחלת הנוירון המוטורי, אולם אף אחד מהם לא סבל ממעורבות שרירים בולבריים או שרירי נשימה. בבדיקה האלקטרופיזיולוגית נצפו חסמי הולכה קשים בסיבים מוטוריים בלבד, בעוד שמבחני ההולכה התחושתית היו תקינים לחלוטין[1].
|
טבלה 1. קריטריונים אבחנתיים ל-MMN[2] קריטריונים הכרחיים:
קריטריונים תומכים:
קריטריונים שאינם תומכים באבחנה:
|
ב-1988 היו Pestronk וחבריו הראשונים שטבעו את המונח Multifocal Motor Neuropathy לאבחנה חשובה זו2. סיבה אפשרית לכך שרק בשלב מאוחר יחסית התגבשה אבחנת MMN כהפרעה נפרדת ^ALS, יכולה להיות כשלון בזיהוי תבנית חולשת השרירים, שהנה בפיזור של עצבים היקפיים נפרדים, בניגוד לחולשה בפיזור של סגמנטים ספינליים 2-ALS. בנוסף, ייתכן כי חסמי ההולכה שנצפו בבדיקה האלקטרודיאגנוסטית בחולי MMN יוחסו לגורמים טכניים כגירוי תת אופטימלי של העצבים בנקודות גירוי פרוקסימליות, ונוכחות וריאנטים של עצבוב אנטומי1. הערכה קלינית ואלקטרופיזיולוגית שיטתית של קבוצות חולים גדולות אפשרה הבנה טובה יותר של הפתופיזיולוגיה של המחלה ומציאת דרכי טיפול יעילות בה. הטיפול המוצלח :-IVIG הווה את אבן הפינה בטיפול במחלה זו ומהווה עד היום את ^gold standard לטיפול בה3. קריטריונים אבחנתיים שנקבעו על ידי אגודות אמריקאיות ואירופאיות למחלה זו, מאפשרים להבדיל בין MMN למחלת הנוירון המוטורי ונוירופתיות נוספות, ^Chronic inflammatory demyelinating) CIDP Multifocal acquired demyelinating) MADSAM-1 (neuropathy Lewis-Sumner syndrome) (sensory and motor neuropathy) (טבלה) . למרות ההתקדמות שחלה באפיון המחלה ובאופן הטיפול בה, נותרו מספר שאלות פתוחות, כגון מהי האטיולוגיה למחלה, הבסיס הביולוגי לחסמי ההולכה, ואופן הטיפול האופטימאלי לטווח ארוך3.
פתוגנזה ההנחה היא כי MMN הנה מחלה דלקתית, כאשר התגובה לטיפול ^IVIG ומספר נקודות דמיון לתסמונת גיליאן ברה והווריאנט המוטורי אקסונלי שלה Acute motor axonal neuropathy) AMAN) תומכות בהשערה זו. יש 2 נקודות דמיון בין AMAN-7 MMN. הראשונה היא נוכחות נוגדנים כנגד הגליקוליפיד GM1, המבוטא במערכת העצבים ההיקפית בסרום של מספר משמעותי של חולים, והשנייה הנה נוכחות חסמי הולכה ופגיעה אקסונלית המשותפת לשתיהן. ניתן למצוא את הנוגדנים כנגד GM1 בכמחצית מחולי GM1 .MMN הנו גליקוליפיד ממשפחת הגנגליוזידים ומצוי בייחוד באזורים פאראנודליים במערכת העצבים ההיקפית. ניתן למצוא נוגדנים כנגד גנגליוזידים במגוון נוירופתיות דלקתיות נוספות, כולל תסמונת גיליאן ברה. בניגוד 7-AMAN הנגרמת מזיהום מקדים, הגורם להיווצרות נוגדנים פתוגנים במנגנון של דמיון מולקולרי, לא ידוע מה הגורם להיווצרות נוגדנים כנגד .4MMN^ GM1 מאפיינים קליניים MMN הנה מחלה נדירה ושכיחותה המוערכת היא 1-2/100,000. הגיל הממוצע למחלה זו הנו 40, כאשר 80% מהלוקים בה מפתחים את הסימפטומים הראשונים של המחלה בגילאים 20-50. המחלה שכיחה יותר בגברים, ביחס של 33:1. מבחינה קלינית מתאפיינת מחלה זו בהתפתחות הדרגתית איטית, או בשלבים, של חולשה אסימטרית דיסטלית בפיזור של עצבים היקפיים, אולם, בשלבים מאוחרים יותר, בהם ישנה חולשה מפושטת, קשה להבדיל בין דפוס החולשה המתואר, לחולשה בפיזור של סגמנטים ספינליים כבמחלות נוירון מוטורי. בניגוד לכך, דמיון לפולינוירופתיה סימטרית כבמקרים של מונונויריטיס מולטיפלקס מפושטת, הנו נדיר1. הגפיים העליונות הן אלה שמעורבות לרוב הן בשלב מוקדם יותר, והן בצורה קשה יותר. חולשה בפיזור פרוקסימלי תיתכן אף היא, אולם בשכיחות נמוכה יחסית, של כ-10%-5% מהמקרים בלבד3. הביטוי השכיח ביותר של MMN הנו צניחת כף יד וחולשה ביכולת הלפיתה, כאשר דיווחים מסוימים מצביעים על כך שחולשה ביישור אצבעות היד עם מעורבות דיפרנציאלית של אגדים שונים בתוך העצב, מהווים ביטוי שכיח המחשיד למחלה זו1. דלדול שרירים אם קיים, קל לרוב בשלבים ההתחלתיים של המחלה, בהם הפגיעה האקסונלית מזערית, ומהווה רמז אבחנתי חשוב למחלה זו. בשלבים מאוחרים יותר של המחלה, בהם ישנו נזק אקסונלי משני משמעותי לסיבים המוטוריים, ניתן למצוא דלדול שרירים בולט יותר, כאשר בשלב זה התגובה לטיפול אימונומודולוטורי טובה פחות. סימפטומים נוספים הקיימים בקרוב למחצית מהחולים הנם פסציקולציות והתכווצויות שרירים (muscle cramps), כאשר לעיתים ניתן לראות מיוקימיה. מעצם הגדרתה של המחלה, ניתן להסיק כי אין סימפטומים תחושתיים בה, אולם מיעוט מהחולים מדווח על הפרעות בתחושה ואובדן תחושת רטט תועד בעד 20% מחולי MMN. במקרים כאלה קיים משנה חשיבות להדגמת הולכות תחושתיות תקינות בבדיקה האלקטרודיאגנוסטית. ההחזרים הגידיים לרוב מופחתים, אולם יכולים להיות תקינים ובמקרים מסוימים אף ערים ולהקשות על היכולת להבדיל מחלה זו ממחלת הנוירון המוטורי. מעורבות עצבי הגולגולת אינה שכיחה, ואם קיימת, מערבת לרוב בעיקר את עצב הלשון (hypoglossus) וגורמת לדלדול במחצית הלשון3.
בדיקות עזר אבחנתיות בדיקות אלקטרופיזיולוגיות הולכות עצביות: הממצא האופייני ביותר 7-MMN הנו נוכחות חסמי הולכה מוטוריים (תמונה 1), באזורים שאינם אופייניים ללכידת עצבים (כתעלה האולנרית או הקרפלית), בשני עצבים או יותר, בנוכחות הולכות תחושתיות תקינות (תרשים). אבחנת MMN ללא נוכחות חסמי הולכה מאתגרת הרבה יותר, ודורשת היכרות מעמיקה של המיוטומים והעצבים ההיקפיים השונים, כך שניתן יהיה לאתר את הבסיס האנטומי לחסרים המוטוריים1.
באופן כללי, חסמי הולכה מוטוריים מוגדרים כירידה באמפליטודה או בשטח מתחת לעקומה של ^compound muscle action) CMAP potential), בגירוי פרוקסימלי, ביחס לגירוי דיסטלי, אולם אין קונצנזוס באשר לגובה הירידה הנדרש באמפליטודה או השטח מתחת לעקומת ^CMAP, ולרוב מקובל לדבר על ירידה של מעל ל-50%. הסיבה לכך שישנה מחלוקת באשר לגובה הירידה הנדרשת באמפליטודה או בשטח שמתחת לעקומת ^CMAP נובע בראש וראשונה מכך שגורמים נוספים עשויים לחקות חסמי הולכה. בפולינוירופתיות דמילינטיביות ישנה מהירות הולכה שונה בין סיבי העצב השונים, תופעה הקרויה פיזור טמפורלי. במצב זה, פאזה חיובית של פוטנציאל פעולה השייך ליחידה מוטורית אחת עשוי לחפוף לפזה שלילית של פוטנציאל פעולה של יחידה מוטורית איטית יותר, ולגרום 7-phase cancellation ולירידה באמפליטודה. דיפיציה טמפורלי נמצא במחלות דמילינטיביות נרכשות של מערכת העצבים ההיקפית, :-CIDP. בנוסף, עצבוב קולטרלי (Collateral sprouting) המתרחש במחלות כגון מחלת הנוירון המוטורי יכול לגרום ליחידות מוטוריות פוליפזיות, ובכך לאמפליטודה נמוכה יותר. ולבסוף, מגבלות טכניות כגירוי חשמלי שאינו סופרמקסימלי באזורים פרוקסימליים הנגישים פחות לגירוי חשמלי, יכול אף הוא לדמות חסם הולכה3. אלקטרומיוגרפיה: על אף ^MMN הנה הפרעה דמילינטיבית בעיקרה, אובדן אקסונים מוטוריים מתרחש ללא יוצא מהכלל ומתבטא בנוכחות פעילות ספונטנית כפיברילציות וגלים חיוביים חדים, וכן ביחידות מוטוריות גדולות ופוליפזיות בזמן הפעלה רצונית של השריר. על אף שאובדן אקסונים מוטוריים מתרחש במידה משמעותית בחולים שאינם מטופלים, נראה כי גם בחולים מטופלים היטב ישנו אובדן אקסונים מוטוריים עם הזמן. בשלבים ראשוניים של המחלה ניתן למצוא מיעוט פעילות ספונטנית בלבד בשרירים חלשים שטרם עברו אטרופיה, אולם ניתן לראות בהם גיוס ירוד. בשרירים בהם התרחשה אטרופיה, ניתן למצוא סימני דנרבציה חדה, ופעמים רבות גם פסציקולציות ובמקרים מסוימים מיוקימיה. בניגוד למחלת הנוירון המוטורי, בה ניתן למצוא סימני דנרבציה מפושטת אף בשרירים ללא חולשה קלינית, :-MMN סימני הדנרבציה החדה מוגבלים לרוב לשרירים החלשים בלבד1. ממצאים מעבדתיים הממצא המעבדתי השכיח ביותר הנו נוכחות נוגדנים בסרום מסוג 1gM כנגד הגנגליוזיד GM1, הנמצא בטיטרים גבוהים ב-80%-30% מהחולים. הסיבה לערכים שונים בדיווחים שונים נובעת קרוב לוודאי משיטות ELISA שונות במחקרים השונים, וכן להטרוגניות של אוכלוסיות הבקרה . נוגדנים כנגד GM1 אינם ספציפיים 7-MMN וניתן למוצאם ב-10%-5% מחולי מחלת הנוירון המוטורי, וכן בנוירופתיות דמילינטיביות נוספות כתסמונת גיליאן ברה -CIDP, ואף באנשים בריאים. בשני שלישים מהחולים ניתן למצוא ערכי CK גבוהים במקצת, ממצא שאינו ספציפי ואינו עוזר להבדיל בין MMN למחלת נוירון מוטורי או נוירופתיות אחרות. בבדיקת נוזל השדרה ניתן למצוא רמת חלבון מעט גבוהה (עד 80 מ"ג/ד"ל), עם ספירת תאים תקינה3. ביופסיית עצב ביופסיית עצב תחושתי, כעצב סורלי, באופן טבעי אינה תורמת כמובן לאבחנת MMN, וצריכה להתבצע רק אם נמצא וישנם חסרים תחושתיים משמעותיים, או חשד למחלה אחרת —C1DP או וסקוליטיס3. MRI בקרוב למחצית מהחולים ניתן למצוא אות גבוה במקלעת הברכיאלית ברצף T2, או ברצף T1 לאחר מתן גדוליניום. על אף שממצא זה אינו ספציפי ואינו חושף את הפתופיזיולוגיה בבסיס הנזק, למעט הדגמת בצקת ופגיעה במחסום הדם עצב. בדיקת MRI יכולה להפוך בעתיד לכלי אלגנטי ולא פולשני להערכת השלמות של סגמנטים עצביים פרוקסימליים3. טיפול אפשרויות הטיפול :-MMN מוגבלות2. בניגוד 7-MMN ,CIDP אינה מגיבה לטיפול בסטרואידים או פלסמפרזיס, אשר אף עלולים להחמיר את הסימפטומים בכ-20% מהמקרים. טיפול :-IVIG הנו הקו הטיפולי הראשון במחלה זו ויעילותו הוכחה במספר מחקרי RCT, כאשר יעילות הטיפול מוערכת ב-86%-70% מהחולים. התועלת הקלינית בטיפול זה לרוב מרשימה, ושיפור הדרגתי בכוח השרירים מתרחש כבר בשבוע הראשון לטיפול. אם לא חל שיפור יש לשקול קיום אבחנה אחרת, אם כי חולשת שרירים המלווה בדלדול שלהם לרוב אינה משתפרת לאחר מתן IVIG. המינון המקובל בתחילת הטיפול במחלה זו הנו 2 גי/ק"ג המחולקים ל-5-2 ימים רצופים. בשל נטייה לירידה מהירה ביעילות הטיפול לאחר מספר שבועות, יש להתאים את מינון הטיפול בהמשך באופן פרטני במטרה למקסם את היחס בין העלות לתועלת. מגוון טיפולים אימונומודולטוריים ואימונוסופרסיביים אחרים, כגון אזטיופרין, מטוטרקסט, ציקלופוספמיד ואחרים, לא הראו ממצאים חד משמעיים3. סיכום מספר רב של מחקרים קליניים ואלקטרופיזיולוגיים בשנים האחרונות הביא להבנה טובה יותר של הפתופיזיולוגיה של MMN ולהתקדמות משמעותית באבחנה ובטיפול במחלה זו. טיפול :-IVIG יכול לשפר את כוח השריר ולעכב את התפתחות המחלה, אולם טיפולים יעילים לטווח הארוך, או טיפולים שיביאו להחלמה מהמחלה עדיין חסרים. ד"ר אלון אברהם, המחלקה לנוירולוגיה, המרכז הרפואי ת"א
3. Meuth SG, Kleinschnitz C, Europ Neurology, 2010:63,193
4. Vlam L, van den Berg LH, Cats EA et al., J. Clin. Immunol, 2013 Jan:33 Suppl 1:38
- ↑ Muley SA, Parry GJ, J. Clin. Neurosci, 2012: 19,1201
- ↑ European Federation of Neurological Societies/Peripheral Nerve Society guideline on management of multifocal motor neuropathy. Report of a joint task force of the European Federation of Neurological Societies and the Peripheral Nerve Society-first revision. JPNS. 2010, 15,:295


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק