סוכרת הריונית - אבחון וטיפול - Gestational diabetes - diagnosis and treatment
| סוכרת הריונית - אבחון וטיפול | ||
|---|---|---|
| Gestational diabetes - diagnosis and treatment | ||

| ||
| שמות נוספים | סוכרת הריונית – קריטריונים לאבחון, סוגי הטיפול וניהול המחלה במהלך ההיריון | |
| ICD-10 | Chapter O 24. | |
| ICD-9 | 648.8 | |
| MeSH | D016640 | |
| יוצר הערך | פרופ' משה הוד וד"ר אמיר אבירם | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סוכרת והיריון
סוכרת משפיעה על עד 10% מהנשים ההרות[1],[2],[3],[4], ורובן המכריע (85-95%) מאובחנות במהלך ההיריון ועל כן נחשבות ללוקות בסוכרת הריונית[2],[5].
בעבר, הרה שאובחנה כלוקה בסוכרת במהלך ההיריון הוגדרה כלוקה בסוכרת הריונית[6],[7], ללא קשר לסוג הסוכרת שאובחן.
עם העלייה בשכיחות השמנת היתר בעולם המערבי, כך גם שכיחות הסוכרת בכלל והסוכרת ההריונית בפרט הולכת ועולה. בנוסף, קריטריונים חדשים להגדרת סוכרת הריונית נמצאים בשלבים אלה בתהליכי הטמעה בעולם ויישומם עלול להעלות בעד פי שניים את שכיחות הסוכרת ההריונית.
הטיפול בסוכרת הריונית הוא טיפול רב-תחומי (Multidisciplinary) המערב מומחה להיריון בסיכון, אנדוקרינולוג, אחות ליווי היריון ודיאטנית. נוכח פרק הזמן המוגבל להתערבות (משבוע 24-28 ועד לתום ההיריון), נדרשים טיפול ומעקב אינטנסיביים על מנת למנוע סיבוכים אימהיים ועובריים. ארסנל הכלים כולל הן טיפול תזונתי והן טיפול תרופתי (פומי או באינסולין), והשליטה בגישות השונות חשובה הן להשגת יעדי המטרה הגליקמיים והן למתן הסברים מושכלים ומכוונים למטופלת אשר נחשפת לעולם המושגים הסוכרתי לראשונה בהיריון.
עם השנים, גישות חדשות מתחום המחקר בסוכרת מוצאות את דרכן גם לעולם הסוכרת ההריונית, ויותר ויותר מחקרים עוסקים בניטור גלוקוז רציף באמצעות חיישנים מיוחדים (Sensors) וכן בטיפול באינסולין במשאבות. נראה שגם כלים אלה יבססו את דרכם אט אט לארסנל הכלים וייתכן שבסופו של דבר יתאפשר טיפול אשר יחקה את הפיזיולוגיה של הפרשת האינסולין האנדוגנית מחד ויפחית למינימום את סיבוכי הסוכרת מאידך.
קריטריונים לאבחון סוכרת הריונית
הקריטריונים המקוריים (והקיימים כיום) לאבחון סוכרת הריונית מתבססים על גישת שני השלבים. בשלב הראשון מבוצעת העמסת סוכר של 50 גרם כבדיקת סקר, ותוצאה ≥140 מ"ג/ד"ל (מיליגרם/דציליטר) נחשבת לתוצאה חיובית. במקרה שהתוצאה חיובית, מתבצעת העמסת סוכר של 100 גרם, שבה תוצאה לא תקינה אחת נחשבת לאבחנתית, לפי הסעיפים הבאים: 95 מ"ג/ד"ל, 180 מ"ג/ד"ל, 155 מ"ג/ד"ל ו-140 מ"ג/ד"ל (בצום, לאחר שעה, שעתיים ושלוש שעות, בהתאמה) (טבלה מספר 1). בהעמסת הסוכר הראשונה, של 50 גרם גלוקוז, הסף שהוחלט הוא שרירותי ונקבע על פי יכולתו לנבא תוצאה חיובית בהעמסת הסוכר של 100 גרם. רגישותו 85% ואילו סגוליותו 86%. במקרה שהסף מופחת ל-130 מ"ג/ד"ל, רגישותו 99% אולם סגוליותו 77% בלבד[8],[9].
בשנת 2010 פורסמו הקריטריונים החדשים לאבחון סוכרת הריונית על ידי International Association of Diabetes and Pregnancy Study Group (IADPSG) ובהם הוחלט לסווג את הנשים המאובחנות במהלך ההיריון לשתי קטגוריות: סוכרת גלויה (Overt) או הריונית (Gestational)[10]. בהמשך, האיגוד האמריקאי לסוכרת (ADA, American Diabetes Association) אימץ את הקריטריונים החדשים (שמעלים את שיעור אבחון הסוכרת ההריונית ל-18% בקירוב)[10],[11],[12]. הסיבה לסיווג לשתי הקטגוריות נעוצה בשכיחות המתגברת של סוכרת לא מאובחנת בקרב נשים צעירות, בעיקר בשל העלייה בשכיחות השמנת היתר, כך שפלח נרחב יותר מהנשים לוקה בסוכרת עוד טרם ההיריון אולם לא מאובחן. בנוסף, סוכרת גלויה מהווה גורם סיכון להתפתחות מומים עובריים ולהתפתחות סיבוכים אימהיים במהלך ההיריון, לכן יש חשיבות עליונה לזיהוי הסוכרת מוקדם.
לפי הגדרות אלו, סוכרת גלויה מאובחנת במפגש הראשון של ההרה עם המערכת הרפואית אם אחד מהתנאים הבאים מתקיים: רמת הגלוקוז בצום ≥126 מ"ג/ד"ל, רמת ההמוגלובין המסוכרר (HgA1C, Hemoglobin A1C) ≥6.5%, או רמת גלוקוז במדידה אקראית ≥200 מ"ג/ד"ל (שלאחר מכן מאושררת ברמת גלוקוז בצום או בדיקת המוגלובין מסוכרר).
אבחון סוכרת הריונית מתבסס על הקריטריונים הבאים: רמת גלוקוז בצום ≥92 מ"ג/ד"ל (אולם נמוכה מ-126 מ"ג/ד"ל) בכל גיל היריון, או העמסת סוכר של 75 גרם בשבועות 24-28 שבה הערך בצום ≥92 מ"ג/ד"ל, הערך לאחר שעה ≥180 מ"ג/ד"ל או הערך לאחר שעתיים ≥153 מ"ג/ד"ל[8].
| העמסת סוכר | צום | לאחר שעה אחת | לאחר שעתיים | לאחר שלוש שעות | |
|---|---|---|---|---|---|
| קריטריונים קיימים | 100 גרם | >95 מ"ג/ד"ל | >180 מ"ג/ד"ל | >155 מ"ג/ד"ל | >140 מ"ג/ד"ל |
| קריטריונים מוצעים | 75 גרם | >92 מ"ג/ד"ל | >180 מ"ג/ד"ל | >153 מ"ג/ד"ל | - |
הסיבה בגינה הוחלט לשנות את הקריטריונים האבחנתיים נעוצה במחקר Hyperglycemia and Adverse Pregnancy Outcome (HAPO)[13] שבחן את התוצאות ההריוניות של היפרגליקמיה (Hyperglycemia) (בניגוד לקריטריונים הישנים שהתבססו על סיכוי האם לפתח סוכרת בעתיד) ומצא שיש קשר ליניארי בין רמת ההיפרגליקמיה לבין תוצאות הריוניות תת מיטביות. בשל הקשר הליניארי, הקריטריונים החדשים נקבעו על בסיס קונצנזוס מומחים.
גורמי סיכון לסוכרת הריונית וסיבוכים
גורמי סיכון לסוכרת הריונית כוללים כל הרה בת 25 ומעלה, השתייכות לקבוצה אתנית בת סיכון (היספנים, אפריקאים, מזרח או דרום אסיה), מדד גוף-מסה (BMI, Body Mass Index) גבוה מ-25, ללא היסטוריה קודמת של תנגודת לאינסולין או היריון עם סוכרת הריונית או אחד מסיבוכיה המוכרים, וללא היסטוריה של קרוב משפחה דרגה ראשונה הסובל מסוכרת[8].
סיבוכי הסוכרת כוללים סיכון מוגבר לפיתוח הפרעות לחץ דם בהיריון, מקרוזומיה עוברית, סיכון מוגבר ללידה מכשירנית או ניתוח קיסרי, פרע כתפיים (Shoulder dystocia) וטראומה במהלך הלידה.
מכאן, שהסיבה לטיפול בסוכרת הריונית נעוצה ביכולת הטיפול להפחית את סיבוכי הסוכרת. במחקר של Langer וחבריו[14] הושוו 555 נשים עם סוכרת הריונית לא מטופלת ל-1,110 נשים עם סוכרת הריונית מטופלת ול-1,110 נשים נוספות ללא סוכרת הריונית. נמצא כי להרות עם סוכרת הריונית לא מטופלת סיכון של 59% לתוצאה הריונית תת מיטבית, לעומת 18% בקרב הרות עם סוכרת הריונית מטופלת ו-11% בקרב הרות ללא סוכרת הריונית, וסיכון גבוה פי שניים עד ארבעה להפרעות מטאבוליות וילוד גדול לגיל ההיריון (LGA, Large for Gestational Age) או ילוד מקרוזומי.
שני מחקרים תצפיתיים אקראיים השוו נשים שאובחנו עם סוכרת הריונית וטופלו מול נשים שאובחנו עם סוכרת הריונית ולא טופלו[15],[16]. למרות ששני המחקרים נבדלו זה מזה במעט באופן אבחון הסוכרת ההריונית, בשניהם נמצא כי הטיפול הפחית באופן משמעותי את שיעורי המקרוזומיה העוברית ופרע הכתפיים על שלל סיבוכיו (שיתוק עצבי, שבר גרמי ומוות), וכי נשים בקבוצת הטיפול העלו במשקלן פחות וסבלו פחות מהפרעות לחץ דם. באחד המחקרים נמצא ששיעור הניתוחים הקיסריים היה נמוך יותר בקבוצת הטיפול[16] ואילו במחקר השני נמצא ששיעור הניתוחים הקיסריים דומה[15]. עם זאת, הטיפול לא הפחית באופן משמעותי את שיעור הסיבוכים המטאבוליים הנאונטליים.
טיפול בסוכרת הריונית
הטיפול ההריוני בסוכרת, פרט למעקב אחרי רמות הגלוקוז, מסווג לשני סוגים: טיפול תזונתי וטיפול תרופתי.
הטיפול התזונתי
ה-ADA ממליץ שהטיפול התזונתי להרות הלוקות בסוכרת הריונית יספק תזונה נאותה לקידום הבריאות האימהית והעוברית תוך השגת רמות גלוקוז נורמליות ללא קטונים (Ketones), ויספק רמות מספקות של אנרגיה לעלייה נאותה במשקל במהלך ההיריון[17]. הרות שמשקלן תקין צורכות 30 קק"ל (קילו קלוריות) לק"ג (קילוגרם) משקלן ביום, בעוד שהרות במשקל עודף נצרכות ל-22-25 קק"ל לק"ג משקלן ביום והרות הסובלות מהשמנת יתר – ל-12-14 קק"ל לק"ג משקלן ביום.
תצרוכת הפחמימות מוגבלת עד ל-40% מסך הקלוריות ומחולקת בין הארוחות העיקריות וארוחות הביניים לאורך היום למניעת היפרגליקמיה[18]. לרוב מומלצות שלוש ארוחות בינוניות עיקריות ועוד שתיים עד ארבע ארוחות ביניים קלות. מומלץ להגביל את כמות הלחם, אורז, דגנים, פסטה, תפוחי האדמה ומיצים ופירות מתוקים. פחמימות מורכבות יותר, בעלות אינדקס גליקמי נמוך (עמילן וירקות), עשירות יותר במרכיבים תזונתיים ומעלות את רמות הגלוקוז שלאחר הארוחה (Postprandial Glucose) פחות מאשר סוכרים פשוטים. שאר הקלוריות מחולקות בין שומנים (40%) וחלבונים (20%).
במהלך הטיפול התזונתי יש להמשיך ולבצע ניטור הדוק של רמות הגלוקוז על מנת לוודא כי הטיפול התזונתי אכן יעיל בהשגת רמת גלוקוז נורמלית. דרך יעילה לבחון את יעילות הטיפול היא למדוד את משקלה של ההרה. במחקר שבדק מעל 31,000 הרות נמצא כי עלייה תקינה במשקל (לעומת עלייה יתרה במשקל) מפחיתה את הסיכון ליילוד LGA, ללידה מוקדמת ולניתוחים קיסריים[19].
גם בקרב הרות שבהן עלה חשד לסוכרת הריונית אולם הן לא עמדו בקריטריונים האבחנתיים (לדוגמה, העמסת סוכר של 50 גרם חיובית עם העמסת סוכר של 100 גרם שלילית, או עם ערך פתולוגי בודד) יש חשיבות לטיפול, ונשים אלו נמצאות אף הן בסיכון לילוד LGA[20].
ניטור רמת הגלוקוז
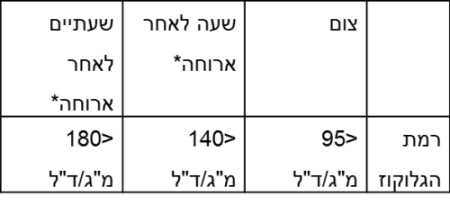
רמת הגלוקוז צריכה להימדד ולהירשם בקפידה לצד הצריכה הקלורית, לכל הפחות ארבע פעמים ביום: בצום ושעה או שעתיים לאחר תחילת כל ארוחה[21]. המדידות מאפשרות מעקב הדוק אחרי רמת האיזון הגליקמי ומאפשרות לאבחן נשים אשר נדרשות לטיפול תרופתי[22]. איזון מיטבי מוגדר כרמת גלוקוז בדם הנמוכה מהערכים הבאים: 95 מ"ג/ד"ל בצום, 140 מ"ג/ד"ל שעה לאחר תחילת הארוחה ו-120 מ"ג/ד"ל שעתיים לאחר תחילת הארוחה[23] (טבלה מספר 2). כאשר ערכים אלה אינם מושגים, יש להתחיל טיפול תרופתי.
עם זאת, אין כלל הסכמה גורפת לגבי המושג "איזון תת מיטבי": יש הגורסים כי אם 20% מהמדידות לאורך שבוע אינן תקינות, אזי מדובר באיזון תת מיטבי, בעוד אחרים טוענים שדי בשתי מדידות לא תקינות בפרק זמן של שבועיים.
מחקר HAPO מצא קשר המשכי בין רמות הגלוקוז לבין תוצאות הריוניות תת מיטביות, כאשר רמת גלוקוז בצום >150 מ"ג/ד"ל כרוכה בסיכון גבוה פי חמישה למקרוזומיה מאשר רמת גלוקוז נמוכה מ-75 מ"ג/ד"ל (25% מול 5%)[13]. עדיין לא ברור לחלוטין אם הפחתת יעדי המטרה לאיזון גליקמי תפחית גם את שיעור המקרוזומיה ושיעור הילודים LGA, אולם ידוע כי איזון ביתר עלול להוביל ללידת ילודים קטנים למועד (קטן לגיל היריון, Small for Gestational Age)[24].
לגבי מדידת המוגלובין מסוכרר - היא רלבנטית לאבחון סוכרת גלויה בתחילת ההיריון, אך לא ברור בשלב זה אם מדידות סדרתיות של המוגלובין מסוכרר יעילות במהלך הניהול של סוכרת הריונית.
פעילות גופנית סדרתית משפרת את הרגישות לאינסולין ויכולה לסייע להשגת רמות גלוקוז תקינות במהלך הטיפול בסוכרת הריונית. מחקר רנדומלי אחד מצא שיפור הן ברמות הגלוקוז בצום והן ברמות הגלוקוז לאחר ארוחות בנשים שקיימו פעילות גופנית מסודרת (20 דקות ביום במשך שלושה ימים בשבוע), אולם מחקרים אחרים מצאו תוצאות מעורבות[25]. עם זאת, מקובל שפעילות גופנית מסודרת היא בעלת יתרונות לנשים עם סוכרת הריונית.
הטיפול התרופתי
במקרה שלא ניתן להשיג רמות גלוקוז תקינות במהלך הטיפול התזונתי, יש להתחיל טיפול אנטי-היפרגליקמי תרופתי[26]. האפשרויות הקיימות לטיפול תרופתי כיום כוללות טיפול באינסולין (הטיפול היחיד המומלץ בארצות הברית[21] או טיפול בתרופות פומיות, כמקובל בין השאר בישראל).
אינסולין - מינון האינסולין משתנה בין אוכלוסיות שונות בהתאם למצוא האתני, לדרגת ההשמנה, לרמת ההיפרגליקמיה ומאפיינים דמוגרפיים נוספים. עם זאת, רוב המחקרים תומכים במינון אינסולין של 0.7-2 יחידות לק"ג משקל גוף על מנת להשיג שליטה גליקמית, כאשר על כל שתי יחידות של אינסולין בטווח פעולה בינוני או ארוך, יש לתת יחידה אחת של אינסולין בטווח פעולה קצר. יחס זה של 2:1 מתאים לדפוס הפרשת האינסולין בנשים ללא סוכרת הריונית בטרימסטר השלישי[27]. התאמת המינון היומי בהתאם לכל ארוחה יכולה להסתמך על עקרונות כלליים:
- במטופלות עם רמת גלוקוז מוגברת בעיקר לאחר ארוחות יש להתחיל טיפול בבוקר
- אם רמת הגלוקוז לאחר ארוחת הערב/צהריים עדיין גבוהה, יש להוסיף אינסולין קצר טווח לפני הארוחה
- אם רמת הגלוקוז בצום גבוהה, יש להוסיף אינסולין בעל טווח פעולה בינוני או ארוך בערב
כלומר, במקרה של חוסר איזון, ניתן להגיע לכל היותר למשטר של ארבע זריקות ביום, המשפר את רמת האיזון הגליקמי ואת התוצאות המיילדותיות בהשוואה למשטר של שתי זריקות ביום, אם כי אינו משפר את שיעור המקרוזומיה[28].
ההתאמה של רמת האינסולין לרמת הגלוקוז בדם מתבצעת על בסיס מדידות רמת הגלוקוז בדם ארבע עד שש פעמים ביום (בצום ולאחר כל ארוחה, וניתן להוסיף מדידות נוספות לפני ארוחת הצהריים או ארוחת הערב), על מנת להשיג יחס אופטימלי בין מינון האינסולין לרמת הגלוקוז. יש לזכור שככל שההיריון מתקדם, דרישות האינסולין של הגוף משתנות ולכן יש להתאים את המינון גם לכך. הסיכוי להיפוגליקמיה (Hypoglycemia) בסוכרת הריונית הוא קלוש ויכול להיות מטופל באמצעות חטיף פחמימות וחלבונים של 10-20 גרם. עם זאת, אירועי היפוגליקמיה מחייבים התאמה מחדש של מינון האינסולין.
מבחינת סוגי האינסולין הקיימים היום, האינסולינים קצרי הטווח Humalog (Lispro) ו-Aspart נחקרו בהיריון ונמצאו בטוחים לשימוש, עם מעבר שלייתי מינימלי וללא השפעות טרטוגניות. כמו כן, תוצאות ההיריון תחת שימוש בהם זהות לתוצאות הריוניות בנשים המשתמשות באינסולין רגיל (Regular)[29]. אינסולינים ארוכי טווח כגון Lantus (Glargine) ו-Levemir (Detemir) נחקרו פחות בהיריון, אולם בשנת 2012 מחקר רב לאומי מצא ש-Levemir בטוח ויעיל לשימוש בנשים עם סוכרת סוג 1 בהיריון[30],[31], ולכן מנהל המזון והתרופות האמריקאי (FDA, Food and Drug Administration) סיווג מחדש את Levemir כ-Class B בהיריון. מחקרים In vitro ב-Lantus הוכיחו שהוא אינו חוצה שליה, אולם עדיין קיימים חששות לגבי המעבר השלייתי In vivo[32], והוא עדיין שייך לקטגוריה C בנוגע לשימוש בו בהיריון. ביחידות היריון בסיכון ברחבי הארץ השימוש ב-Levemir, בעקבות ממצאים אלה, הפך לנפוץ.
טיפול פומי - בעוד שפרדיגמת הטיפול באינסולין בסוכרת הריונית היתה מקובעת זמן רב, סקירה של מחקרים מבוססי ראיות הוכיחה שרמת הגלוקוז האימהית אינה שונה באופן משמעותי תחת טיפול באינסולין או בטיפול היפוגליקמי פומי וכן שאין עדויות ברורות שהטיפול ב-Gluben (Glibenclamide) או ב-Metformin כרוך בעלייה בשיעור תוצאות הריוניות (אימהיות או עובריות) תת מיטביות[29],[33],[34]. עם זאת, חוסר העקביות במדידת התוצאות ההריוניות בין המחקרים השונים והיעדר מידע לגבי תוצאות ארוכות טווח מקשים על הסקת מסקנות ברורות.
למרות זאת, השימוש ב-Gluben הפך לנפוץ בשימוש בסוכרת הריונית בשנים האחרונות. מחקרים שונים הראו ששימוש ב-Gluben במהלך ההיריון אינו כרוך בסיכון גבוה יותר להיפוגליקמיה עוברית או למומים מולדים וכן שהוא טיפול יעיל בסוכרת הריונית[34],[35],[36],[37],[38],[39],[40].
גם הטיפול הפומי נדרש להתאמת מינון בהתאם לרמת הגלוקוז בדם ויש לאזנו בהתאם לארוחות למניעת היפוגליקמיה. לרוב המינון ההתחלתי של ה-Gluben עומד על 1.25-2.5 מ"ג בשעות הבוקר וניתן להעלות את המינון עד 20 מ"ג המתפרשים על פני שתי מנות יומיות.
השימוש בשאר התרופות ההיפוגליקמיות הפומיות בהיריון (Metformin, Acarbose ועוד) אינו נפוץ. לדוגמה, Metformin הוכחה כיעילה בטיפול בסוכרת הריונית במהלך הטרימסטרים השני והשלישי, אולם בין שליש לחצי מהנשים הנוטלות את התרופה ייאלצו להשתמש גם באינסולין להשגת איזון גליקמי[41]. בנוסף, Gluben הוכחה כיעילה יותר מ-Metformin בהשגת האיזון הגליקמי (16% מהמשתמשות ב-Gluben נאלצו להוסיף אינסולין לטיפול לעומת 35% מהנוטלות Metformin)[42].
קביעת משטר הטיפול
עם ביסוס האבחנה, יש להתחיל טיפול תזונתי או תרופתי, כאשר הרציונל הבסיסי הוא התחלת טיפול תזונתי ובמידת הצורך, התחלת טיפול תרופתי.
עם התחלת הטיפול התזונתי ההרה מתבקשת לנהל יומן רישום מסודר עם רמות הגלוקוז בארבע עד שבע מדידות יומיות. במקרה שיעדי המטרה נשמרים במשך 7 ימים עד 14 יום והמטופלת מפגינה היענות טובה למשטר התזונתי, אפשר להפחית את מספר המדידות היומיות. מדד אובייקטיבי טוב להיענות הוא משקלה של ההרה, כאשר לאחר האבחנה, אם היא שומרת על משקלה, הרי שהיא מקפידה על המשטר התזונתי.
אין מידע מבוסס לגבי פרק הזמן שבמהלכו יש לנסות את הטיפול התזונתי בטרם מתקבלת ההחלטה על התחלת טיפול תרופתי. באחד המחקרים נמצא כי 70% מהמטופלות עם רמת גלוקוז בצום נמוכה מ-95 מ"ג/ד"ל השיגו את יעדי המטרה תחת טיפול תזונתי במהלך השבועיים הראשונים לטיפול[43]. מחד, התחלת טיפול תרופתי טרם המועד עלולה לגרום לטיפול תרופתי מיותר, ומאידך, תוצאותיו של טיפול תת מיטבי הן ברורות. לכן, במטופלת עם רמת סוכר בצום נמוכה מ-95 מ"ג/ד"ל אשר אובחנה בשבוע 26 ניתן להתחיל טיפול תזונתי ולבחון האם היא מצליחה להגיע ליעדי המטרה, אולם במטופלת שאובחנה באיחור (שבוע 33-34) או מטופלת שרמת הסוכר בצום גבוהה מ-100-105 מ"ג/ד"ל יש מקום להתחלת טיפול תרופתי כקו טיפולי ראשון.
ביבליוגרפיה
- Alwan N, Tuffnell DJ, West J. Treatments for gestational diabetes. Cochrane Database Syst Rev 2009; :CD003395.
- Langer O, Conway DL, Berkus MD, et al. A comparison of glyburide and insulin in women with gestational diabetes mellitus. N Engl J Med 2000; 343:1134.
- ↑ National Diabetes Information Clearinghouse (Internet). Maryland: National Institutes of Health 2011. Available at: http://diabetes.niddk.nih.gov/dm/pubs/statistics/#Gestational. Accessed January 20, 2013
- ↑ 2.0 2.1 Wier LM, Witt E, Burgess J, Elixhauser A. Healthcare cost and utilization project. Statistical brief #102. Hospitalizations related to diabetes in pregnancy, 2008. Rockville (MD): Agency for Health Care Policy and Research; 2010. 5. O’Sullivan JB. Body weight and subsequent diabetes mellitus
- ↑ Anna V, van der Ploeg HP, Cheung NW, et al. Sociodemographic correlates of the increasing trend in prevalence of gestational diabetes mellitus in a large population of women between 1995 and 2005. Diabetes Care 2008; 31:2288.
- ↑ Engelgau MM, Herman WH, Smith PJ,German RR, Aubert RE. The epidemiology of diabetes and pregnancy in the US, 1988. Diabetes Care 18:1029–1033, 1995
- ↑ Langer O, Management of Gestational Diabetes: Pharmacologic Treatment Options and Glycemic Control. Endocrinol Metab Clin N Am 35 (2006) 53–78
- ↑ Proceedings of the 4th International Workshop-Conference on Gestational Diabetes Mellitus. Chicago, Illinois, USA. 14-16 March 1997. Diabetes Care 1998; 21 Suppl 2:B1.
- ↑ Committee opinion no. 504: screening and diagnosis of gestational diabetes mellitus. Obstet Gynecol 2011; 118:751.
- ↑ 8.0 8.1 8.2 ACOG Practice Bulletin Number 30, September 2001, Gestational diabetes. Obstet Gynecol 2001; 98:525.
- ↑ Hartling L, Dryden DM, Guthrie A, Muise M, Vandermeer B, Aktary WM, Pasichnyk D, Seida JC, Donovan L. Screening and Diagnosing Gestational Diabetes Mellitus. Evidence Report/Technology Assessment No. 210. (Prepared by the University of Alberta Evidence-based Practice Center under Contract No. 290-2007-10021-I.) AHRQ Publication No. 12(13)-E021-EF. Rockville, MD: Agency for Healthcare Research and Quality. October 2012. eww.effectivehealthcare.ahrq.gov/reports/final.cfm. (Accessed on January 27, 2013).
- ↑ 10.0 10.1 International Association of Diabetes and Pregnancy Study Groups Consensus Panel, Metzger BE, Gabbe SG, et al. International association of diabetes and pregnancy study groups recommendations on the diagnosis and classification of hyperglycemia in pregnancy. Diabetes Care 2010; 33:676.
- ↑ American Diabetes Association. Diagnosis and classification of diabetes mellitus. Diabetes Care 2011; 34 Suppl 1:S62.
- ↑ American Diabetes Association. Diagnosis and classification of diabetes mellitus. Diabetes Care 2012; 35 Suppl 1:S64.
- ↑ 13.0 13.1 HAPO Study Cooperative Research Group, Metzger BE, Lowe LP, et al. Hyperglycemia and adverse pregnancy outcomes. N Engl J Med 2008; 358:1991.
- ↑ Langer O, Yogev Y, Most O, Xenakis EM. Gestational diabetes: the consequences of not treating. Am J Obstet Gynecol 2005; 192:989.
- ↑ 15.0 15.1 Crowther CA, Hiller JE, Moss JR, et al. Effect of treatment of gestational diabetes mellitus on pregnancy outcomes. N Engl J Med 2005; 352:2477.
- ↑ 16.0 16.1 Landon MB, Spong CY, Thom E, et al. A multicenter, randomized trial of treatment for mild gestational diabetes. N Engl J Med 2009; 361:1339.
- ↑ Franz MJ, Bantle JP, Beebe CA, et al. Evidence-based nutrition principles and recommendations for the treatment and prevention of diabetes and related complications. Diabetes Care 2003; 26 Suppl 1:S51.
- ↑ The Art and Science of Diabetes Self-Management Education, Mensing, C (Eds), American Association of Diabetes Educators, 2006. p.241.
- ↑ Cheng YW, Chung JH, Kurbisch-Block I, et al. Gestational weight gain and gestational diabetes mellitus: perinatal outcomes. Obstet Gynecol 2008; 112:1015.
- ↑ Han S, Crowther CA, Middleton P. Interventions for pregnant women with hyperglycaemia not meeting gestational diabetes and type 2 diabetes diagnostic criteria. Cochrane Database Syst Rev 2012;
- ↑ 21.0 21.1 American Diabetes Association. Gestational diabetes mellitus. Diabetes Care 2004; 27 Suppl 1:S88.
- ↑ Hawkins JS, Casey BM, Lo JY, et al. Weekly compared with daily blood glucose monitoring in women with diet-treated gestational diabetes. Obstet Gynecol 2009; 113:1307.
- ↑ American Diabetes Association. Standards of medical care in diabetes--2013. Diabetes Care 2013; 36 Suppl 1:S11.
- ↑ Langer O, Levy J, Brustman L, et al. Glycemic control in gestational diabetes mellitus--how tight is tight enough: small for gestational age versus large for gestational age? Am J Obstet Gynecol 1989; 161:646.
- ↑ Ceysens G, Rouiller D, Boulvain M. Exercise for diabetic pregnant women. The Cochrane Database of Systematic Reviews 2006, Issue 3. Art. No.: CD004225. DOI: 10.1002/14651858.CD004225.pub2.
- ↑ Thompson DJ, Porter KB, Gunnells DJ, et al. Prophylactic insulin in the management of gestational diabetes. Obstet Gynecol 1990; 75:960.
- ↑ Lewis SB, Wallin JD, Kuzuya H, et al. Circadian variation of serum glucose, C-peptide immunoreactivity and free insulin normal and insulin-treated diabetic pregnant subjects. Diabetologia 1976; 12:343.
- ↑ Nachum Z, Ben-Shlomo I, Weiner E, Shalev E. Twice daily versus four times daily insulin dose regimens for diabetes in pregnancy: randomised controlled trial. BMJ 1999; 319:1223.
- ↑ 29.0 29.1 Nicholson WK, Wilson LM, Witkop CT, et al. Therapeutic management, delivery, and postpartum risk assessment and screening in gestational diabetes. Evid Rep Technol Assess (Full Rep) 2008;1.
- ↑ Mathiesen ER, Hod M, Ivanisevic M, et al. Maternal efficacy and safety outcomes in a randomized controlled trial comparing insulin determir with NPH insulin in 310 pregnant women with type 1 diabetes mellitus. Diabetes Care 2012; :in press.
- ↑ Hod M, McCance DR, Ivanisevic M, et al. Perinatal Outcomes in a Randomized Trial Comparing Insulin Detemir with NPH Insulin in 310 Pregnant Women with Type 1. Abstract 62-LB. American Diabetes Association. 71st Scientific Sessions. June 24 - 28, 2011 San Diego Convention Center - San Diego, California
- ↑ Pollex EK, Feig DS, Lubetsky A, et al. Insulin glargine safety in pregnancy: a transplacental transfer study. Diabetes Care 2010; 33:29.
- ↑ Nicholson W, Bolen S, Witkop CT, et al. Benefits and risks of oral diabetes agents compared with insulin in women with gestational diabetes: a systematic review. Obstet Gynecol 2009; 113:193.
- ↑ 34.0 34.1 Dhulkotia JS, Ola B, Fraser R, Farrell T. Oral hypoglycemic agents vs insulin in management of gestational diabetes: a systematic review and metaanalysis. Am J Obstet Gynecol 2010; 203:457.e1.
- ↑ Kremer CJ, Duff P. Glyburide for the treatment of gestational diabetes. Am J Obstet Gynecol 2004; 190:1438.
- ↑ Langer O, Yogev Y, Xenakis EM, Rosenn B. Insulin and glyburide therapy: dosage, severity level of gestational diabetes, and pregnancy outcome. Am J Obstet Gynecol 2005; 192:134.
- ↑ Yogev Y, Ben-Haroush A, Chen R, et al. Undiagnosed asymptomatic hypoglycemia: diet, insulin, and glyburide for gestational diabetic pregnancy. Obstet Gynecol 2004; 104:88.
- ↑ Jacobson GF, Ramos GA, Ching JY, et al. Comparison of glyburide and insulin for the management of gestational diabetes in a large managed care organization. Am J Obstet Gynecol 2005; 193:118.
- ↑ Conway DL, Gonzales O, Skiver D. Use of glyburide for the treatment of gestational diabetes: the San Antonio experience. J Matern Fetal Neonatal Med 2004; 15:51.
- ↑ Rochon M, Rand L, Roth L, Gaddipati S. Glyburide for the management of gestational diabetes: risk factors predictive of failure and associated pregnancy outcomes. Am J Obstet Gynecol 2006; 195:1090.
- ↑ Rowan JA, Hague WM, Gao W, et al. Metformin versus insulin for the treatment of gestational diabetes. N Engl J Med 2008; 358:2003.
- ↑ Moore LE, Clokey D, Rappaport VJ, Curet LB. Metformin compared with glyburide in gestational diabetes: a randomized controlled trial. Obstet Gynecol 2010; 115:55.
- ↑ McFarland MB, Langer O, Conway DL, Berkus M. Dietary therapy for gestational diabetes: how long is long enough? Obstet Gynecol 1999;93:978–82.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי פרופ' משה הוד - הפקולטה לרפואה ע"ש סאקלר, אוניברסיטת תל אביב, רמת אביב וד"ר אמיר אבירם - היחידה לרפואת האם והעובר, בית החולים לנשים ע"ש הלן שניידר, המרכז הרפואי רבין, פתח תקוה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק