הבדלים בין גרסאות בדף "סרטן הריאה - טיפול - Lung cancer - treatment"
| שורה 60: | שורה 60: | ||
*כטיפול בקווים מתקדמים. | *כטיפול בקווים מתקדמים. | ||
| − | ====Tarceva כטיפול קו ראשון לחולים עם תשנית ב- EGFR==== | + | ====[[Tarceva]] כטיפול קו ראשון לחולים עם תשנית ב- EGFR==== |
בקרב כ- 15% מחולי סרטן ריאה קיימת תשנית בקולטן EGFR הגורמת לפעילות יתר שלו בתאי הגידול. עבור קבוצת חולים זו נמצא כי עיכוב פעילות הקולטן המוטנטי על ידי טיפול ב- TKI הוא יעיל במיוחד. | בקרב כ- 15% מחולי סרטן ריאה קיימת תשנית בקולטן EGFR הגורמת לפעילות יתר שלו בתאי הגידול. עבור קבוצת חולים זו נמצא כי עיכוב פעילות הקולטן המוטנטי על ידי טיפול ב- TKI הוא יעיל במיוחד. | ||
| שורה 72: | שורה 72: | ||
#שיפור שיעור תגובה (Response rate){{כ}} (54.5% לעומת 10.5%). | #שיפור שיעור תגובה (Response rate){{כ}} (54.5% לעומת 10.5%). | ||
| − | ====Tarceva כטיפול אחזקה בסיום טיפול כימותרפי ראשוני {{הערה|שם=הערה5|Cappuzzo et al. Lancet oncol 2010;11:521-29.}}==== | + | ====[[Tarceva]] כטיפול אחזקה בסיום טיפול כימותרפי ראשוני {{הערה|שם=הערה5|Cappuzzo et al. Lancet oncol 2010;11:521-29.}}==== |
מחקר SATURN, מחקר שלב III רב-מרכזי ובעל הקצאה אקראית, השווה את יעילות Tarceva לעומת אינבו (Placebo) כטיפול אחזקה ב- 889 חולי NSCLC גרורתי אשר מחלתם לא התקדמה לאחר טיפול כימותרפי מבוסס-פלטינום בקו ראשון. הטיפול עם Tarceva הדגים שיפור משמעותי בזמן החציוני עד התקדמות המחלה (PFS) ובהישרדות הכוללת (Overall survival) של החולים בהשוואה לקבוצת הביקורת. במחקר נצפתה הארכה של מעל חודשיים בהישרדות החציונית הכוללת בקרב כלל המטופלים שמחלתם הייתה יציבה (Stable disease) בתום הטיפול הראשוני בכימותרפיה: 11.9 חודשים בקבוצה שטופלה ב- Tarceva לעומת 9.6 חודשים בקבוצת הביקורת (יחס סיכונים=0.72, {{כ}}0.002=p{{כ}}). בתת-קבוצת החולים ללא תשנית בגן ל- EGFR, נצפתה הארכת חיים של מעל 3 חודשים. | מחקר SATURN, מחקר שלב III רב-מרכזי ובעל הקצאה אקראית, השווה את יעילות Tarceva לעומת אינבו (Placebo) כטיפול אחזקה ב- 889 חולי NSCLC גרורתי אשר מחלתם לא התקדמה לאחר טיפול כימותרפי מבוסס-פלטינום בקו ראשון. הטיפול עם Tarceva הדגים שיפור משמעותי בזמן החציוני עד התקדמות המחלה (PFS) ובהישרדות הכוללת (Overall survival) של החולים בהשוואה לקבוצת הביקורת. במחקר נצפתה הארכה של מעל חודשיים בהישרדות החציונית הכוללת בקרב כלל המטופלים שמחלתם הייתה יציבה (Stable disease) בתום הטיפול הראשוני בכימותרפיה: 11.9 חודשים בקבוצה שטופלה ב- Tarceva לעומת 9.6 חודשים בקבוצת הביקורת (יחס סיכונים=0.72, {{כ}}0.002=p{{כ}}). בתת-קבוצת החולים ללא תשנית בגן ל- EGFR, נצפתה הארכת חיים של מעל 3 חודשים. | ||
| − | ====Tarceva לטיפול בסרטן ריאות גרורתי בקו שני (לאחר התקדמות מחלה) {{הערה|שם=הערה6|Shepherd F, et al. N Engl J Med 2005;353:123-32.}}==== | + | ====[[Tarceva]] לטיפול בסרטן ריאות גרורתי בקו שני (לאחר התקדמות מחלה) {{הערה|שם=הערה6|Shepherd F, et al. N Engl J Med 2005;353:123-32.}}==== |
מחקר ה- BR.21, מחקר שלב III שכלל 731 חולים שמחלתם התקדמה לאחר טיפול בכימותרפיה בקו ראשון, השווה את יעילות Tarceva לעומת אינבו כטיפול בקו שני או שלישי. במחקר הודגם שמתן Tarceva האריך את ההישרדות החציונית הכוללת של החולים ב- 43% (6.7 לעומת 4.7 חודשים) והדגים שיפור משמעותי בכל המדדים הקליניים הנוספים: שיעור התגובה לטיפול, הזמן עד התקדמות המחלה ותסמיני המחלה. התועלת בטיפול ב- Tarceva בקו שני הודגמה הן בחולים עם תשנית בגן ל- EGFR והן בחולים ללא תשנית. | מחקר ה- BR.21, מחקר שלב III שכלל 731 חולים שמחלתם התקדמה לאחר טיפול בכימותרפיה בקו ראשון, השווה את יעילות Tarceva לעומת אינבו כטיפול בקו שני או שלישי. במחקר הודגם שמתן Tarceva האריך את ההישרדות החציונית הכוללת של החולים ב- 43% (6.7 לעומת 4.7 חודשים) והדגים שיפור משמעותי בכל המדדים הקליניים הנוספים: שיעור התגובה לטיפול, הזמן עד התקדמות המחלה ותסמיני המחלה. התועלת בטיפול ב- Tarceva בקו שני הודגמה הן בחולים עם תשנית בגן ל- EGFR והן בחולים ללא תשנית. | ||
גרסה מ־09:51, 26 בספטמבר 2014
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| סרטן הריאה - טיפול | ||
|---|---|---|
| Lung cancer - treatment | ||
| יוצר הערך | ||
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן ריאה
אפידמיולוגיה וגורמי סיכון
שיעור התחלואה בסרטן הריאה מצוי בעלייה מתמדת, וממאירות זו מהווה כיום את גורם התמותה המוביל מסרטן בקרב גברים ונשים כאחד. בישראל מאובחנים מידי שנה כ- 2000 חולי סרטן ריאה חדשים.
גורם הסיכון העיקרי לסרטן ריאה הוא עישון, אשר מעלה את הסיכון לכל סוגי סרטן הריאה. כ- 85% מהחולים הינם מעשנים או שעישנו בעברם. גורמי סיכון נוספים כוללים עישון סביל (Passive) וחשיפה לאסבסט (Asbestos), גז רדון (Radon) וזיהום אוויר.
התסמינים השכיחים של סרטן ריאה כוללים שיעול, קוצר נשימה, כיח דמי, כאבים בחזה ודלקות ריאה נשנות. האבחנה מבוצעת בדרך כלל על ידי נטילת ביופסיה באמצעות בדיקת שקיפת סימפונות (Bronchoscopy) או דיקור מונחה תהודה מגנטית (Computed tomography guided lung biopsy), אשר באמצעותם ניתן לקבוע גם את סוג הגידול המסוים [1].
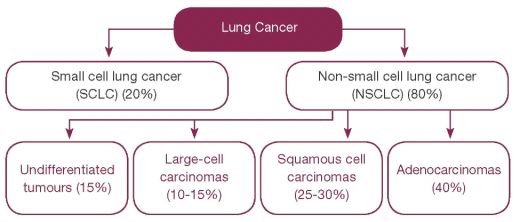
סוגי סרטן הריאה
ניתן לסווג את הגידולים הממאירים בריאה על סמך מאפיינים היסטולוגיים:
בנוסף לקביעת הסוג ההיסטולוגי של הגידול, נערכת כיום בדיקה לתאי הגידול לנוכחות תשנית (Mutation) בקולטן לגורם גדילה אפידרמלי (EGFR ,Epidermal Growth Factor Receptor), אשר קיימת בכ- 15% מחולי סרטן ריאה של תאים שאינם קטנים (NSCLC ,Non-Small-Cell Lung Carcinoma). נוכחות תשנית זו חשובה לצורך בחירת הטיפול המערכתי המתאים ביותר לחולים בשלב מחלה מתקדם.
התשנית מביאה לפעילות יתר של הקולטן אליו נקשר גורם הגדילה, ובעקבות כך מופעלת שרשרת של תהליכים אשר מעודדים את גדילת והתרבות התאים הממאירים והתפתחות גרורות.
קבוצת החולים בעלי השתנית ב- EGFR מפיקה תועלת קלינית ייחודית מטיפול התחלתי עם תרופות מקבוצת מעכבי טירוזין קינאז (TKIs ,Tyrosine-Kinase Inhibitors), המהווים כיום את טיפול הבחירה בקו ראשון בחולים אלו.
שלבי המחלה
דירוג התפשטות המחלה (Staging) נקבע על סך שלושה מאפיינים [2]:
- T: מידת החדירה של הגידול הראשוני.
- N: מיקום בלוטות הלימפה המעורבות.
- M: הימצאות גרורות מרוחקות.
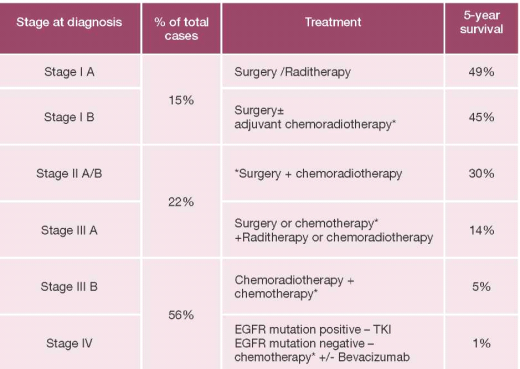
עקרונות הטיפול ופרוגנוזה
הן הטיפול בסרטן הריאה והן הפרוגנוזה של החולים משתנים בהתאם לשלב המחלה [1][2]:
הטיפול הכימותרפי המקובל עבור NSCLC הוא משלבים מבוססי-פלטינום (Platinum-based antineoplastic) הכוללים Abiplatin (Cisplatin) או Carboplatin הניתנים עם אחת מבין התרופות הבאות: Blastovin (Vinblastine), Navelbine (Vinorelbine), Alimta (Pemetrexed), Etoposide, Paclitaxel, Gemcitabine או Docetaxel.
בטיפול בקו ראשון בחולים עם מחלה מתקדמת, ניתן להוסיף למשלב גם Avastin (Bevacizumab).
לאחר התקדמות המחלה ניתן בדרך כלל טיפול עם תרופה כימותרפית בודדת או TKI.
טיפולים ממוקדים
Tarceva (Erlotinib)
Tarceva הינה תרופה נוגדת גידול (Antineoplastic agent) מקבוצת ה- TKIs. זוהי מולקולה קטנה (Small molecule) החוסמת באופן ממוקד את פעילות האנזים טירוזין קינאז שבקולטן EGFR, ובכך מונעת העברת מסרים ביולוגיים בתוך התא הסרטני ומעכבת את גדילת הגידול והתפשטותו.
הטיפול ב- Tarceva הוכח כמאריך חיים ומעכב את התקדמות המחלה במספר מחקרים קליניים גדולים עבור התוויות שונות:
- כטיפול קו ראשון לחולים עם תשנית ב- EGFR.
- כטיפול אחזקה (Maintenance) לחולים שמחלתם לא התקדמה לאחר טיפול כימותרפי מבוסס-פלטינום בקו ראשון.
- כטיפול בקווים מתקדמים.
Tarceva כטיפול קו ראשון לחולים עם תשנית ב- EGFR
בקרב כ- 15% מחולי סרטן ריאה קיימת תשנית בקולטן EGFR הגורמת לפעילות יתר שלו בתאי הגידול. עבור קבוצת חולים זו נמצא כי עיכוב פעילות הקולטן המוטנטי על ידי טיפול ב- TKI הוא יעיל במיוחד.
לאור זאת, קיימת חשיבות רבה לאבחון תשנית בגן ל- EGFR לכל חולה עם גידול מסוג NSCLC לפני תחילת הטיפול במחלה גרורתית. במידה והחולה נמצא חיובי לתשנית, הטיפול ב- TKI הוא הטיפול המועדף.
יעילות Tarceva כקו ראשון לחולים עם תשנית בגן ל- EGFR נבחנה והוכחה בשני מחקרי שלב III- הן באוכלוסייה אסייתית והן באוכלוסייה מערבית:
- מחקר OPTIMAL [3]: מחקר שלב III פרוספקטיבי ובעל הקצאה אקראית, השווה את יעילות טיפול ב- Tarceva לעומת טיפול כימותרפי בחולים עם מוטציה בגן ל- EGFR ממוצא אסיאתי. הטיפול ב- Tarceva האריך את הזמן החציוני ללא התקדמות מחלה (PFS ,Progression-Free Survival) ל- 13.1 חודשים לעומת 4.6 חודשים בלבד בחולים שטופלו בכימותרפיה (יחס סיכונים=0.16), תוצאה חסרת תקדים בקבוצת חולים זו.
- בנוסף, בקרב החולים שטופלו ב- Tarceva, נצפה שיפור משמעותי בכל מדדי איכות החיים, בהשוואה לחולים שטופלו בכימותרפיה.
- מחקר EURTAC [4]: מחקר שלב III פרוספקטיבי ובעל הקצאה אקראית, השווה לראשונה את יעילות הטיפול ב- Tarceva לעומת כימותרפיה בחולים עם תשנית בגן ל- EGFR ממוצא מערבי. בקבוצה שטופלה ב- Tarceva נצפה שיפור מובהק בכל המדדים הקליניים, בהשוואה לקבוצה שטופלה בכימותרפיה:
- הכפלת משך הזמן החציוני עד התקדמות המחלה (PFS חציוני) — 9.7 חודשים לעומת 5.2 חודשים, תוך הפחתת הסיכון להתקדמות המחלה בכ- 63% (יחס סיכונים=0.37, 0.0001>p).
- שיפור שיעור תגובה (Response rate) (54.5% לעומת 10.5%).
Tarceva כטיפול אחזקה בסיום טיפול כימותרפי ראשוני [5]
מחקר SATURN, מחקר שלב III רב-מרכזי ובעל הקצאה אקראית, השווה את יעילות Tarceva לעומת אינבו (Placebo) כטיפול אחזקה ב- 889 חולי NSCLC גרורתי אשר מחלתם לא התקדמה לאחר טיפול כימותרפי מבוסס-פלטינום בקו ראשון. הטיפול עם Tarceva הדגים שיפור משמעותי בזמן החציוני עד התקדמות המחלה (PFS) ובהישרדות הכוללת (Overall survival) של החולים בהשוואה לקבוצת הביקורת. במחקר נצפתה הארכה של מעל חודשיים בהישרדות החציונית הכוללת בקרב כלל המטופלים שמחלתם הייתה יציבה (Stable disease) בתום הטיפול הראשוני בכימותרפיה: 11.9 חודשים בקבוצה שטופלה ב- Tarceva לעומת 9.6 חודשים בקבוצת הביקורת (יחס סיכונים=0.72, 0.002=p). בתת-קבוצת החולים ללא תשנית בגן ל- EGFR, נצפתה הארכת חיים של מעל 3 חודשים.
Tarceva לטיפול בסרטן ריאות גרורתי בקו שני (לאחר התקדמות מחלה) [6]
מחקר ה- BR.21, מחקר שלב III שכלל 731 חולים שמחלתם התקדמה לאחר טיפול בכימותרפיה בקו ראשון, השווה את יעילות Tarceva לעומת אינבו כטיפול בקו שני או שלישי. במחקר הודגם שמתן Tarceva האריך את ההישרדות החציונית הכוללת של החולים ב- 43% (6.7 לעומת 4.7 חודשים) והדגים שיפור משמעותי בכל המדדים הקליניים הנוספים: שיעור התגובה לטיפול, הזמן עד התקדמות המחלה ותסמיני המחלה. התועלת בטיפול ב- Tarceva בקו שני הודגמה הן בחולים עם תשנית בגן ל- EGFR והן בחולים ללא תשנית.
אווסטין (Avastin (Bevacizumab
מנגנון פעולה
אנגיוגנזה (היווצרות כלי דם חדשים) הוא תהליך המאפשר לגידולים ממאירים לקבל אספקת חמצן וחומרי מזון, ולפיכך חיוני לצמיחתם ולשליחת גרורות לאיברים מרוחקים. תהליך זה משופעל ע"י הגידול באמצעות הפרשת החלבון Vascular Endothelial Growth Factor) VEGF). כלי הדם החדשים שנוצרים נבדלים במבנם ובתכונותיהם מכלי דם בשלים, והישרדותם תלויה בהמשך נוכחות VEGF. רמות מוגברות של VEGF הודגמו בממאירויות שונות כדוגמת מעי, שד, ריאה ומוח, ונמצא מתאם הפוך בין רמתן לפרוגנוזה. אווסטין הוא התכשיר הראשון שנכנס לשימוש קליני הפועל במנגנון של עיכוב אנגיוגנזה. אווסטין הוא נוגדן מונוקלונלי הנקשר ספציפית ל-VEGF ומונע ממנו להיקשר לקולטנים על פני תאי האנדותל ולשפעלם, וכך מעכב את תהליך האנגיוגנזה. בנוסף, אווסטין משפר את הגעת הכמותרפיה לגידול עךי הפחתת החדירות הגבוהה המאפיינת את דופן כלי-הדם שנוצרו בתהליך האנגיוגנזה. הפגיעה באספקת הדם לגידול ושיפור הגעת הכמותרפיה אליו גורמים לנסיגתו ולהגבלת התפשטותו בגוף בתהליך האנגיוגנזה. הפגיעה באספקת הדם לגידול ושיפור הגעת הכמותרפיה אליו גורמים לנסיגתו ולהגבלת התפשטותו בגוף.
יעילות
הטיפול באווסטין הוכח כמאריך חיים בחולי סרטן ריאה גרורתי מסוג non-squamous NSCLC בקו טיפול ראשון.
במחקר פרוספקטים, רנדומלי פאזה Ill[7] נבדקה יעילות אווסטין בשילוב עם משלב כמותרפי מקובל של קרבופלטין וטקסול לטיפול כמותרפי בלבד בקרב 878 חולי סרטן ריאה גרורתי. המחקר הראה כי הוספת אווסטין לכמותרפיה הביאה להארכה מובהקת בהישרדות הכוללת החציונית של החולים בהשוואה לכמותרפיה לבד (12.3 לעומת 0.3ו חודשים) ולשיפור בזמן עד התקדמות המחלה ובשיעור התגובה לטיפול. בקבוצת החולים עם גידול מסוג אדנוקרצינומה, שהנו הסוג הנפוץ ביותר, נמצא כי אווסטין הביאה להארכה של 4 חודשים בהישרדות הכוללת החציונית של החולים (4.2ו לעומת 0.3ו חודשים).
מחקר פרוספקטים, רנדומלי, פאזה Ill נוסף, AVAiL[8], בחן את היעילות של אווסטין בשילוב עם ציספלטין וגימציטבין לעומת המשלב הכמותרפי לבד בקרב למעלה מ-000ו חולי סרטן ריאה גרורתי. המחקר תוכנן להוכיח הארכת משך הזמן עד התקדמות המחלה והראה כי מתן אווסטין הפחית את הסיכון להתקדמות המחלה בכ-30%. ההישרדות החציונית של החולים במחקר הגיעה למעל 3ו חודשים. מחקר AVAPERL[9] מחקר פאזה III פרוספקטים רנדומלי, אשר פורסם לאחרונה, הראה ששילוב אווסטין עם אלימטה כקו טיפול ראשון ועד להתקדמות המחלה הדגים יעילות מרשימה, עם נתוני PFS של 0.2ו חודשים ללא התקדמות המחלה. נתוני OS טרם פורסמו, אך מסתמן כי השילוב של אווסטין עם אלימטה הינו פוטנטי ביותר. בשני מחקרי פאזה IV[10] , [11] הודגם כי בחולים שהמשיכו טיפול באווסטין עד התקדמות המחלה, נצפתה הישרדות חציונית של מעל 8ו חודשים, הארכת חיים משמעותית ביותר עבור חולים אלו.
בטיחות אווסטין בחולי NSCLC
בשני מחקרי פאזה IV[10], [11] בהם טופלו באווסטין למעלה מ-4000 חולי סרטן ריאה גרורתי מסוג - non-squamous NSCLC, בהם גם חולים מבוגרים, חולים עם גרורות מוחיות וחולים המטופלים באנטי-קואגולנטים, הודגם כי הטיפול באווסטין נסבל היטב.
ביבליוגרפיה
- Tarceva Israeli MoH approved prescribing information.
- Avastin Israeli MoH approved prescribing information.
- ↑ 1.0 1.1 http://www.seer.cancer.gov/statfacts/html/lungb.html.
- ↑ 2.0 2.1 NCCN guidelines version I 2011 Tarceva.
- ↑ R. Rosell et al. NEJM 2009;361:958-67.
- ↑ R.Rosell et al. ASCO 2011.
- ↑ Cappuzzo et al. Lancet oncol 2010;11:521-29.
- ↑ Shepherd F, et al. N Engl J Med 2005;353:123-32.
- ↑ Sandler, et al. NEJM 2006.
- ↑ Reck, et al. Annals of oncol. 2009.
- ↑ F. Barlesi et al. ECCO-ESMO 2011; Abstract LBA34.
- ↑ 10.0 10.1 Crino, et al. Lancet Oncol 2010.
- ↑ 11.0 11.1 Wozniak, et al. J Clin Oncol 2010; 28:15s.


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק