סרטן השד - טיפול טרום ניתוחי - Breast cancer - neoadjuvant therapy
| סרטן השד - טיפול טרום ניתוחי | ||
|---|---|---|
| Breast cancer - neoadjuvant therapy | ||

| ||
| שמות נוספים | טיפול כימותרפי טרום ניתוחי בסרטן השד | |
| יוצר הערך | ד"ר רוית אגסי ופרופ' דויד גפן | |
לערכים נוספים הקשורים לנושא זה, ראו את דפי הפירושים: – סרטן השד, הכנה לניתוח
בשנת 1983 דווח לראשונה על אפשרות טיפול חדשה בסרטן השד - מתן טיפול כימי טרום ניתוחי (Neoadjuvant). אפשרות טיפול זו נבדקה על ידי Hortobagyi וחבריו ממרכז הסרטן אנדרסון (MD Anderson cancer center) שבטקסס ארצות הברית, כאשר במהלך עבודתם בדקו החוקרים 52 מקרים של סרטן שד מתקדם, במטרה להפוך גידול בלתי נתיח למחלה נתיחה הניתנת לריפוי[1].
בשל התוצאות המעודדות בחולות אלה, שימש בהמשך הטיפול הכימי הטרום ניתוחי גם כטיפול בסרטן שד נתיח (במטרה לצמצם את ממדי הניתוח - מניתוח גדול הכולל כריתה מלאה לניתוח קטן יותר הכולל כריתה חלקית בלבד).
בהמשך הפך הטיפול הכימי לאופציה טיפולית גם בקרב חולות עם סרטן שד מוקדם[2]. בשנת 2013 פורסם מחקר שכלל 2,072 חולות סרטן שד שקיבלו טיפול טרום ניתוחי. רוב החולות היו בשלב מוקדם, מתוכן 67.8% עם גידול בשלב T1-T2 ו-45% עם בלוטות שליליות באופן קליני בבית השחי. חציון משך המעקב היה 62 חודשים. שיעור ההישרדות וההישרדות ללא מחלה היו 86.8% ו-66.9%, בהתאמה[3].
יתרונות הטיפול הטרום ניתוחי
לטיפול הטרום ניתוחי מספר יתרונות בהשוואה לטיפול המשלים (Adjuvant):
צמצום הגידול - הטיפול מצמצם את הגידול ומעלה לפיכך את שיעור הניתוחים משמרי השד. המחקר ACOSOG Z1071 בדק אם ניתן להפחית את הצורך בדיסקציה אקסילרית. התוצאות היו מבטיחות אבל לא חד משמעיות[4].
הערכה וניטור של התגובה לטיפול - הערכה זו מאפשרת לשנות את הטיפול במידת הצורך, ומספקת מידע לגבי אפשרויות טיפול עתידיות[3].
ניבוי תוצאות לטווח ארוך - התגובה לטיפול מהווה סמן פרוגנוסטי להישרדות, ומנבאת תוצאות לטווח ארוך[5]. בנוסף, באופן תאורטי, ניתן לומר כי טיפול מוקדם יותר בגרורות מיקרוסקופיות יביא לתוצאות טובות יותר לטווח הארוך (עובדה זו טרם הוכחה מחקרית).
טיפול כימי
מאז שנות ה-80 של המאה הקודמת ידוע שטיפול משלים אצל נשים עם סרטן שד מוקדם או אזורי, מפחית את שיעור ההישנות, ויכול לשפר את ההישרדות ללא מחלה, וכן את ההישרדות הכוללת[6].
נעשו בעבר מספר ניסיונות השוואה בין טיפול כימי ראשוני לטיפול משלים. במחקר 18-B שערך ה-NSABP (National Surgical Adjuvant Breast Project) קיבלו החולות שהשתתפו בו באופן רנדומלי, 4 מחזורים של טיפול כימי במשלב AC הכולל Doxorubicin ו-Endoxan (Cyclophosphamide), לפני או אחרי ניתוח. מחקרים אלה לא הראו הבדלים בהישרדות הכללית או בהישרדות ללא מחלה בין שתי הקבוצות, אחרי 16 שנות מעקב.
במחקר אחר של ה-B-27 ,NSABP, היו 3 קבוצות של חולות. כולן קיבלו טיפול במשלב AC לפני הניתוח כאשר קבוצה אחת קיבלה בנוסף Docetaxel לפני הניתוח, וקבוצה שנייה קיבלה Docetaxel אחרי הניתוח. בתום 8 שנות מעקב, לא נמצאו הבדלים בין הקבוצות בהישרדות הכללית או בהישרדות ללא מחלה[7]. עבודות אלה ואחרות שפורסמו אמנם לא הוכיחו עליונות של שיטה זו על אחרת, אך הוכח לפחות שטיפול כימי טרום ניתוחי יעיל לא פחות מטיפול כימי אחרי ניתוח, ומאפשר להעלות את שיעור הניתוחים משמרי השד.
תוספת של תרופה מקבוצת הטקסנים (Taxane) נבדקה במסגרת מחקרים אחרים, כמו 27-B וכן במטא-אנליזה שפורסמה בשנת 2008[8]. עבודות אלה לא הוכיחו יתרון מבחינת הישרדות בכלל והישרדות ללא מחלה, אך נמצא שבקרב הנשים שנכללו בקבוצה שקיבלה תוספת מקבוצת טקסנים הושג שיעור גבוה יותר של תגובה פתולוגית מלאה (PCR, Pathologic Complete Response).
תגובה זו התבססה על עבודות שהוכיחו שטיפול משלים הניתן במנות צפופות (Dose Dense) של כימותרפיה כל שבועיים יעיל יותר לעומת טיפול בכל 3 שבועות. כמו כן, מעבודות שנערכו בנושא הטיפול הטרום ניתוחי, עולה שטיפול במנות צפופות יעיל יותר מטיפול הניתן בכל 3 שבועות, אם כי לפעמים הטיפול כרוך במחיר של רעילות יתר[9]. מסיבה זו טיפול כימי טרום ניתוחי (משלב AC) נפוץ (נכון לשנת 2015) והוא ניתן כל שבועיים ל-4 מחזורים, ולאחר מכן ניתן טיפול באמצעות Paclitaxel כל שבועיים, 4 פעמים, או במינון נמוך יותר, כל שבוע, למשך 12 שבועות.
טיפול בתרופה חדשה, Ixempra (Ixabepilone), מקבוצת ה-Taxanes נבדק בטיפול טרום ניתוחי מול Paclitaxel, אך שיעור התגובה לא עלה[10]. בשנת 2013 פרסם החוקר Von Minckwitz יחד עם חוקרים נוספים, עמדה לפיה יש להחליף כימותרפיה כעבור שני מחזורים של Taxane ומשלב AC, במקרים בהם לא התקבלה תגובה קלינית. במחקר כל החולות קיבלו התחלת טיפול טרום ניתוחי של שני מחזורים שכללו משלב TAC - Docetaxel, Doxorubicin ו-Endoxan. חולות אצלן צומצם הגידול הסרטני, קיבלו בצורה אקראית עוד 4 מחזורים או 6 מחזורים של TAC (הטיפול הסטנדרטי). חולות שלא הגיבו לטיפול, קיבלו עוד 4 מחזורים של TAC, או 4 מחזורים של טיפול אחר שכלל מתן Vinorelbine ו-Capecitabine (משלב NX). במקרים שחולות לא הגיבו לטיפול TAC והועברו לטיפול NX, הושגה הישרדות ללא מחלה לזמן רב יותר מאשר אצל אלו שהטיפול שלהן לא הוחלף. מחקר זה (הנמצא, נכון לשנת 2015, בפאזה 3) הוא המחקר הראשון שמצביע על היתרון בשינוי הטיפול הטרום ניתוחי על סמך התגובה הראשונית לטיפול[3].
טיפול כימי טרום ניתוחי הוא טיפול נפוץ, המאפשר בעיקר ביצוע ניתוחים שמרניים יותר. השאלה האם טיפול כזה יעיל בהפחתת הסיכון להישנות המחלה והעלאת שיעורי הריפוי, אינה מוכחת. קרוב לוודאי שמחקרים בתרופות ישנות כמו Abiplatin (Cisplatin) ו-Carboplatin ובתרופות חדשות יביאו לשיפור ביעילות הטיפול הטרום ניתוחי והתאמתו למטופלת באופן אישי.
טיפול ביולוגי
בחולות סרטן שד עם ביטוי יתר של HER2, התברר כי תוספת של הנוגדן החד שבטי (Monoclonal) Herceptin (Trastuzumab) מעלה באופן משמעותי את שיעור התגובה הפתולוגית המלאה. במחקר הראשון, שפורסם בשנת 2005, טופלו חולות סרטן שד עם ביטוי יתר של HER2 בכימותרפיה טרום ניתוחית. באופן אקראי נבחרו מחצית מהחולות וטופלו ב-Herceptin בנוסף לכימותרפיה כחלק מהטיפול הטרום ניתוחי. המחקר הופסק אחרי שרק 34 חולות סיימו את הטיפול (מתוך 164 חולות שהיו מתוכננות להיות כלולות במחקר) בגלל היתרון הגדול בהשגת תגובה פתולוגית מלאה שבאה לידי ביטוי בשלבים מוקדמים של המחקר[11].
בשנת 2011 פורסמו תוצאות מחקר TECHNO שבדק את היעילות והבטיחות של הוספת Herceptin לטיפול טרום ניתוחי בחולות עם ביטוי יתר של HER2. במחקר השתתפו 217 חולות שסבלו מגידול שממדיו גדולים מ-2 סנטימטר שקיבלו, בנוסף לטיפול הכימי, תוספת של Herceptin לפני הניתוח. הטיפול בתרופה זו נמשך שנה לאחר הניתוח. התגובה לטיפול (תגובה פתולוגית מלאה) הוגדרה כהיעדר מחלה חודרנית בשד או בבלוטות הלימפה. שיעור התגובה עמד על 39%, וניתוח משמר שד התאפשר בקרב 64% מהחולות. ההישרדות ללא מחלה עמדה על 88% בקבוצת הנשים עם תגובה פתולוגית מלאה, לעומת 73% בקבוצה ללא תגובה מלאה, ואילו ההישרדות ל-3 שנים עמדה על 96% לעומת 86%, בהתאמה. מסקנת הניסוי הייתה שתוספת Herceptin העלתה את שיעור התגובה הפתולוגית המלאה בגידולים עם ביטוי יתר של HER2, ובחולות אצלן הייתה תגובה פתולוגית מלאה, התוצאות לטווח ארוך היו טובות יותר. לעומתן, הקבוצה שבה נמצאה שארית גידול הייתה בסיכון להישנות מחלה ואף למוות[12].
התפתחות נוספת בטיפול הטרום ניתוחי בחולות עם ביטוי יתר של HER2 הייתה תוספת הנוגדן Perjeta (Pertuzumab). בשנת 2012 פורסם מחקר 417 NeoSphere בו חולות סרטן שד עם HER2 חיובי שהיו מיועדות לקבל טיפול טרום ניתוחי טופלו באופן אקראי באחד מ-4 הטיפולים הבאים:
- Docetaxel ו-Perjeta (הטיפול הסטנדרטי)
- docetaxel, Perjeta ו-Herceptin
- Perjeta ו-Herceptin
- docetaxel ו-Perjeta
אלו שקיבלו את כל 3 התרופות, Docetaxel, Perjeta ו-Herceptin, השיגו את שיעור התגובה הפתולוגית המלאה הגבוה ביותר - 45.8%, לעומת 29.0% בלבד בזרוע הטיפול הסטנדרטי. ממצא נוסף במחקר זה היה בזרוע של החולות שטופלו בנוגדנים בלבד, ללא כימותרפיה ציטוטוקסית (ללא Docetaxel) - 16.8% מהחולות השיגו תגובה פתולוגית מלאה. תוצאה זו מראה שגם כאשר נמנע מהחולות לקבל טיפול כימי בשל רעילותו, עדיין ניתן לטפל בהן באופן מוצלח יחסית, באמצעות נוגדנים בלבד[13].
ה-FDA (Food and Drug Administration) אישר טיפול ב-Perjeta יחד עם Herceptin וכימותרפיה, כטיפול טרום ניתוחי בסרטן שד עם HER2 חיובי.
ההגדרה והמשמעות הפרוגנוסטית של תגובה פתולוגית מלאה לאחר טיפול טרום ניתוחי בסוגים השונים של סרטן שד נבדקה באמצעות ניתוח מסכם (Pooled analysis) שכלל 7 מחקרים בטיפול טרום ניתוחי, בעבודה שנערכה בגרמניה שפורסמה בשנת 2012. סוגי הסרטן שנבדקו היו:
- Estrogen receptor) ER positive) ו/או Progesterone receptor) PgR positive) ו-HER2 negative ודרגה היסטולוגית 1 או 2 (Luminal A)
- ER positive ו/או PgR positive ו-HER2 positive או ER positive ו/או PgR Positive, HER2 negative ודרגה היסטולוגית 3 (Luminal B)
- PgR negative ,ER negative ו-HER2 positive
- ER negative, PgR negative ו-HER2 negative (TNBC, Triple negative Breast Cancer)
העבודה באה לענות על שתי סוגיות: האחת, חוסר אחידות בהגדרה של תגובה פתולוגית מלאה, והשנייה - העובדה שסרטן שד היא מחלה הטרוגנית. המשמעות הפרוגנוסטית של תגובה פתולוגית מלאה שונה בתתי הסוגים השונים של סרטן השד. המאמר כלל 6,377 חולות במסגרת 7 מחקרים אקראיים, בהם קיבלו המשתתפות טיפול טרום ניתוחי. נמצא הבדל משמעותי בהישרדות ללא מחלה בחולות ללא שארית מחלה חודרנית או גידול מסוג In situ, לעומת אלה שנמצאה אצלן שארית גידול מסוג חודרני או מסוג DCIS (Ductal Carcinoma In Situ). ממצא חשוב במחקר היה שהשגת תגובה פתולוגית מלאה שיפרה את שיעורי ההישרדות ללא מחלה בחולות שסבלו מאחד מסוגי הסרטן הללו: TNBC, HER2 חיובי עם PgR/ER שלילי וסרטן מסוג Luminal B עם HER2 שלילי. אך לא בגידולים מסוג Luminal A עם ER חיובי ו-HER2 שלילי, או מסוג Luminal B עם HER2 חיובי[5].
ניתוח מסכם (מחקר באמצעות שאלונים) שפורסם ביוזמת ה-FDA, אסף נתונים מ-12 מחקרים בין לאומיים (כולל 7 המחקרים מגרמניה שהוזכרו לעיל), בטיפול טרום ניתוחי בסרטן שד שכללו בסך הכל 11,955 חולות ומתוכם עבור 5,694 (52%) חולות נאסף מידע על תת-הסוג של המחלה. הזמן הממוצע של המעקב היה גבוה במקצת מ-5 שנים. בדומה לממצאי המחקר הגרמני, האנליזה הראתה קשר ישיר בין תגובה פתולוגית מלאה והישרדות בקרב חולות ב-3 תתי סוגים: סרטן שד מסוג HER2 pos, ER neg ו-PgR neg; בקבוצה של Luminal B; ובאלו עם TNBC. אלו גם הקבוצות עם האחוזים הכי גבוהים של תגובה פתולוגית מלאה. בנוסף לכך, עבודה זאת הראתה שלא היה הבדל משמעותי בין הגדרות של תגובה פתולוגית מלאה שמאפשר שארית מחלה In situ, או לא מאפשר שארית בכלל, בהשלכות על ההישרדות[14]. לכן ההגדרה של תגובה פתולוגית מלאה היא: ללא מחלה חודרנית בבלוטות או בשד, אך מחלה In situ עדיין מקובלת כסטנדרט[15]. בשתי העבודות, חלק ניכר מהחולות עם מחלת HER2 חיובי, לא קיבלו Herceptin מכיוון שהן חלו לפני העידן שבו טיפול זה הוכח כיעיל, בטיפול משלים או טרום ניתוחי[5],[14].
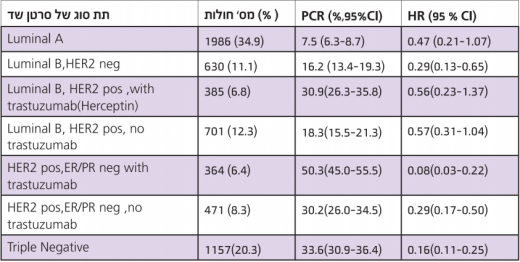
תוצאות של 5,694 חולות מ-12 מחקרים באנליזה של Cortazar. ככל שה-HR יותר נמוך השגת תגובה פתולוגית מלאה משפיעה באופן חיוני יותר על ההישרדות
Cortazar, et al. Pathological complete response and long-term clinical benefit in breast cancer: the CTNeoBC pooled analysis. Lancet. Feb 14 [13]
בטבלה ניתן לראות שאחוזי התגובה הפתולוגית המלאה מגיעים ל-50% בקרב חולות שקיבלו Herceptin עם תת-סוג HER2 חיובי ו-ER/PR שלילי. יחס הסיכון (Hazard ratio) הנמוך - 0.08, מראה שהתגובה הפתולוגית המלאה בתת-סוג זה, מעלה משמעותית את הסיכוי להישרדות[14].
עבודה שנערכה במרכז הסרטן MD Anderson בשנת 2008, השוותה תגובה לטיפול כימי טרום ניתוחי והישרדות בחולות עם סרטן שד מסוג TNBC, לעומת סוגי סרטן אחרים. נמצא, ששיעור התגובה הפתולוגית המלאה היה כפול בקבוצת ה-TNBC, לעומת הקבוצה שכללה חולות עם סוגים אחרים של סרטן שד Non-TNBC (22% לעומת 11%), אך למרות הנתון הזה, שיעור ההישרדות ל-3 שנים היה נמוך משמעותית בקבוצת ה-TNBC. בחולות שהשיגו תגובה פתולוגית מלאה, לא נמצא הבדל בהישרדות בין שתי הקבוצות. בחולות בהן נמצאה שארית מחלה, ההישרדות ל-3 שנים הייתה נמוכה משמעותית בקבוצת ה-TNBC בהשוואה לנשים שנכללו בקבוצת ה-Non-TNBC[16].
נעשו ניסיונות נוספים לשפר את תוצאות הטיפול הטרום ניתוחי על ידי שימוש בתרופות חדשות וותיקות. בשנת 2012 בדקה קבוצת NSABP תוספת של Gemcitabine ו-Capecitabine לטיפול הטרום ניתוחי אך לא נמצא שיפור מבחינת שיעורי התגובה הפתולוגית המלאה, שכן כתוצאה מנטילת תרופות אלה עלה שיעור הרעילות. בחלקה השני של העבודה בדקו החוקרים תוספת של Avastin (Bevacizumab) - נוגדן חד שבטי הפועל נגד VEGF (Vasculare Endothelial Growth Factor). החוקרים מצאו שתוספת זו הביאה לעלייה מתונה אך משמעותית בשיעור התגובה הפתולוגית המלאה בשד, אך לא בבלוטות הלימפה. ממצאים אלה היו תקפים בעיקר עבור חולות עם קולטנים חיוביים לאסטרוגן, מה שמרמז על אפקט הרבה פחות משמעותי מבחינת התוצאות לטווח ארוך. נוסף על כך, מתן Avastin העלה בצורה משמעותית את מספר האירועים הטוקסיים - בעיקר הלבביים[17].
טיפול ביולוגי, במעכב mTOR, Everolimus, נחקר עדיין (נכון לשנת 2015), ובשלב זה לא נראה כי הטיפול העלה את אחוז התגובה הפתולוגית המלאה, כאשר התווסף ל-Paclitaxel בטיפול טרום ניתוחי[18].
טיפול קרינתי
יש להעריך את ההשלכות של טיפול כימי טרום ניתוחי על טיפול בקרינה המכוון לשד ולבלוטות הלימפה שמנקזות אותו. במשך מספר עשורים ההתוויות לטיפול קרינתי הסתמכו על בדיקת הרקמה הגידולית כולה, יחד עם בלוטות הלימפה שהוצאו בניתוח לפני התחלת הטיפול הסיסטמי. יש עדות ממחקרים קליניים שתגובה פתולוגית מלאה יכולה להוריד את הסיכון להישנות מקומית. לכן התגובה לטיפול כימי טרום ניתוחי הפכה לחלק מהשיקולים בהחלטה על טיפול בקרינה, לאחר טיפול בכימותרפיה טרום ניתוחית, וניתוח. לגבי קרינה אחרי טיפול טרום ניתוחי, אין תמימות דעים בדבר הוראות לטיפול.
אחד המחקרים שטרם הסתיים (נכון לשנת 2015), בודק האם יש צורך להקרין בלוטות בבית השחי במקרים בהם הטיפול הטרום ניתוחי הפך את הבלוטות שהיו מעורבות באבחנה, למצב ללא מחלה [(NSABP B51/RTOG 1304) (PCR)][19].
טיפול קרינתי נכון חשוב על מנת להפחית את הסיכון להישנות מקומית ואזורית, וכנראה גם לתוצאות לטווח הארוך, אך הוא כרוך בתופעות לוואי לא רצויות. כאשר הטיפול הכימי ניתן לפני הניתוח, ממדי הגידול ומעורבות הבלוטות שנמצאים בניתוח, אינם זהים לאלה שהיו בעת האבחנה.
מכאן עולה כי יש צורך בהערכה מחודשת ובחינה של ההתוויות לקרינה בעידן הטיפול הכימי הטרום ניתוחי. אין מחקרים מבוקרים גדולים שמאפשרים שינוי של ההחלטה. העבודה הגדולה ביותר בנושא זה, היא של Mamounas וחבריו, בה נמצא שנשים שעברו כריתת שד ובלוטות לימפה ולא נמצאה אצלן שארית גידול בשד ובבלוטות (הדבר נכון במיוחד לקבוצה בה בלוטות חיוביות התבררו כשליליות), שיעור ההישנות המקומית היה נמוך מאד, ולכן ניתן היה לשקול האם אפשר להימנע אצל חולות אלו ממתן טיפול קרינתי משלים. לעומתן, בקרב חולות שאצלן לא הושגה תגובה פתולוגית מלאה, במיוחד כאשר שארית הגידול נמצאה בבלוטות הלימפה, שיעור ההישנות המקומית והאזורית ללא קרינה היה גבוה (11-22%), לכן לקבוצת חולות זו, הומלץ על טיפול בקרינה לאחר הניתוח[20].
טיפול הורמונלי
כיוון נוסף של טיפול תרופתי טרום ניתוחי, הוא טיפול אנדוקריני ראשוני (הורמונותרפיה טרום ניתוחית), המהווה אפשרות טיפול נוספת בגידולים המבטאים רמות גבוהות של הקולטן לאסטרוגן. המטרות זהות לאלה של טיפול כימי ראשוני, קרי צמצום מסת הגידול על מנת לאפשר ניתוח בכלל וניתוחים משמרי שד בפרט. עבודות שהשוו בין מתן Tamoxifen לתרופות מקבוצת מעכבי ארומטז (Aromatase inhibitor) בנשים אחרי גיל הבלות, מצאו יתרון מבחינת תגובת הגידול ושיעור הניתוחים משמרי השד, בעקבות טיפול בתרופות אלה. ברוב העבודות נמצא שכאשר משך הטיפול עולה על שלושה חודשים, התגובה טובה יותר.
אין עבודות רבות המשוות בין מתן כימותרפיה לטיפול אנדוקריני טרום ניתוחי. עם זאת זוהי אופציית טיפול טובה[21], בעיקר עבור נשים מבוגרות עם גידולים גדולים בשד שמתאפיינים בקולטנים חיובים לאסטרוגנים.
בדיקות מולקולריות
על מנת לסייע לחולות להחליט על טיפול (טיפול טרום ניתוחי לעומת ניתוח, או טיפול כימי טרום ניתוחי לעומת טיפול אנדוקריני), נבדק שימוש בבדיקה המולקולרית 21-Gene Recurrence Score (Oncotype-DX) באמצעותה ניתן להעריך מהו הסיכון להישנות הגידול על בסיס ביטוי של 21 גנים הנבדקים על ידי מדידת RNA. כבר בשנת 2005 פרסמו Gianni וחבריו עבודה בה נבדק בין היתר ה-Recurrence Score) RS) בקרב 89 חולות סרטן שד שקיבלו טיפול כימי טרום ניתוחי. התברר כי ככל שה-RS היה גבוה יותר, הסיכויים לתגובה פתולוגית מלאה עלו[22].
עבודה אחרת מיפן, שפורסמה בשנת 2013, בדקה קשר בין RS נמוך, בינוני, וגבוה באמצעות בדיקת 21-Gene Recurrence Scored, וטיפול אנדוקריני טרום ניתוחי בחולות סרטן שד חיובי לאסטרוגן, ובחולות לאחר גיל הבלות שטופלו ב-Exemestane. החולות נבדקו במשך 24 שבועות, ולאחריהם נותחו. ה-RS בוצע על ביופסיית הגידול או הפרפרט הניתוחי. נמצא שבקרב נשים עם RS נמוך ובינוני, התגובה לטיפול האנדוקריני הייתה גבוהה, כאשר ל-59% מהחולות הייתה נסיגה לפחות חלקית של המחלה בצורה משמעותית. לעומתן, בקבוצה עם RS גבוה התגובה לטיפול האנדוקריני הייתה נמוכה - רק אצל 20% הייתה נסיגה של המחלה. כמו כן שיעור הניתוחים משמרי השד היה גבוה יותר בקרב חולות עם RS נמוך מאשר בקרב חולות בעלות RS גבוה[23].
ביבליוגרפיה
- ↑ Hortobagyi GN, Blumenschein GR, Spanos W, et al. Multimodal treatment of locoregionally advanced breast cancer. Cancer. 1983 Mar 1;51(5): 763-768.
- ↑ Gralow JR, Burstein HL, Wood W, et al. Preoperative therapy in invasive breast cancer: pathologic assessment and systemic therapy issues in operable disease. J Clin Oncol. 2008 Feb 10;26(5):814-9.
- ↑ 3.0 3.1 3.2 von Minckwitz G, Blohmer JU, Costa SD, et al. Response-guided neoadjuvant chemotherapy for breast cancer. J Clin Oncol. 2013 Oct 10;31(29):3623-30. Epub2013 Sep 3.
- ↑ Boughey JC, Suman VJ, Mittendorf EA, et al. Sentinel lymph node surgery after neoadjuvant chemotherapy in patients with node-positive breast cancer: the ACOSOG Z1071 (Alliance) clinical trial. JAMA. 2013 Oct 9;310(14):1455-61.
- ↑ 5.0 5.1 5.2 von Minckwitz G, Untch M, Blohmer JU,et al. Definition and impact of pathologic complete response on prognosis after neoadjuvant chemotherapy in various intrinsic breast cancer subtypes. J Clin Oncol. 2012 May 20;30(15): 1796¬804. Epub 2012 Apr 16.
- ↑ Early Breast Cancer Trialists' Collaborative Group (EBCTCG). Effects of chemotherapy and hormonal therapy for early breast cancer on recurrence and 15-year survival: an overview of the randomized trials. Lancet. 2005 May 14-20:365(9472): 1687-717.
- ↑ Rastogi P, Anderson SJ, Bear HD, et al. Preoperative chemotherapy: updates of National Surgical Adjuvant Breast and Bowel Project Protocols B-18 and B-27. J Clin Oncol. 2008 Feb 10;26(5):778-85.
- ↑ Cuppone F, Bria E, Carlini P, et al.. Taxanes as primary chemotherapy for early breast cancer: meta-analysis of randomized trials. Cancer. 2008 Jul 15;113(2):238-46.
- ↑ Untch M, Mobus V, Kuhn W, et al. Intensive dose-dense compared with conventionally scheduled preoperative chemotherapy for high-risk primary breast cancer. J Clin Oncol. 2009 Jun 20:27(18):2938-45. Epub 2009 Apr 13.
- ↑ Horak CE, Pusztai L, Xing G, et al. Biomarker analysis of neoadjuvant doxorubicin/cyclophosphamide followed by ixabepilone or paclitaxel in early-stage breast cancer. Clin Cancer Res. 2013 Mar 15:19(6):1587-95. Epub 2013 Jan 22.
- ↑ Buzdar AU, Ibrahim NK, Francis D, et al. Significantly higher pathologic complete remission rate after neoadjuvant therapy with trastuzumab, paclitaxel, and epirubicin chemotherapy: results of a randomized trial in human epidermal growth factor receptor 2-positive operable breast cancer. J Clin Oncol. 2005 Jun 1:23(16)3676-85. Epub 2005 Feb 28.
- ↑ Untch M, Fasching PA, Konecny GE, et al. Pathologic complete response after neoadjuvant chemotherapy plus trastuzumab predicts favorable survival in human epidermal growth factor receptor 2-overexpressing breast cancer: results from the TECHNO trial of the AGO and GBG study groups. J Clin Oncol. 2011 Sep 1;29(25):3351-7. Epub 2011 Jul 25.
- ↑ Gianni L, Pienkowski T, Im YH, et al. Efficacy and safety of neoadjuvant pertuzumab and trastuzumab in women with locally advanced, inflammatory, or early HER2-positive breast cancer (NeoSphere): a randomized multicentre, open-label, phase 2 trial. Lancet Oncol. 2012 Jan;13(1 ):25-32. Epub 2011 Dec 6.
- ↑ 14.0 14.1 14.2 Cortazar P, Zhang L, Untch M, et al. Pathological complete response and long-term clinical benefit in breast cancer: the CTNeoBC pooled analysis. Lancet. 2014 Jul 12:384(9938); 164-72. Epub 2014 Feb 14.
- ↑ Berruti A, Generali D, Kaufmann M, et al. International expert consensus on primary systemic therapy in the management of early breast cancer: highlights of the Fourth Symposium on Primary Systemic Therapy in the Management of Operable Breast Cancer, Cremona, Italy (2010). J Natl Cancer Inst Monogr. 2011:2011(43): 147-51.
- ↑ Liedke C, Mazouni C, Hess KR, et al. Response to neoadjuvant therapy and long-term survival in patients with triple-negative breast cancer. J Clin Oncol. 2008 Mar 10;26(8):1275-81. Epub 2008 Feb 4.
- ↑ Bear HD, Tang G, Rastogi P, et al. Bevacizumab added to neoadjuvant chemotherapy for breast cancer. N Engl J Med. 2012 Jan 26;366(4):310-20.
- ↑ Huober J, Fasching PA, Hanusch C, etal. Neoadjuvant chemotherapy with paclitaxel and everolimus in breast cancer patients with non-responsive tumours to epirubicin/cyclophosphamide (EC) ± bevacizumab - results of the randomized GeparQuinto study (GBC 44). Eur J Cancer. 2013 Jul;49(10):2284-93. Epub 2013 Mar 27.
- ↑ White J, Mamounas E. Locoregional radiotherapy in patients with breast cancer responding to neoadjuvant chemotherapy: a paradigm for treatment individualization. J Clin Oncol. 2014 Feb 20;32(6):494-5. Epub 2013 Dec 30.
- ↑ Mamounas EP, Anderson SJ, Dignam JJ, et al. Predictors of locoregional recurrence after neoadjuvant chemotherapy: results from combined analysis of National Surgical Adjuvant Breast and Bowel Project B-18 and B-27. J Clin Oncol. 2012 Nov 10;30(32):3960-6. Epub 2012 Oct 1.
- ↑ Freedman OC, Verma S, demons MJ. Using aromatase inhibitors in the neoadjuvant setting: evolution or revolution? Cancer Treat Rev. 2005 Feb;31(1):1-17. Epub 2004 Nov 18.
- ↑ Gianni L, Zambetti M, Clark K et al. Gene expression profiles in paraffin-embedded core biopsy tissue predict response to chemotherapy in women with locally advanced breast cancer. J Clin Oncol. 2005 Oct 10;23(29):7265-77. Epub 2005 Sep 6.
- ↑ Ueno T, Masuda N, Yamanaka T, et al. Evaluating the 21-gene assay Recurrence Score® as a predictor of clinical response to 24 weeks of neoadjuvant exemestane in estrogen receptor-positive breast cancer. Int J Clin Oncol. 2013 Oct 8. [Epub ahead of print]
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר רוית אגסי - כירורגית בכירה, מרכז אשכול לבריאות השד, המרכז הרפואי האוניברסיטאי סורוקה, הפקולטה למדעי בריאות, אוניברסיטת בן-גוריון בנגב, באר שבע ופרופ' דויד גפן - מנהל יחידת טיפול יום אונקולוגי, המרכז הרפואי האוניברסיטאי סורוקה, הפקולטה למדעי הבריאות אוניברסיטת בן- גוריון בנגב, באר שבע


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק