סרטן השד - שוליים בניתוח משמר שד - Breast cancers - borders in breast conserving surgery
| סרטן השד - שוליים בניתוח משמר שד | ||
|---|---|---|
| Breast cancers - borders in breast conserving surgery | ||
| יוצר הערך | ד"ר תניר אלוייס | |
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – סרטן השד
טיפול מקומי בסרטן שד הכולל כריתה חלקית עם שוליים נקיים, מהווה במשך שנים רבות את החלופה הטובה ביותר עבור חולות סרטן השד, שנמצאו מתאימות להליך זה. עם זאת, ההגדרה של שוליים נקיים השתנתה לאורך השנים.
מעורבות השוליים מהווה את גורם הסיכון העיקרי לחזרה מקומית במיטת הגידול. נוכחות גידול בשולי התכשיר, מעלה באופן משמעותי את הסיכון לחזרה מקומית של המחלה הן בגידולים חודרניים והן בגידולים מסוג DCIS (Ductal Carcinome In Situ).
הערכה תוך ניתוחית של נוכחות גידול מיקרוסקופי בשולי פרפרט אינה מדויקת. על פי מחקרים שונים 15-40% מן הנשים שעוברות ניתוח משמר שד, נזקקות לניתוח חוזר בשל מעורבות שוליים[1]. קיימות מספר טכנולוגיות המסייעות למנתח לבצע הערכה תוך ניתוחית של השוליים, ובכר להוריד את הסיכון לניתוח חוזר.
ניתוח משמר שד (Lumpectomy)
ניתוח משמר שד הוא הניתוח הנפוץ ביותר לטיפול בסרטן השד, והוא מתבצע בתדירות גבוהה - 60-70% מן המאובחנות החדשות תעבורנה ניתוח משמר שד. מספר מחקרים שנערכו בשנות ה-70 של המאה הקודמת הראו כי טיפול בסרטן השד באמצעות כריתת שד חלקית בתוספת טיפול קרינתי משלים, יעיל כמו כריתת שד מלאה, בהתייחס לסיכויי ההחלמה והסיכון להישנות המחלה[2],[3]. הבשורה על ניתוחים אלה יצאה אמנם ממילאנו ומפילדלפיה, אך עד מהרה התפשטה בעולם. נשים שחלו בסרטן השד העדיפו באופן טבעי לשמר את השד ככל שניתן. הדרישה מצד החולות לניתוחים משמרי שד, השפיעה על כירורגים רבים, בהם כאלה שנחשבו לשמרנים, ובמהרה הפך ניתוח זה, לטיפול הנפוץ ביותר כנגד סרטן השד.
המטרה בניתוח משמר שד, היא כריתה מלאה של הגידול מחד, ושמירה אופטימלית על צורת השד, מאידך. מטרה זו מהווה אתגר לכל כירורג שעוסק בניתוחי שד: ככל שהכריתה רחבה יותר, הסיכון להיווצרות עיוות בשד, גבוה יותר. שתי המטרות הללו, כריתה מקסימלית לעומת שימור מקסימלי, הן לכאורה מטרות סותרות, ומציאת האיזון המיטבי בין שתי המטרות הללו הוא האתגר העיקרי בניתוחים משמרי שד.
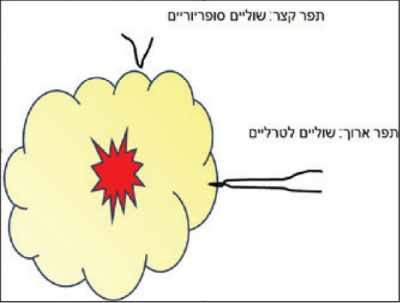
תשובה פתולוגית מלאה אחרי כריתת שד חלקית, כוללת מדידה של המרחק מן השוליים, בכל אחת משש הפאות של התכשיר (קדמי, אחורי, עליון, תחתון, מדיאלי ולטרלי). על מנת לקבל תמונה מלאה לגבי מעורבות השוליים, חשוב לסמן את התכשיר באופן כזה, שהאוריינטציה של התכשיר תהיה ברורה לפתולוג. הסימון נעשה בדרך כלל על ידי סימון שולי התכשיר בתפרים באופן מוסכם (איור 1). סימון זה מאפשר לפתולוג לדווח מהו המרחק מהשוליים, הן של הגידול החודרני והן של המרכיב הטרום סרטני הקיים בחלק גדול מן הגידולים החודרניים.
שוליים תקינים
ארגון NCCN (National Comprehensive Cancer Network), המפרסם מידי שנה המלצות קליניות לטיפול בסוגי סרטן שונים, על סמר ספרות עדכנית ופרסומים אחרונים, ממליץ על שוליים שאורכם עולה על מילימטר אחד, לגידולים חודרניים וטרום חודרניים. במקרים בהם הגידול הוא טרום חודרני ממקור אוניות השד LCIS (Lobular Carcinoma In Situ), הגידול נחשב כסמן של סיכון מוגבר בלבד ולא מצב טרום סרטני ולפיכך אין צורך בשוליים נקיים.
האיגודים האמריקאים לכירורגיה אונקולוגית ורדיותרפיה פירסמו הנחיות[4] המבוססות על מטא-אנליזה של 33 מחקרים בהשתתפות למעלה מ-28,000 חולות. ממחקרים אלה עולות שתי נקודות חשובות:
- היעדר תאי גידול בשולי הכריתה מהווים שוליים נקיים בניתוחי שד, גם כאשר מדובר בשוליים צרים ביותר (שכבת תאים בודדת)
- נוכחות של תאי גידול בשוליים מהווה גורם סיכון משמעותי לחזרה מקומית של גידול ומצריכה ניתוח חוזר
הערכת השוליים במהלך הניתוח
מידע מלא לגבי מרחק הגידול מן השוליים הניתן במהלך הניתוח, מפחית את הצורך בניתוחים חוזרים. ישנם מספר כלים העומדים לרשות המנתח בזמן הניתוח, באמצעותם ניתן להעריך את המרחק מן השולים:
מישוש: בגושים הניתנים למישוש, אפשר להעריך אם הגוש קרוב לשולי הכריתה. במקרה כזה יש צורך להרחיב את הפאה הנגועה מייד. הבעיה נעוצה בכך שמישוש אינו מזהה אזורי גידול שאינם גושיים, ולכן הסתמכות על מישוש בלבד - אינה אמינה.
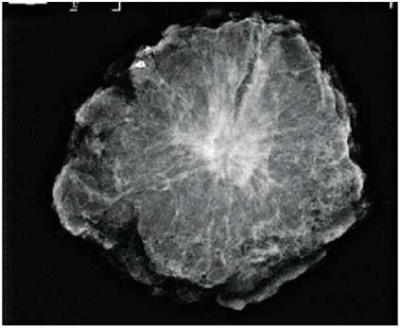
צילום פרפרט: ניתן לבצע צילום רנטגן של התכשיר שהוצא בניתוח, על מנת להעריך את המרחק מן השוליים. צילום רנטגן של הפרפרט יעיל רק במקרים בהם הגידול נראה בממוגרפיה (איור 2), כשם שאולטרסאונד של הפרפרט, יעיל רק בגידולים שנראו במקור באולטרסאונד. צילום של התכשיר חיוני בעיקר בגידולים שאינם ניתנים למישוש, אך הוא יכול לתרום גם כאשר מדובר בגידולים אותם ניתן למשש. צילום רנטגן אינו מדגים גידול מיקרוסקופי, ולכן גם במקרים בהם הצילום מדגים מרחק טוב מהשוליים, תתכן תשובה פתולוגית בה נראה כי הגידול מגיע לשוליים, ולפיכך יש צורך בניתוח חוזר.
הערכה מיקרוסקופית תוך ניתוחית של השוליים
חיתוך של הפרפרט שהוצא אפשרי, אך אינו מדויק וכך גם הערכה מיקרוסקופית של מרחק הגידול מן השוליים - הערכה כזו במהלך הניתוח אינה מעשית ממספר סיבות: ראשית יש צורך בהערכה של כמות רקמה גדולה, דבר שעשוי לקחת זמן רב. בנוסף, רקמת השד שומנית ברובה, ולכן ישנו קושי טכני משמעותי לקבל חתכים קפואים באיכות טובה מרקמה כזו. כמו כן, בחתך קפוא ייתכנו ארטיפקטים רבים, והרקמה שנבדקת באמצעותו אינה יכולה לשמש לחתכים קבועים ולכן למעשה - הולכת לאיבוד.
MarginProbe: מכשיר Win להערכת השוליים במהלך הניתוח
מכשיר ה-MarginProbe הוא פרי פיתוח ישראלי, שייחודו מתבטא בכך שהוא מסוגל להבחין ברמת דיוק גבוהה בין רקמת גידול לרקמה תקינה על סמך תכונות חשמליות של הרקמה.
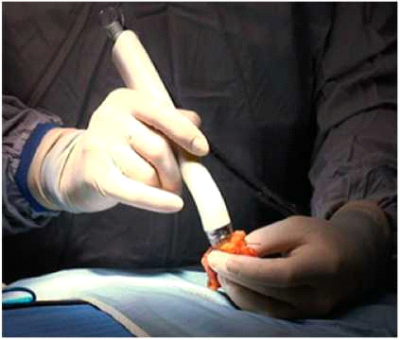
אחרי כריתת הגוש, המנתח מודד באמצעותו את שולי התכשיר מכל הכיוונים (איור 3). המכשיר נותן משוב לכל מדידה תוך פחות משנייה, ובפאות בהן הוא מזהה גידול קרוב לשוליים, המנתח יכול לבצע הרחבה מידית ואף למדוד אותה בעזרת המכשיר. במחקר מבוקר רנדומלי נמצא שהשימוש ב-MarginProbe הפחית את הצורך בניתוחים חוזרים ב-56%[5],[6]. המכשיר קיבל את אישור מנהל המזון והתרופות האמריקאי (FDA, Food and Drug Administration) והוא משווק בארצות הברית ובארץ.
ביבליוגרפיה
- ↑ Veronesi U et al. Breast conservation is a safe method in patients with small cancer of the breast. Long-term results of three randomised trials on 1,973 patients Eur J Cancer. 1995 Sep;31A(10):1574-9.
- ↑ Fisher B et al. Reanalysis and results after 12 years of follow-up in a randomized clinical trial comparing total mastectomy with lumpectomy with or without irradiation in the treatment of breast cancer. N Engl J Med. 1995 Nov 30;333(22):1456-61.
- ↑ McCahill LE, et al. Variability in reexcision following breast conservation surgery JAMA. 2012 Feb I ;307(5)1467-75.
- ↑ Moran MS et al. Society of Surgical Oncology-American Society for Radiation Oncology Consensus Guideline on Margins for Breast-Conserving Surgery With Whole-Breast Irradiation in Stages I and II Invasive Breast Cancer. Int J Radiat Oncol Biol Phys. 2014 Mar 1;88(3):553-64.
- ↑ Allweis TM, et al. A prospective, randomized, controlled, multicenter study of a real-time, intraoperative probe for positive margin detection in breast-conserving surgery Am J Surg. 2008 Oct;196(4):483-9
- ↑ Schnabel F, et al. A Randomized Prospective study of lumpectomy Margin Assessment with Use of MarginProbe in patients with nonpable breast malignancies. Ann Surg Oncol. 2014 May;21(5): 1589-1595.
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר תניר אלוייס - כירורגית שד, מנהלת המרכז לבריאות השד ע"ש שרה מרקוביץ', המרכז הרפואי קפלן, רחובות


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק