צריבה של רפרוף ופרפור פרוזדורים - Ablation of atrial flutter and atrial fibrillation
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| צריבה של רפרוף ופרפור פרוזדורים | ||
|---|---|---|
| Ablation of atrial flutter and atrial fibrillation | ||
| יוצר הערך | ד"ר חורחה שליאמסר
|
|
לערכים נוספים הקשורים לנושא זה, ראו את דף הפירושים – פרפור פרוזדורים
רפרוף פרוזדורים (ר"פ; Atrial Flutter) ופרפור פרוזדורים (פ"פ; Atrial Fibrillation) הן הפרעות קצב עלייתיות שכיחות הגורמות לתחלואה משמעותית. סקירה זו עוסקת בטיפול בצריבה של ר"פ טיפוסי ופ"פ.
צריבה בגלי רדיו של רפרוף פרוזדורים
רקע
ר"פ טיפוסי (Type 1) היא הפרעת קצב המופיעה לעתים באסוציאציה עם פ"פ, ועלולה לגרום לסימפטומים ולתחלואה דומים לאלו של פ"פ.
לעתים, כמו במקרה של פ"פ, ר"פ עלול לגרום לקרדיומיופתיה על רקע של תגובה חדרית מהירה (Tachycardia Induced Cardiomyopathy).
שיעור ר"פ הוא כ-15% מכלל הפרעות הקצב העל-חדריות, ויכול להופיע באופן פרוקסיסמלי בחולים ללא מחלה מבנית, או שבאופן כרוני, בחולים עם פתולוגיה מסתמית, איסכמית או קרדיומיופתיה.
פתופיזיולוגיה
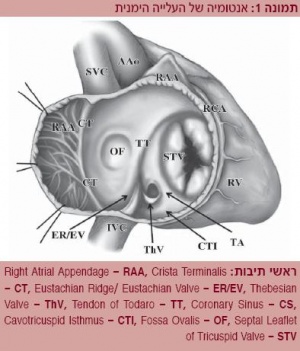
היכרות מעמיקה עם האנטומיה של העלייה הימנית (תמונה 1) הכרחית לצורך הבנת המנגנונים האלקטרופיזיולוגיים העומדים בבסיס ר"פ.
אנטומיה של העלייה הימנית
בעלייה הימנית יש מספר פתחים ושרידים אנטומיים הקשורים להתפתחות האמבריונלית.
הפתחים כוללים את הווריד הנבוב העליון והווריד הנבוב התחתון, הנמצאים בחלק העליון והתחתון של העלייה, בהתאמה.
באנדוקרד של העלייה ניתן להבחין בשני סוגי רקמה שונים: אנדוקרד עם טרבקולות בחלק הקדמי-צדדי (אוזנית - Right Atrial Appendage) ואנדוקרד חלק בחלק האחורי, ממקור אמבריונלי שונה. מפריד ביניהם מבנה שרירי מעובה בצורת סהר, הקרוי CT (Crista Terminalis). מבנה זה משתרע מהחלק העליון של הספטום הבין-עלייתי, עובר קדמית לפתח של הווריד הנבוב העליון, ומשם עם מהלך אחורי-צדדי מסתיים קדמית לפתח של הווריד הנבוב התחתון. מאזור זה ממשיך ה-EV/ER (Eustachian Valve Ridge), שריד אמבריונלי של המסתם של הסינוס ונוזוס בעל מרקם פיברו-מוסקולורי. רכס זה ממשיך עד לפתחו של הסינוס הקורונרי (CS), שם מתחבר ל-Thebesian Valve. מפגשם יוצר את הגיד ע"ש Todaro. האזור בין הווריד הנבוב התחתון והמסתם הטריקוספידלי בחלק התחתון של העלייה הימנית הוא אזור צר הקרוי מצר (Cavotricuspid Isthmus – CTI). החלק התחתון של טבעת המסתם הטריקוספידלי ממוקם קדמית ל-ER (4-1 ס"מ).
אלקטרופיזיולוגיה
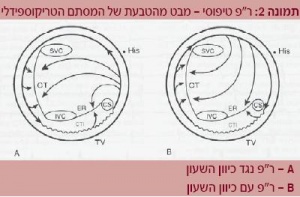
ר"פ נוצר בשל שילוב של הולכה חשמלית איטית באזור המצר (Isthmus) וחסם הולכה אנטומי'פזיולוגי באזור ה-CT וה-ER. תנאים אלו מאפשרים היווצרות מעגל Reentry מתמשך. בתמונה 2 מודגמים שני מעגלי הרפרוף הנפוצים.
פעימות עלייתיות מוקדמות או אירועים קצרים של פ"פ נמנים עם הגורמים (Triggers) לר"פ. מקורם בעלייה השמאלית ובוורידי הריאה, בהתאמה. לאחר התנעת ר"פ, הפעלת העלייה השמאלית מתרחשת באופן פסיבי ע"י הולכה דרך המחיצה הבין-עלייתית ו'או ע"י הולכה דרך הצרור ע"ש Bachman.
לנוכח העובדה שר"פ הוא הפרעת קצב עמידה באופן יחסי לטיפול פרמקולוגי, הן בגישה של Rhythm Control והן בגישה של Rate Control, הטיפול הפולשני ע"י אבלציה תפס מקום מרכזי בשנים האחרונות והוא היום טיפול הבחירה בר"פ.
קלסיפיקציה
ניתן לסווג ר"פ לשתי קבוצות עיקריות:
- טיפוסי או תלוי מצר וריד נבוב-מסתם טריקוספידלי
- לא טיפוסי
ר"פ טיפוסי או תלוי מצר (CTI Dependent Atrial Flutter) הוא הפרעת קצב הנגרמת בשל Reentry שמתרחש כולו בעלייה הימנית. המעגל של הפרעת הקצב תחום אנטריורית ע"י המסתם הטריקוספידלי ופוסטריורית ע"י הוורידים הנבובים, ה-Crista Terminalis וה-Eustachian Ridge.
אזור המצר (CTI) הוא החלק הצר של מעגל ה-Reentry ועל כן הוא מטרה מתאימה לביצוע אבלציה. המעגל של ר"פ טיפוסי מתואר על פי תנועתו סביב הטבעת של המסתם הטריקוספידלי. ברוב המקרים (90%) כיוונו נגד כיוון השעון, (Counter Clockwise) CCW, ובמיעוט המקרים עם כיוון השעון Clockwise) CW או Reverse Typical Atrial Flutter).
רפרוף נוסף, אך נדיר, המערב גם את המצר, הוא Lower Loop Reentry. וריאנט זה, מקורו במעגל חשמלי מסביב לווריד הנבוב התחתון. ר"פ לא טיפוסי מתייחס לכל טכיקרדיה עלייתית (ימנית או שמאלית) במנגנון של Macro Reentry שאינו תלוי ב-CTI. קצרה היריעה מלהכיל קבוצה זו בסקירה הנוכחית, אך חשוב לציין, שהפרעות קצב מעין אלו עלולות להופיע כסיבוך של ניתוחים לבביים, צריבות כירורגיות (Maze Procedure ודומיו) וצריבות של פ"פ'ר"פ.
אק"ג
לגלי P או לגלי F של ר"פ יש בדרך כלל מורפולוגיה, ציר וזמן מחזור קבועים.
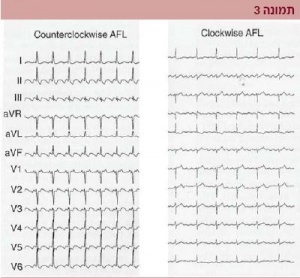
בר"פ נגד סיבוב השעון ניתן לזהות באק"ג טכיקרדיה עלייתית סדירה בקצב של 340-240 לדקה, עם גלי F בצורת מסור, שליליים בחיבורים תחתונים (חיוביים בר"פ עם סיבוב השעון).
גלי F ב- V1ב-CCW הם חיוביים (שליליים או איזואלקטריים ב-CW) (תמונה 3).
ההולכה לרוב 2:1, או בכפולות.
קליניקה
בדומה לקליניקה של פ"פ, מאופיין ר"פ בתסמינים של דפיקות לב, עייפות, סחרחורת וקוצר נשימה. בכ-60% מהמקרים ר"פ מתלווה למחלה חריפה, כמו ניתוחים, החמרה של מחלה ריאתית ועוד.
טיפול
כמו במקרה של פ"פ, הטיפול בר"פ מבוסס על מניעת סיבוכים טרומבו-אמבוליים וגישה של Rhythm Control או Control Rate.
תוצאות הטיפול בשתי הגישות האחרונות פחות טובות מאשר בפ"פ, על כן, ולאור יעילות ובטיחות של טיפול בצריבה של ר"פ, האחרון הוא היום טיפול הבחירה.
עקרונות הטיפול בצריבה: מקור האנרגייה הנפוץ בשימוש באבלציות הוא גלי רדיו (RF). אפליקציה של אנרגייה זו מחממת את הרקמה וגורמת נמק שמטרתו לקטוע מעגלי Reentry או להעלים מוקדים אוטומטיים.
מקור זה מבוסס על שימוש בזרם חילופין בתדר שאינו גורם לדפולריזציה של המיוקרד (~500kHz) ובמתח נמוך (40V), הניתן בין קצה הקתטר (Tip) לאלקטרודת ייחוס הנמצאת על עור החולה (Skin Patch).
טיפול בצריבה של ר"פ: תחילה יש לאמת את האבחנה של ר"פ טיפוסי ע"י בחינת תבנית האקטיבציה החשמלית של הרפרוף. במקום ראשון יש להוכיח שאכן מדובר במנגנון של Reentry ולא בטכיקרדיה מוקדית, ובמקום שני, שה-CTI הוא חלק ממעגל זה.
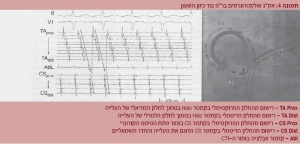
לצורך זה מקובל להשתמש בקתטר עם 20 אלקטרודות (Halo) שממוקם סביב הטבעת של המסתם הטריקוספידלי. קתטרים נוספים ממוקמים בצרור ע"ש His ובסינוס הקורונרי (תמונה 4).
בר"פ מטרת הצריבה היא לקטוע את מעגל ה-Reentry באזור הצר ביותר במעגל, שהוא כאמור, ה-CTI. יתרון נוסף של ה-CTI כאתר מטרה לצריבה, הוא השיעור הנמוך של פרפורציות או גרימת נזק לקשרית ה-AV.
מיפוי בתלת-ממד (Electroanatomical Mapping) ע"י מערכות, כגון CARTO או NavX, מאפשר הבנה של האקטיבציה החשמלית ע"י תצוגה חזותית של התפשטות האריתמיה בתוך העלייה (תמונה 5).
לאחר השלב האבחנתי, קתטר צריבה מוחדר דרך הווריד הפמורלי, וממוקם באזור המצר. קצה הקתטר נמצא בחלק התחתון של הטבעת של המסתם הטריקוספידלי.
על ידי צריבת ה-CTI מושג נתק חשמלי במעגל הפרעת הקצב. הצריבה מבוצעת ע"י אפליקציה של RF באופן נקודתי או רציף, כדי ליצור צלקת רציפה. הקו נמתח באזור ה-CTI, בין הטבעת של המסתם הטריקוספידלי לבין הווריד הנבוב התחתון (תמונה 6).
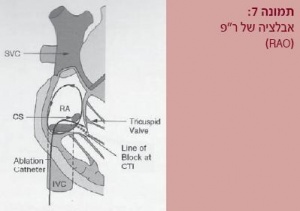
בשיטה הקונוונציונלית נעזרים בשיקוף רנטגן במבטים LAO ו-RAO (תמונה 7) ובאלקטרוגרמים של אזור האבלציה (רישום האותות החשמליים המתקבלים ממגע הקתטרים עם רקמת הלב). במגע עם רקמה חיה מתקבל אות חשמלי. היעדר אות מצביע על אזור צלקתי. עם ביצוע האפליקציות של RF, נצפית היעלמות של האותות החשמליים לאורך קו האבלציה.
אם האבלציה מוצלחת, הפרעת הקצב תסתיים תוך כדי הצריבות, אך לא די בכך מאחר שמחקרים מצביעים על אחוז הישנות קטן יותר לאחר השגת חסם דו-כיווני בהולכה החשמלית באזור של קו האבלציה.
כמו כן, יש לוודא שהחסם אינו פונקציונלי (תלוי קצב), ולכן מומלץ לבדוק הולכה בקיצוב לא מהיר ובמחזורי גל שונים. ניתן גם להיעזר במערכת מיפוי אלטקרו-אנטומי לצורך בניית קו צריבה רציף. שימוש במערכות אלו מפחית את כמות הקרינה בזמן הפעולה ומשפר גם את התוצאות. עקרון שיטת האבלציה אינו שונה במהותו במקרה של מטופל בקצב סינוס בעת ביצוע הפעולה. במקרה זה, הצריבה מתבצעת תוך כדי קיצוב בעלייה כדי לעקוב אחר התפתחות של חסם בהולכה ב-CTI. לעתים יש צורך בביצוע צריבות נוספות להשגה תוצאה אופטימלית. קווי אבלציה נוספים נמתחים בין המסתם הטריקוספידלי לסינוס הקורונרי ובין הסינוס הקורונרי לווריד הנבוב התחתון (תמונה 6).
במקרים נדירים יש צורך בצריבה מתוך הפתח של הסינוס הקורונרי, דבר המעלה את הסיכון לסיבוכים, כדוגמת חסם עלייתי-חדרי.
אפליקציות מוצלחות של RF מבוצעות בעזרת גנרטור של אנרגייה זו עם כיוון אוטומטי של העוצמה (עד 50W), לצורך השגת טמפרטורה יציבה של 70%-50?C. הטמפרטורה של הרקמה מנוטרת ע"י חיישן מובנה בתוך הקצה הדיסטלי של אלקטרודה. טמפרטורות גבוהות מאלו עלולות לגרום לאידוי הרקמה, ולהיווצרות של קריש (Coagulum) המכיל בין היתר שאריות רקמה ואשר מכסה את קצה האלקטרודה וגורם לעלייה בתנגודת ולעליית הטמפרטורה. אלה, בסופו של דבר, עלולים לגרום לסיבוכים, כגון פרפורציה או אמבוליזציה.
בשנים האחרונות נכנסו לשימוש קתטרים עם מערכות קירור ע"י תמיסת מלח, סגורות או פתוחות, שמאפשרים השגת טמפרטורות גבוהות יותר ברקמה וכתוצאה מכך, השגת נזק רקמתי גדול יותר, מבלי להסתכן בעליית טמפרטורה באזור של המגע בין הקתטר לרקמה שעלול לגרום להיווצרות קריש עם הסיכונים הכרוכים בכך.
השוואה בין קתטרים רגילים (4 מ"מ) לבין קתטרים בעלי קוטר גדול יותר (10-8 מ"מ) או קתטרים עם מערכת קירור, הראתה תוצאות טובות יותר באחרונים (1). מטה-אנליזה על 7 מחקרים שבה השוו קתטר 8 מ"מ לקתטר מקורר, הוכיחה יעילות זהה (2).
במקרה של קתטרים בעלי קוטר גדול יותר (10-8 מ"מ), יש צורך בעוצמת אנרגייה המגיעה ל-100W כדי להשיג טמפרטורה של 70-50?C. לעומת זאת, בקתטרים עם קירור, עוצמה של 35-40W וטמפרטורה של 50-45?C, מספיקות להשגת טמפרטורה מתאימה ברקמה.
תוצאות של צריבה
בעבודה פרוספקטיבית, שהשוותה טיפול תרופתי לצריבה כטיפול קו ראשון בר"פ, דיווח Natale על יתרון לצריבה בנוגע לשמירה על קצב הסינוס, איכות חיים והפחתה של הישנות ר"פ (3). במחקר על צריבה של ר"פ בחולים מבוגרים (מעל גיל 75) דווח על יעילות ובטיחות של גישה זו (4).
בחולים עם ר"פ לאחר צריבה מוצלחת והיסטוריה של פ"פ, אי ספיקה מיטרלית וירידה בהתכווצות חדר שמאל קיים סיכוי משמעותי להישנות או הופעת פ"פ חדש ((5. על כן, לא מומלץ להתחיל צריבה של ר"פ, אלא אם כן הטיפול התרופתי נכשל קודם לכן.
הצלחה של האבלציה בזמן פעולה היא יותר מ-90%, עם צורך בפעולה חוזרת ב-15%-5% מהחולים (7,6).
סיבוכים
סיבוכים הם נדירים (3.5%-0.4%) וכוללים חסם הולכה עלייתי-חדרי, טמפונדה, שטפי דם במפשעות, אוטם כתוצאה מפגיעה ב-RCA, סיבוכים טרומבו-אמבוליים וטכיקרדיה חדרית (8). פ"פ יכול להופיע בחלק ניכר מהחולים לאחר אבלציה מוצלחת של ר"פ (כ-70% לאחר 5 שנים), אך יש לזכור שבמקרים מסוימים טיפול בר"פ יכול גם לגרום להיעלמות של פ"פ. טיפול בצריבה של ר"פ מומלץ בחולים עם ר"פ טיפוסי שהופיע לאחר התחלת טיפול אנטי-אריתמי (גישה היברידית).
סיכום
הקושי בטיפול פרמקולוגי בר"פ, במקביל לתוצאות המצוינות המושגות בעזרת צריבה עם גלי רדיו (שיעור הישנות וסיבוכים נמוכים), מעמידים גישה פולשנית זו בקו הראשון בטיפול בהפרעת קצב זו. מעבר למקומה בחולים עם ר"פ עמיד לטיפול תרופתי, יש לשקול טיפול בצריבה כאפשרות ראשונה במטופלים שאינם מעוניינים בטיפול אנטי-אריתמי או שרוצים להימנע מהיפוכי קצב חוזרים.
צריבה של פרפור פרוזדורים
רקע
פ"פ היא הפרעת הקצב השכיחה ביותר והאחראית לשליש מהאשפוזים בגין אריתמיה. שכיחותה באוכלוסייה הכללית היא 2%-1%. היא שכיחה יותר אצל גברים. שכיחותה עולה עם הגיל, ובגיל 80 10% סובלים ממנה. קיים קשר בין פ"פ לעלייה בשיעורי התמותה, אירועים תרומבואמבוליים, אי ספיקת לב, אשפוזים, ירידה בדרגה התפקודית, ירידה בתפקוד הקוגניטיבי, פגיעה בתפקוד חדר שמאל וירידה באיכות החיים (9).
פתופיזיולוגיה של פ"פ
במנגנון היווצרות פ"פ משחקים תפקיד שני גורמים עיקריים: הגירוי (Trigger) והגורמים המנציחים את הפרעת הקצב (Substrate).
באופן טיפוסי, פעילות חשמלית שמקורה בוורידים הריאתיים היא "מתנע" לפ"פ, ואילו הרקמה של העלייה השמאלית היא זו שמאפשרת את הנצחת הפרעת הקצב. בחלק מהמקרים, פעילות חשמלית מתמדת של Triggers גורמת ל-Fibrillatory Conduction בתוך העלייה וגירויים אלו מנציחים את הפ"פ (Focal Theory).
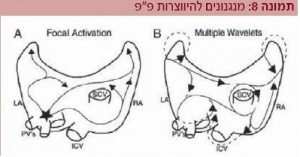
במקרים אחרים, אין הכרח ב-Triggers מכיוון שהנצחת הפרפור מובטחת ע"י מעגלי Reentry רבים המתרחשים בעלייה עצמה (Multiple-Wavelet Hypothesis) (תמונה 8).
האמרה "Atrial Fibrillation Begets Atrial Fibrillation" מקבלת משנה תוקף בשל השינויים המבניים והחשמליים המתרחשים בעליות, ולכן ככל שמטופל יימצא יותר זמן בפ"פ, סיכוייו לחזור לקצב סינוס פחותים.
קיים קשר בין הופעת פ"פ למצבים שונים אחרים, כמו מחלת לב מבנית (מסתמית, איסכמית), פריקרדיטיס, אי ספיקת לב, יתר תריסיות, מחלות ריאה, שתיית אלכוהול ועוד.
נוסף על כך, פ"פ שכיח לאחר ניתוחי לב.
טיפול
הגישה הטיפולית בפ"פ כוללת:
- מניעת סיבוכים תרומבו-מבוליים
- האטה של התגובה החדרית בזמן פרפור (Rate Control) או שמירה על הסינוס (Rhythm Control)
מחקרים אפידמיולוגיים בעבר לא הצביעו על עדיפות של האטת הקצב או של שמירה על הסינוס. זאת בשל תחלואה ותמותה עודפות באסטרטגיה של Rhythm Control. היעדר עדיפות לגישה של שמירה על הסינוס במחקרים שהשוו את שתי הגישות הטיפוליות, Rate vs Rhythm Control, קשור לתכנון המחקרים. אלו נועדו להשוות את שתי הגישות הטיפוליות Rhythm Control ו-Rate Control ולא את החולים שהשיגו קצב סינוס לעומת אלו שלא. ההסבר טמון בין היתר ברעילות של התרופות האנטי-אריתמיות בזרוע של Rhythm Control, כישלון בשמירה על הסינוס ובתחלואה לאחר הפסקת מדללי דם לאחר השגת קצב סינוס.
בתת-אנליזות שהשוו חולים בסינוס וחולים לא בסינוס היה יתרון ל-Rhythm Control, וזהו הרציונל העומד מאחורי הטיפולים הפולשניים בצריבות. בגישה של Rhythm Control קיימות שתי אסטרטגיות עיקריות: טיפול פרמקולוגי וטיפול פולשני בעזרת צריבות.
- הטיפול הפולשני כולל
- התערבות כירורגית (Maze Procedure על סוגיו)
- התערבות מילעורית (צריבה בעזרת צנתור)
סקירה זו תתמקד בגישה הפולשנית בעזרת צנתור (Catheter Ablation).
צריבה של פרפור פרוזדורים
ברוב המקרים פ"פ נוצר בשל פעילות חשמלית לא תקינה שמקורה בוורידי הריאה. פעילות זו הכרחית לאתחול פ"פ בעלייה השמאלית. ורידי הריאה מכילים סעיפי רקמת שריר ((Sleeves שמקורם בעלייה השמאלית, בעלי פוטנציאל דפולריזציה עצמית. אלו עלולים "להתניע" אירועים של פ"פ.
ב-1998 דיווחו לראשונה Haisaguerre וחב', שפ"פ התקפי מופיע לרוב בשל גירוי חשמלי בוורידי הריאה, וניתן לטפל בו באופן מוצלח ע"י צריבה של אותם מוקדים בגלי רדיו (9). מאז, חלה התפתחות אדירה בתחום זה, הן בהבנה של הפתופיזיולוגיה והן בשיטות וטכנולוגיות המיושמות.
בניגוד לגישה הפרמקולוגית, הגישה הפולשנית טומנת בחובה פוטנציאל ריפוי, אך מאחר שהפעולה אינה נטולת סיכון, וטרם הוכחה תועלת במטופלים אתסמיניים, טיפול בצריבה מומלץ בחולים תסמיניים רק לאחר כישלון תרופתי.
קלסיפיקציה של פ"פ
- פ"פ פרוקסיסמלי: חולף עצמונית. יכול להימשך עד שבוע.
- פ"פ פרסיסטנטי: דורש התערבות לצורך הפסקתו (תרופות, היפוך, אבלציה).
- פ"פ פרמננטי: שלא ניתן לסיימו, או שהוחלט להשאיר את החולה בקצב זה.
צריבה של פ"פ פרוקסיסמלי
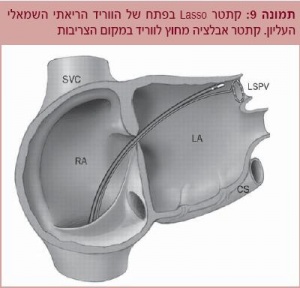
השיטה מתבססת על כך שרוב המקרים של פ"פ (90%<) מקורם בפעילות חשמלית של ורידי הריאה (PVs). בשנים הראשונות היו מוקדי הצריבות ורידי הריאה עצמם, והמטרה הייתה להשתיק את אותם מוקדים. בשיטה זו בוצעה הצריבה בתוך הוורידים, ולכן גרמה כסיבוך, להיצרויות בוורידי הריאה (PV Stenosis). מאוחר יותר הוחלפה השיטה בטכניקה של צריבה מחוץ לוורידי הריאה, באזור של החיבור של רקמת הוורידים הריאתיים עם העלייה השמאלית. מיפוי חשמלי מבוצע בעזרת קתטר עגול עם מספר רב של אלקטרודות (Lasso), והאתרים עם פעילות חשמלית נצרבים בעזרת קתטר צריבה (תמונה 9).
המטרה היא להשיג בידוד מושלם של כל אחד מארבעת ורידי הריאה, כך שלא יוכלו לגרום לפ"פ בעלייה השמאלית (Segmental Ostial PV Isolation - PVI). ניתן גם לבצע בידוד היקפי של שני ורידים מאותו צד, במיוחד אם הם בעלי פתח משותף.
עדיף לצרוב בזמן סינוס או קיצוב עלייתי מכיוון שבזמן פ"פ זיהוי הפוטנציאלים מהוורידים הריאתיים קשה יותר.
קיימים מוקדים (Triggers) מחוץ לוורידים הריאתיים שגם הם עלולים לגרום לפ"פ במיעוט המקרים: וריד נבוב עליון, קריסטה טרמינליס, סינוס קורונרי, עלייה שמאלית ומחיצה בין עלייתית. גישת צריבה שונה היא זו שפותחה ע"י Pappone. בניגוד לשיטה של PVI המונחה ע"י הפעילות החשמלית, שיטתו מתבססת על צריבה מונחה ע"י אנטומיה, באזור מרוחק מהוורידים הריאתיים: Circumferential or Wide Area Antral PVI. הטענה היא ששיטה זו לא מטפלת רק ב-Triggers אלא גם ב-Substrate שבעלייה השמאלית ובשל כך, גורמת לשינויים (Electroanatomical Remodeling) המונעים הופעת פ"פ.
בחלק האחורי של העלייה השמאלית קיימים גם אתרי מטרה אחרים, כגון: מוקדים עם פעילות חשמלית בתדירות
גבוהה, CFAEs (Complex Fractionated Atrial Electrograms), סיבים אוטונומיים (מה-Vagus Nerve) וגנגליונים אוטונומיים שצריבתם עשויה אף היא לתרום להצלחת השיטה.
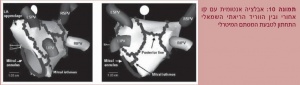
לעתים, מוסיפים קווי צריבה בגג של העלייה השמאלית (Roof Line), ובין הווריד הריאתי השמאלי תחתון לטבעת של המסתם המיטרלי (Mitral Annulus-Left Inferior PV Line) (תמונה 10).
עקרונות הצריבה של פרפור פרוזדורים
- השיטה מחייבת הכנה של החולה
- יש להפסיק טיפול אנטי-אריתמי 5-3 ימים לפני הפעולה.
- ניתן לבצע את הפעולה ב-INR טיפולי, אך לרוב מפסיקים טיפול אנטיקואגולנטי כ-5 ימים לפני הפעולה, ומבצעים חפיפה עם הפרין'הפרין נמוך משקל מולקולרי עד 6-4 שעות או 24-12 שעות לפני ביצוע הצריבה, בהתאמה.
- יש לבצע TEE בסמוך לפעולה לשלילת נוכחות קריש. ניתן לא לבצע בחולים ללא מחלה מבנית ופ"פ פרוקסיסמלי.
- מומלץ ביצוע CT או MRI לצורך הדגמה אופטימלית של ורידי הריאה ואינטגרציה עם מפה אלקטרו-אנטומית הנבנית בזמן הפעולה.
מהלך הפעולה
- ניתן לבצע בהרדמה כללית או בטשטוש (Conscious Sedation).
- מעבר לעלייה השמאלית דרך PFO או לאחר דקירה טרנס-ספטלית. מומלץ שימוש ב-ICE (Intracardiac Echocardiography).
- מתן אנטיקואגולציה מלאה עם הפרין לפני המעבר לצד שמאל או אחריו (גם בחולים בטיפול בקומדין). יש לשאוף לזמן קרישה (ACT) של 400-300 ש'.
- בצריבה אנטומית הכרחית מערכת מיפוי (CARTO, EnSiteNavX/Velocity) ? שילוב עם דימות CT/MR.
- גלי רדיו הם מקור האנרגייה הנפוץ, אך יש מקורות חלופיים (Cryo).
- הקתטרים הנפוצים: 8 מ"מ או קתטר עם מערכת קירור פתוחה. יש גם קתטרים חדשים בצורות גאומטריות שונות המיועדים לבצע צריבות ממספר קטבים בו-זמנית.
- מומלץ להפחית את עוצמת הצריבה באזורים הסמוכים לוושט (קיר אחורי של העלייה).
לאחר הצריבה
- ניתן לחדש קומדין והפרין'הפרין נמוך משקל מולקולרי כ-12-6 שעות לאחר הפעולה. החלטה על הפסקת טיפול אנטיקואגולנטי צריכה להישקל בכובד ראש גם במקרה של צריבה מוצלחת בשל אפשרות של אירועים אתסמיניים של פ"פ. בחולים בסיכון גבוה לא מומלץ כלל להפסיק.
סיבוכים
צריבה של פ"פ היא פעולה מורכבת הדורשת ניסיון ומיומנות.
שיעור הסיבוכים המשמעותיים אינו גבוה, אך אחדים מהם כרוכים בתחלואה משמעותית ואף בתמותה, ביניהם: שבץ (1%>), היצרות של ורידי הריאה (10%-5%), פיסטולה בין העלייה לוושט (1%>) וטמפונדה (6%). נזקים וסקולריים באזור החדרת הצנתרים אינם נדירים, במיוחד לנוכח השימוש במדללי דם בזמן הפעולה ולאחריה.
סיבוך נוסף המופיע בשיעור לא מבוטל, בעיקר לאחר צריבה בגישה האנטומית, הוא הופעת טכיקרדיה עלייתית שמאלית שמקורה ב-Reentry סביב קווי אבלציה. צריבות של טכיקרדיות אלו מצריכות מיפוי אקטיבציה מדויק בעלייה שכבר עברה צריבות רבות, ובשל כך, מהוות אתגר אבחנתי וטיפולי. שיעור התמותה נמוך מ-1% (10).
תוצאות
שיעורי ההצלחה של צריבת פ"פ שונים בסדרות שונות. כעיקרון, שיעור ההצלחה בפ"פ פרוקסיסמלי הוא יותר גבוה (90%-70%) מאשר בפ"פ פרמננטי (60%-50%), אך לעתים נדרשת יותר מפעולה אחת להשגת תוצאות אלו (13-11).
בהשוואה של צריבה עם טיפול תרופתי אנטי-אריתמי, הוכח יתרון לטובת הטיפול הפולשני, למרות שיעורי הישנות מאוחרים לא זניחים (17-14).
שיעור הסיבוכים המשמעותיים במטה-אנליזה שפורסמה ב-2009 היה 4.9%, וכללו בשכיחות יורדת, היצרות של הווריד הריאתי, טמפומדה ושבץ. שיעור התמותה עמד על 0.7% ((14, בדומה לתוצאות האנליזה שביצעו Cappato וחב', אשר כללה 45,115 פעולות שבוצעו ב-32,569 חולים בשנים 1995 עד 2006, עם תמותה מדווחת סביב צריבה של פ"פ בשיעור של 1 ל-1,000 חולים (18).
התוויות
צריבת פ"פ משפרת את איכות החיים של המטופלים, אך טרם הוכח באופן ברור יתרון הישרדותי. לנוכח המורכבות של הפעולה, התחלואה והתמותה הנלוות, מומלץ להפנות לפעולה זו אך ורק מטופלים עם פ"פ פרוקסיסמלי או פרסיסטנטי, תסמיניים ולאחר כישלון תרופתיClass IIa to IIb Indication) ) על פי הקווים המנחים של האיגוד הקרדיולוגי האירופאי) (10). ההמצלות של האיגודים האמריקאיים דומות לאירופאיות, אך במקרה של מועמד אידאלי (מטופל עם פ"פ התקפי, ללא מחלת לב מבנית משמעותית) במרכזים עם ניסיון מוכח, המלצתם היא ברמה של Class Ia Indication(19).
סיכום
צריבת פ"פ היא פעולה מורכבת שעודנה בשלבי התפתחות.
אף שלא מדובר בטיפול הבחירה, היא הולכת ותופסת מקום מכובד בטיפול בפ"פ.
חידושים טכנולוגיים והבנה מעמיקה של מנגנונים פתופיזיולוגיים עשויים לשפר את מעמדה בשנים הבאות, במיוחד, לאור העובדה, שבניגוד לטיפולים האחרים, טמון בה פוטנציאל ריפוי מלא.
ביבליוגרפיה
- Marrouche NF, Schweikert R, Saliba W, et al. Use of different catheter ablation technologies for treatment of typical atrial flutter: acute results and long-term follow-up. Pacing Clin Electrophysiol 2003;26(3):743-746
- Da Costa A, Cucherat M, Pichon N, et al. Comparison of the efficacy of cooled-tip and 8-mm-tip catheters for radiofrequency catheter ablation of the cavotricuspid isthmus: a meta-analysis. Pacing Clin Electrophysiol 2005;28(10):1081-1087
- Natale A, Newby KH, Pisanó E, et al. Prospective randomized comparison of antiarrhythmic therapy versus first-line radiofrequency ablation in patients with atrial flutter. J Am Coll Cardiol 2000;35(7):1898-1904
- Da Costa A, Zarqane-Sliman N, Romeyer-Bouchard C, et al. Safety and efficacy of radiofrequency ablation of common atrial flutter in elderly patients: a single center prospective study. Pacing Clin Electrophysiol 2003;26(8):1729-1734
- Da Costa A, Romeyer-Bouchard C, Zarqane-Sliman N, et al. Impact of first line radiofrequency ablation in patients with lone atrial flutter on the long term risk of subsequent atrial fibrillation. Heart 2005;91(1):97-98
- Feld GK. Radiofrequency ablation for atrial flutter using large-tipelectrode catheters. J Cardiovasc Electrophysiol 2004;15:18-23
- Ventura R, Klemm H, Lutomsky B, et al. Pattern of isthmus recovery using open cooled and solid large-tip catheters for radiofrequency ablation of typical atrial flutter. J Cardiovasc Electrophysiol 2004;15:1126-1130
- Morady F. Catheter Ablation of supraventricular arrhythmias: State of the art. J Cardiovasc Electrophysiol 2004;15:124-139
- Haisaguerre M, Jais P, Shah DC, et al. Spontaneous initiation of atrial fibrillation by ectopic beats originating in the pulmonary veins. NEJM 1998;339:659-666
- Camm AJ, Kirchhof P, Lip GY, et al. Guidelines for the management of atrial fibrillation: the Task Force for the Management of Atrial Fibrillation of the European Society of Cardiology (ESC). Eur Heart J 2010;(19):2369-429. Epub 2010
- Oral H, Knight BP, Tada H, et al, Pulmonary vein isolation for paroxysmal and persistent atrial fibrillation. Circulation 2002;105:1077-1081
- Pappone C, Rosanio S, Oreto G, et al. Circumferential radiofrequency ablation of pulmonary vein ostia. Circulation 2000;102:2619-2628
- Pappone C, Rosanio S, Oreto G, et al. Circumferential radiofrequency ablation of pulmonary vein ostia. Circulation 2000;102:2619-26128
- Calkins H, Reynolds MR, Spector P, et al. Treatment of atrial fibrillation with antiarrhythmic drugs or radiofrequency ablation: twosystematic literature reviews and meta-analyses. Circ Arrhythmia Electrophysiol 2009;2(4):349-61. Epub 2009
- Shah AN, Mittal S, Sichrovsky TC, et al. Long term outcome following successful pulmonary vein isolation: pattern and prediction of very late recurrence. J Cardiovasc Electrophysiol 2008;19:661-667
- Weerasooriya R, Khairy P, Litalien J, et al. Catheter ablation for atrial fibrillation: are results maintained at 5years follow-up? J Am Coll Cardiol 2011;57(2):160-166
- Jais P, Cauchemez B, Macle L, et al. Catheter ablation versus antiarrhythmic drugs for atrial fibrillation: the A4 study. Circulation 2008;118(24):2498-505. Epub 2008
- Cappato R, Calkins H, Chen SA, et al. Prevalence and causes of fatal outcome in catheter ablation of atrial fibrillation. J Am Coll Cardiol 2009;53(19):1798-1803
- Wann LS, Curtis AB, January CT, et al. 2011 ACCF/AHA/HRS focused update on the management of patients with atrial fibrillation (Updating the 2006 Guideline): a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2011;57(2):223-42. Epub 2010
קישורים חיצוניים
- צריבה של רפרוף ופרפור פרוזדורים, מדיקל מדיה


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק