הבדלים בין גרסאות בדף "תסמיני דרכי השתן התחתונות בגברים - ההקשר ההורמונלי - Lower urinary tract symptoms in men - hormonal aspect"
שירה פרנקל (שיחה | תרומות) |
שירה פרנקל (שיחה | תרומות) |
||
| שורה 13: | שורה 13: | ||
|אחראי הערך= | |אחראי הערך= | ||
}} | }} | ||
| − | פתגם צרפתי אומר: "ארבעים הוא גיל הזקנה של הנעורים; חמישים הוא גיל הנעורים של הזקנה", ואכן, מבחינה הורמונלית בשנות הארבעים המוקדמות מתחילה להופיע בגבר ירידה ברמות ה[[אנדרוגנים]] בדם ההיקפי, ויש המצביעים על כך כתחילת [[תהליך ההזדקנות]], ובתחילת שנות החמישים לחייו מתחילות להיראות התוצאות הראשונות של תהליך זה. החל מגיל 40, רמת ה[[טסטוסטרון]] בדם הגבר יורדת בממוצע של 1% כל שנה. ירידה זו היא תוצאה של ירידה במספר תאי ליידיג (Leydig cells) באשכים כמו גם ירידה ברגישותם של תאים אלה להשפעת | + | פתגם צרפתי אומר: "ארבעים הוא גיל הזקנה של הנעורים; חמישים הוא גיל הנעורים של הזקנה", ואכן, מבחינה הורמונלית בשנות הארבעים המוקדמות מתחילה להופיע בגבר ירידה ברמות ה[[אנדרוגנים]] בדם ההיקפי, ויש המצביעים על כך כתחילת [[תהליך ההזדקנות]], ובתחילת שנות החמישים לחייו מתחילות להיראות התוצאות הראשונות של תהליך זה. החל מגיל 40, רמת ה[[טסטוסטרון]] בדם הגבר יורדת בממוצע של 1% כל שנה. ירידה זו היא תוצאה של ירידה במספר תאי ליידיג (Leydig cells) באשכים כמו גם ירידה ברגישותם של תאים אלה להשפעת [[הורמון מחלמן]] LH {{כ}}(Luteinizing Hormone, LH). התוצאה היא [[תת-פעילות בלוטות מין]] (Hypogonadism) ביוכימי בכ-10% מהגברים מתחת לגיל 60, והוא עולה עד יותר מ-35% באוכלוסיית הגברים מעל גיל 60. לירידה בערכי הטסטוסטרון מתלווה עם הגיל עליה ברמת ה[[גלובולין הקושר הורמוני מין]] SHBG {{כ}} (Sex Hormone-Binding Globulin, SHBG). חלבון זה קושר טסטוסטרון חופשי, ועם ירידה בהיענות לטסטוסטרון של אברי המטרה כמו המוח, עצמות, ערמונית ושרירים, מביא לכך שסך כמות הטסטוסטרון הזמינה לפעילות התאים יורדת בצורה משמעותית. ירידה זו ברמות הטסטוסטרון נקשרת להופעת תסמינים רבים חיצוניים ופנימיים בגוף האדם האופייניים לתהליך הזקנה. כמו כן, נמצא גם קשר בין רמות נמוכות של טסטוסטרון והופעת [[מחלות לב]] ו[[מחלות כלי דם|כלי דם]], [[הפרעה בשומני הדם]] (Dyslipidemia), [[טרשת עורקים]] ו[[סוכרת סוג 2]], כך שחוקרים רבים סבורים שרמות נמוכות של טסטוסטרון, קרי [[תסמונת של חסר בטסטוסטרון|תת-פעילות בלוטות מין בהופעה בגיל המבוגר]] {{כ}} (Late Onset Hypogonadism, LOH) או בשמה האחר, ה[[תסמונת של חסר בטסטוסטרון]] {{כ}} (Testosterone Deficiency Syndrome, TDS) הוא חלק מהתסמינים המאפיינים את [[התסמונת המטבולית]] ואף מהווה גורם סיכון להופעתה. |
החל מגיל חמישים ההיארעות של הגדלה {{כ}} (Benign Prostatic Enlargement, BPE) ו/או [[הגדלה שפירה של הערמונית|שגשוג שפיר של הערמונית]] {{כ}} (Benign Prostatic Hyperplasia, BPH) הולכת ועולה עם הגיל. הגדלת הערמונית יכולה להוביל ללחץ על השופכה, צוואר ובסיס כיס השתן ולגרום למערך של תסמינים הכוללים היסוס במתן שתן, זרם שתן חלש ומקוטע, טפטוף ארוך, תכיפות בעיקר בלילה, דחיפות ואף לאי נקיטת שתן. כך, שנים רבות קישרו את התסמינים הללו אך ורק לתוצאת הלחץ של ערמונית הולכת וגדלה על השופכה והאבחנה של הגדלת ערמונית מצאה לה מקום של כבוד במילון הרפואי. אלא ש[[תסמינים בדרכי שתן תחתונות]] {{כ}} (Lower Urinary Tract Symptoms, LUTS) יכולים להופיע גם ללא הגדלה משמעותית בנפח הערמונית. רק ב-50% מהחולים עם הוכחה היסטולוגית לשגשוג שפיר של הערמונית קיימת הגדלה של הערמונית. בנוסף על כך, הצטברו עבודות אפידמיולוגיות שהראו כי לאחר גיל 60 ההיארעות של תסמינים בדרכי שתן תחתונות מופיעה באופן שווה בגברים ובנשים כאחת. בעבודות מעבדה על ארנבים זכרים מסורסים נמצאה ירידה בהיענות של כיס השתן והופעה של כיס שתן בפעילות יתר, שחלפה לאחר הזרקת טסטוסטרון. מכאן התפתחה ההשערה, שהופעה של תסמיני דרכי שתן תחתונות בגיל המבוגר קשורה לא רק להגדלת נפח הערמונית, אלא גם לתופעות של שינויים הורמונליים המתרחשים בתהליך הזקנה. | החל מגיל חמישים ההיארעות של הגדלה {{כ}} (Benign Prostatic Enlargement, BPE) ו/או [[הגדלה שפירה של הערמונית|שגשוג שפיר של הערמונית]] {{כ}} (Benign Prostatic Hyperplasia, BPH) הולכת ועולה עם הגיל. הגדלת הערמונית יכולה להוביל ללחץ על השופכה, צוואר ובסיס כיס השתן ולגרום למערך של תסמינים הכוללים היסוס במתן שתן, זרם שתן חלש ומקוטע, טפטוף ארוך, תכיפות בעיקר בלילה, דחיפות ואף לאי נקיטת שתן. כך, שנים רבות קישרו את התסמינים הללו אך ורק לתוצאת הלחץ של ערמונית הולכת וגדלה על השופכה והאבחנה של הגדלת ערמונית מצאה לה מקום של כבוד במילון הרפואי. אלא ש[[תסמינים בדרכי שתן תחתונות]] {{כ}} (Lower Urinary Tract Symptoms, LUTS) יכולים להופיע גם ללא הגדלה משמעותית בנפח הערמונית. רק ב-50% מהחולים עם הוכחה היסטולוגית לשגשוג שפיר של הערמונית קיימת הגדלה של הערמונית. בנוסף על כך, הצטברו עבודות אפידמיולוגיות שהראו כי לאחר גיל 60 ההיארעות של תסמינים בדרכי שתן תחתונות מופיעה באופן שווה בגברים ובנשים כאחת. בעבודות מעבדה על ארנבים זכרים מסורסים נמצאה ירידה בהיענות של כיס השתן והופעה של כיס שתן בפעילות יתר, שחלפה לאחר הזרקת טסטוסטרון. מכאן התפתחה ההשערה, שהופעה של תסמיני דרכי שתן תחתונות בגיל המבוגר קשורה לא רק להגדלת נפח הערמונית, אלא גם לתופעות של שינויים הורמונליים המתרחשים בתהליך הזקנה. | ||
גרסה מ־13:55, 11 ביוני 2014
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| תסמיני דרכי השתן התחתונות בגברים - ההקשר ההורמונלי | ||
|---|---|---|
| Lower urinary tract symptoms in men - hormonal aspect | ||
| יוצר הערך | ד"ר משה שלו 
|
|
פתגם צרפתי אומר: "ארבעים הוא גיל הזקנה של הנעורים; חמישים הוא גיל הנעורים של הזקנה", ואכן, מבחינה הורמונלית בשנות הארבעים המוקדמות מתחילה להופיע בגבר ירידה ברמות האנדרוגנים בדם ההיקפי, ויש המצביעים על כך כתחילת תהליך ההזדקנות, ובתחילת שנות החמישים לחייו מתחילות להיראות התוצאות הראשונות של תהליך זה. החל מגיל 40, רמת הטסטוסטרון בדם הגבר יורדת בממוצע של 1% כל שנה. ירידה זו היא תוצאה של ירידה במספר תאי ליידיג (Leydig cells) באשכים כמו גם ירידה ברגישותם של תאים אלה להשפעת הורמון מחלמן LH (Luteinizing Hormone, LH). התוצאה היא תת-פעילות בלוטות מין (Hypogonadism) ביוכימי בכ-10% מהגברים מתחת לגיל 60, והוא עולה עד יותר מ-35% באוכלוסיית הגברים מעל גיל 60. לירידה בערכי הטסטוסטרון מתלווה עם הגיל עליה ברמת הגלובולין הקושר הורמוני מין SHBG (Sex Hormone-Binding Globulin, SHBG). חלבון זה קושר טסטוסטרון חופשי, ועם ירידה בהיענות לטסטוסטרון של אברי המטרה כמו המוח, עצמות, ערמונית ושרירים, מביא לכך שסך כמות הטסטוסטרון הזמינה לפעילות התאים יורדת בצורה משמעותית. ירידה זו ברמות הטסטוסטרון נקשרת להופעת תסמינים רבים חיצוניים ופנימיים בגוף האדם האופייניים לתהליך הזקנה. כמו כן, נמצא גם קשר בין רמות נמוכות של טסטוסטרון והופעת מחלות לב וכלי דם, הפרעה בשומני הדם (Dyslipidemia), טרשת עורקים וסוכרת סוג 2, כך שחוקרים רבים סבורים שרמות נמוכות של טסטוסטרון, קרי תת-פעילות בלוטות מין בהופעה בגיל המבוגר (Late Onset Hypogonadism, LOH) או בשמה האחר, התסמונת של חסר בטסטוסטרון (Testosterone Deficiency Syndrome, TDS) הוא חלק מהתסמינים המאפיינים את התסמונת המטבולית ואף מהווה גורם סיכון להופעתה.
החל מגיל חמישים ההיארעות של הגדלה (Benign Prostatic Enlargement, BPE) ו/או שגשוג שפיר של הערמונית (Benign Prostatic Hyperplasia, BPH) הולכת ועולה עם הגיל. הגדלת הערמונית יכולה להוביל ללחץ על השופכה, צוואר ובסיס כיס השתן ולגרום למערך של תסמינים הכוללים היסוס במתן שתן, זרם שתן חלש ומקוטע, טפטוף ארוך, תכיפות בעיקר בלילה, דחיפות ואף לאי נקיטת שתן. כך, שנים רבות קישרו את התסמינים הללו אך ורק לתוצאת הלחץ של ערמונית הולכת וגדלה על השופכה והאבחנה של הגדלת ערמונית מצאה לה מקום של כבוד במילון הרפואי. אלא שתסמינים בדרכי שתן תחתונות (Lower Urinary Tract Symptoms, LUTS) יכולים להופיע גם ללא הגדלה משמעותית בנפח הערמונית. רק ב-50% מהחולים עם הוכחה היסטולוגית לשגשוג שפיר של הערמונית קיימת הגדלה של הערמונית. בנוסף על כך, הצטברו עבודות אפידמיולוגיות שהראו כי לאחר גיל 60 ההיארעות של תסמינים בדרכי שתן תחתונות מופיעה באופן שווה בגברים ובנשים כאחת. בעבודות מעבדה על ארנבים זכרים מסורסים נמצאה ירידה בהיענות של כיס השתן והופעה של כיס שתן בפעילות יתר, שחלפה לאחר הזרקת טסטוסטרון. מכאן התפתחה ההשערה, שהופעה של תסמיני דרכי שתן תחתונות בגיל המבוגר קשורה לא רק להגדלת נפח הערמונית, אלא גם לתופעות של שינויים הורמונליים המתרחשים בתהליך הזקנה.
הורמונים אנדרוגניים, הגדלה שפירה של הערמונית ותסמינים של דרכי שתן תחתונות
האנדרוגן הפעיל ביותר בערמונית הוא ה-5 אלפא דהידרוטסטוסטרון (Dihydrotestosterone, DHT) שנוצר בערמונית על ידי פעילות של האנזים 5 אלפא רדוקטז על הטסטוסטרון. טסטוסטרון גם עובר ארומטיזציה והופך לאסטרוגן בערמונית, בכבד, בעור וברקמת השומן. אסטרוגן ו-DHT לעומת זאת, אינם יכולים להפוך לטסטוסטרון. ריכוז ה-DHT בערמונית גדול פי 5 מהטסטוסטרון (5 נ"ג/גר' משקל רטוב של רקמה).
הערמונית מגיבה לשינויים ההורמונליים המתרחשים במהלך חייו של הגבר. בגיל שבין 10 ל-20 שנים, תחת השפעה של רמות טסטוסטרון הולכות ועולות עוברת הערמונית תהליך של גדילה מואצת. תחת המשך השפעה של רמות גבוהות של טסטוסטרון, לאחר גיל 20, שומרת הערמונית על נפח קבוע תוך כדי איזון בין התפתחות של תאים חדשים ואפופטוזה (Apoptosis). החל מגיל 50 מתחילה שוב הערמונית במקרים רבים לעלות בנפחה ומתפתח שגשוג שפיר של הערמונית ובמקרים רבים גם (אחד מכל 6 גברים) ממאירות. ההתפתחות הזו של הערמונית מתרחשת בד-בבד עם ירידה איטית והדרגתית ברמות האנדרוגנים ועלייה יחסית ברמות האסטרוגנים בדם ההיקפי בתהליך ההזדקנות. אחת התיאוריות המסבירה את התופעה, גורסת כי עם ירידה ברמות האנדרוגנים נוצר בערמונית "רעב" להורמונים אלה. כדי לשמור על מנות מתאימות של אנדרוגנים מתבצעת פעילות גנטית מואצת לבניית חלבונים לצורך העלאת ריכוזי הקולטנים האנדרוגניים ברקמת הערמונית. תהליכים אלה יכולים להביא לחוסר יציבות גנטית, להפר את האיזון שבין התפתחות תאים חדשה ואפופטוזה, ולהביא להיפרטרופיה (BPE) והיפרפלזיה בערמונית (BPH) ולהתפתחות של ממאירות. בעבודה על מודל של כלבים נמצא שפעילות סינרגיסטית של אסטרוגן ו-DHT גורמת להיפרפלזיה והגדלת הערמונית בקצב ובממדים גדולים יותר מאשר פעילות של אנדרוגנים בלבד וכן גורמת להאטה ניכרת של האפופטוזיס של תאים בערמונית. האסטרוגנים על ידי האצת הפעילות של הארומטזות מביאה גם לעלייה בריכוז הקולטנים האנדרוגניים. בגבר המבוגר, עם ירידה ברמות הטסטוסטרון רמות האסטרוגנים נשארות יחסית קבועות או עולות כך שייתכן שבהשפעה הגוברת של האסטרוגנים עולה ריכוז הקולטנים האנדרוגנים ופעילות הארומטזות בערמונית שיכולה להביא להיפרטרופיה והיפרפלזיה של הבלוטה. נשאלת השאלה, האם ניתן יהיה למנוע את ההגדלה השפירה של הערמונית בגבר המבוגר על ידי החזרת היחס בין טסטוסטרון ואסטרוגן ליחס שהיה קיים בשנות השלושים לחייו? לכך אין עדיין תשובה בידנו. כדי לסבך יותר את הנושא הראו Walsh ו-Bartsch בעבודותיהם רמות דומות של DHT בערמוניות של גברים ללא BPH ובגברים מבוגרים עם BPH, וכך גם לא היה הבדל ברמות של פרוגסטרון, אסטריול, אסטרון ואסטרדיול בין שתי הקבוצות.
עבודות אפידמיולוגיות מאוחרות יותר הראו שבו בזמן שרמות טסטוסטרון יורדות בתהליך ההזדקנות, רמות ה-DHT בערמונית נשארות יחסית קבועות ואף מעט גבוהות יותר בערמוניות עם BPH. כך הראו שטיפול בתרופות החוסמות את פעילות האנזים 5 אלפא רדוקטז יכול להוריד את נפח הערמונית ולהקל את התסמינים של LUTS וזאת מבלי להשפיע על רמות הטסטוסטרון בדם הפריפרי. נוסף על כך, לא נמצא יחס ישיר בין רמות טסטוסטרון לנפח הערמונית, מה גם שטיפול משלים בטסטוסטרון לחולים עם LOH לא גרם להגדלת נפח הערמונית. המסקנה המתבקשת היא, אם כן, שהגדלה שפירה של הערמונית עם או בלי הופעת LUTS תלויה ברמות ה-DHT רק באופן חלקי ויתכן שקיימת עלייה עם הגיל בפעילות הארומטזות בערמונית הגורמת גם לעלייה יחסית ברמות האסטרוגן, ופעילות סינרגיסטית זו מביאה להגדלה של הערמונית ו-BPH. אולם, כמו שכבר שנינו, הופעת LUTS בגיל המבוגר אינה תלויה רק בגודל הערמונית ואפילו לא בעצם הימצאותה של הבלוטה.
באופן טבעי ומסורתי רוב המחקר על חסר בהורמוני מין בגבר המבוגר התמקד סביב התפקוד של אברי המין והרבייה ולא התמקד סביב הקשר של הורמונים אלה לתפקוד מערכת השתן. ידוע כי ל-DHT יש תפקיד חשוב בהתפתחות השופכה וצוואר כיס השתן בתקופה העוברית, ונשאלת השאלה אם גם בגבר המבוגר יש לטסטוסטרון תפקיד כלשהו בתפקוד מערכת השתן. קיימות מספר עבודות מעוררות עניין בנושא זה, בעיקר על חיות מעבדה. בחולדות נמצאו קולטנים אנדרוגניים ואסטרוגניים באפיתל המעבר המצפה את דרכי השתן כמו גם בדטרוזור, בשריר המשורטט של השופכה הקריבנית ובגנגליונים האוטונומיים המעצבבים את הערמונית. גם העצבים האוטונומיים המוטוריים שמקורם בגנגליונים שבאגן, נתגלו כרגישים ביותר להורמונים האנדרוגניים והאסטרוגניים. סירוס גרם לירידה בריכוז הקולטנים האלפא אדרנרגיים בבסיס כיס השתן, ואילו הזרקת טסטוסטרון העלתה את ריכוז הקולטנים הכולינרגיים מוסקריניים. כך גם בשריר החלק שבמערכת השתן התחתונה: סירוס הביא לירידה בפעילות של הקולטנים אלפא 1 אדרנרגיים וכולינרגיים מוסקריניים והזרקת טסטוסטרון הביאה לעלייה בריכוז של קולטנים אלה. סירוס גם גרם לירידה ביכולת ההרפיה על ידי השריה חשמלית של שריר חלק מהשופכה הפרוסטטית קרוב לוודאי כביטוי לחוסר יכולת של השריר להגיב לחומרי הרפיה. כמו כן, גרם הסירוס לשיבושים בפעילות אנזימים מיטוכונדריאליים בדרכי שתן תחתונות בארנבים.
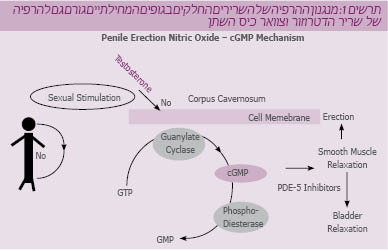
הרבה עבודות נכתבו על מקומם של נוירוטרנסמיטורים לא אדרנרגיים ולא כולינרגיים כגורם ל- LUTS בגברים ונשים מעל גיל 50. החשוב שבהם הוא ה-(Nitric Oxide) NO אשר יש לו השפעה מרפה על איברים במערכת האורוגניטלית. NO אחראי לתהליך הזקפה, אך גם גורם להרפיה של צוואר כיס השתן והשופכה. כ-96%-72% מהנוירונים בדופנות כיס השתן (בשריר הדטרוזור) ובשופכה בבני אדם מכילים את האנזים Nitric Oxide Synthase. פעילותו של אנזים זה תלויה בהימצאות רמות פיזיולוגיות תקינות של טסטוסטרון. הזרקה של טסטוסטרון בעכברים עם חסר ב-NO Synthase גרם לירידה בתכיפות ההשתנה. האנזים פוספודיאסטרז Phosphodiesterase 5) PDE5) מהווה שליח שניוני ל-NO ותפקידו בתהליך הזקפה ידוע, אך לאחרונה אף הוכח שיש לו תפקיד בוויסות הטונוס של השריר החלק בכיס השתן (תרשים 1). תרופות החוסמות PDE5 מסוגלות להקל את התסמינים של כיס שתן רגיז ו-LUTS. בחיות מעבדה גרם סירוס לירידה בהתבטאות הגנטית של PDE5, ותוספת של טסטוסטרון הביא לחידוש ההתבטאות הגנטית של אנזים זה. גם בבני אדם קיים רמז להקשר זה, שכן ידוע שאחוז ניכר מהחולים עם LUTS ו-BPH סובלים גם מאין אונות ו-LOH. המסקנה מעבודות אלה היא שהורמונים אנדרוגניים אחראיים גם לפעילות התקינה של מערכת השתן התחתונה. אם כך, לירידה ברמות הטסטוסטרון בגבר המבוגר יכולה להיות השפעה בהופעת LUTS בקבוצת גיל זו. עבודות אפידמיולוגיות הראו שכ-20% מהגברים מעל 50 עם LUTS הם גם היפוגונדליים (LOH). בעבודה על 30 חולים עם LUTS ו-LOH שטופלו בטסטוסטרון פומי או בזריקות, נמצא שיפור בתסמינים כפי שנמדדו על יד טבלאות של IPSS (International Prostate Symptom Score) וכן היה שיפור בתסמינים של LOH שנמדדו על פי טבלאות של AMS (Aging Male Symptoms) וזאת בד-בבד עם עלייה ברמות הטסטוסטרון בדם פריפרי.
LUTS, טסטוסטרון והתסמונת המטבולית
התסמונת המטבולית היא מערכת של תסמינים המופיעים בגבר המבוגר וכוללים היפרגליקמיה או סוכרת מסוג 2, רמות מוגברות של שומנים בדם, יתר לחץ דם והשמנה בטנית. ירידה ברמות הטסטוסטרון גם היא נקשרת להופעת תסמינים רבים האופייניים לתהליך הזקנה, כמו ירידה במסת השריר והכוח הגס, ירידה בתשעורת ובעובי העור, כאבי גב ואוסטאופורוזיס, הגדלת השדיים, שינויים במצבי הרוח, הופעת גלי חום והזעות לילה, נטייה לדיכאון וירידה בחיוניות, ירידה בתשוקה ובתפקוד המיני והופעת תכיפות ודחיפות במתן שתן (LUTS). נוסף על כך, נמצא גם קשר בין רמות נמוכות של טסטוסטרון להופעת תסמינים אופייניים לתסמונת המטבולית כמו מחלות לב וכלי דם, דיסליפידמיה, טרשת עורקים, השמנה בטנית וסוכרת מסוג 2, כך שחוקרים רבים סבורים שרמות נמוכות של טסטוסטרון, הן חלק מהתסמינים המאפיינים את התסמונת המטבולית ואולי אף גורם להופעתה.
בעבודה על עכברים זכרים שלא היו מסוגלים לייצר טסטוסטרון, וקיבלו תזונה עתירת שומן, נמצאו השמנת יתר ותהליך מוגבר של טרשת עורקים משמעותי בהשוואה לעכברים עם רמות טסטוסטרון תקינות שקיבלו את אותה תזונה. בעבודה אחרת, גברים עם LOH היו עם השמנה בטנית משמעותית יותר מאשר גברים עם רמות טסטוסטרון תקינות באותה קבוצת גיל.
חוקרים מבריטניה הראו בעבודה כפולת-סמיות על 24 חולים עם LOH וסוכרת מסוג 2 שקיבלו טיפול בטסטוסטרון, שיפור משמעותי בשליטה על רמות הסוכר בדם, בעמידות לאינסולין, בהיקף המותניים, ברמות הכולסטרול בדם הפריפרי וירידה משמעותית ברמות הלפטין. כך גם עבודות רבות הצליחו להראות קשר בין רמות טסטוסטרון ויתר לחץ דם היפרכולסטרולמיה והיפרליפידמיה.
בעבודה שמטרתה הייתה לברר את הקשר בין LUTS והתסמונת המטבולית נבדקו 1,899 גברים בגילים 30 עד 79, ונמצא שבגברים עם תסמינים של LUTS בינוניים עד קשים שכללו חוסר התרוקנות של כיס השתן, תכיפות ונוקטוריה היה הסיכוי הגדול ביותר למצוא את הסימנים האופייניים לתסמונת המטבולית. ההקשר היה חזק יותר בגברים מתחת לגיל 60. מסקנת החוקרים בעבודה זו הייתה ש-LUTS והתסמונת המטבולית הם סימנים משותפים להפרעה כרונית שמקורה מחוץ לדרכי השתן. החוקרים אף ציינו שהחולים עם תסמונת מטבולית גם התלוננו באופן משמעותי יותר על הפרעות בתפקוד המיני.
הגורם המשותף ל-LUTS, הפרעות בתפקוד המיני והתסמונת המטבולית, כפי שעולה אינטואיטיבית מעבודות אלה, הוא החסר באנדרוגנים בגבר המבוגר עם כי עדיין יש מקום לעבודות נוספות כדי להוכיח שבסיס כל ההפרעות הללו הוא התהליך של ירידה בטסטוסטרון המופיעה בתהליך ההזדקנות.
סיכום
בחקר תהליך הזקנה בגברים הולך ומתברר שבבסיס הרבה מתהליכי התחלואה האופייניים המופיעים בגבר המבוגר, כמו LUTS, השמנה בטנית, התסמונת המטבולית והפרעות בתפקוד המיני, נמצא מכנה משותף ולמעשה מדובר בתהליכים הקשורים זה בזה. אותו בסיס משותף הוא רמות של טסטוסטרון נמוכות, תופעה שמתפתחת החל מגיל 40 ונותנת את ביטוייה הקליניים בגבר המזדקן. היגיע כעת הזמן לבדוק בעבודה נרחבת ומבוקרת אם טיפול משלים בטסטוסטרון יכול למנוע את התסמינים הללו או לעזור בטיפול בהם לאחר הופעתם.
דגלים אדומים
ביבליוגרפיה
- Veltri R, Rodriguez R. Molecular biology, endocrinology, and physiology of the prostate and seminal vesicles. In. Campbell – Walsh Urology 9th ed
2007;2677-2726
- Roehrborn CG, McConnell JD. Benign prostatic hyperplasia: etiology, pathophysiology, epidemiology, and natural history. In: Campbell – Walsh Urology 9th ed 2007;2727-2765
- Krieg M, et al. Effect of aging on endogenous level of 5 alpha-dihydrotestosterone, testosterone, estradiol, and estrone in epithelium and stroma of normal and hyperplastic human prostate. J Clin Endocrinol Metab 1993;77:375–381
- Brendler CB, et al. Spontaneous benign prostatic hyperplasia in the beagle. Age-associated changes in serum hormone levels, and the morphology and secretory function of the canine prostate. J Clin Invest 1983;1114
- Walsh P C, et al. Tissue content of dihydrotestosterone in human prostatic hyperplasia is not supranormal. J Clin Invest 1983;1772
- Barrack ER, et al. Subcellular distribution of androgen receptors in human normal, benign hyperplastic, and malignant prostatic tissues: characterization of nuclear salt-resistant receptors. Cancer Res 1983;1107–1116
- Bartsch G. Correlation of biochemical (receptors, endogenous tissue hormones) and quantitative morphologic (stereologic) findings in normal and hyperplastic human prostates. J Urol 1987;559-564
- Bartsch G, et al. Light-microscopic stereologic analysis of spontaneous and steroid-induced canine prostatic hyperplasia. J Urol 1987;552-558
- Schatzl G, et al. Endocrine patterns in patients with benign and malignant prostatic diseases. Prostate 2000;p219-224
- Hajjar RR, et al. Outcomes of long- term Testosterone replacement in older hypogonadal males: a retrospective analysis. J clin Endocrinol Metab 1997;3793-3796
- Marks LS, et al. Effect of Testosterone replacement therapy on prostate tissue in men with late-onset hypogonadism: a randomized controlled trial. JAMA 2006;2351-2361
- Pradidarcheep W. Lower urinary tract symptoms and its potential relation with late-onset hypogonadism. The Aging Male 2008;51–55
- Kalichenko S, et al. Beneficial effects of Testosterone administration on symptoms of the lower urinary tract in men with late-onset hypogonadism: A pilot study. The Aging Male 2008;57-61
- Agledahl I, et al. Low serum Testosterone in men is inversely associated with non-fasting serum triglycerides: the Tromso study. Nutr Metab Cardiovasc Dis 2008;256–262
- Shabsigh R, et al. The triad of erectile dysfunction, hypogonadism and the metabolic syndrome. Int J Clin Pract 2008;791–798
- Kupelian V, et al. Association of lower urinary tract symptoms and the metabolic syndrome: results from the Boston Area Community Health Survey. J Urol 2009;616–624
קישורים חיצוניים
המידע שבדף זה נכתב על ידי ד"ר משה שלו - המחלקה לאורולוגיה, מרכז רפואי מאיר, כפר סבא; יו"ר החברה לחקר וטיפול בגבר המבוגר, ההסתדרות הרפואית בישראל; בית הספר לרפואה ע"ש סאקלר, אוניברסיטת תל אביב


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק