פפסין - Pepsin
הופניתם מהדף Pepsin לדף הנוכחי.
| מדריך בדיקות מעבדה | |
| פפסין | |
|---|---|
| Pepsin | |
מבנה מרחבי של החלבון פפסין
| |
| מעבדה | כימיה בדם ובנוזלי גוף |
| תחום | אנזים פרוטאוליטי |
| טווח ערכים תקין | פחות מ-12.5 ננוגרם/מ"ל -שלילי; 12.5-100 ננוגרם/מ"ל - חלש עד חיובי באופן מתון; מעל 10 ננוגרם/מ"ל - חיובי חזק. |
| יוצר הערך | פרופ' בן-עמי סלע |
מטרת הבדיקה
בחינת העיכול של חלבונים במערכת עיכול.
כללי
פפסין (Pepsin מיוונית עתיקה πέψις - עיכול) מאבד במהירות את יציבותו ב-pH בסיסי (מעל 6.0) בהיותו לא יציב בתנאים בסיסיים. דגימות עם pH מעל 6.0 הן בעלות תוצאת פפסין מופחתת. ריכוז חלבון בדגימה הגבוה (מעל 2 מיליגרם/מ"ל, או גבוה מכך), עלול להפריע למדידת פעילות פפסין, ולקבלת תוצאת ריכוז פפסין שלילית. אם מתקבלת תוצאה גבולית של פפסין בדגימה עם ריכוז גבוה של חלבון, יש לחזור על הבדיקה, על ידי מיהול של ריכוז החלבון בדגימה לרמה הנמוכה מ-2 מיליגרם/מ"ל. תוצאה שלילית אינה שוללת אירוע של מיקרו-אספירציה. הגילוי של פפסין בדרכי אוויר נקבעת במהלך האספירציה, דרגת האספירציה ורמת ה-pH בנוזל האספירציה. תוצאת הבדיקה צריכה להיבחן ביחד עם הממצאים הקליניים ותוצאות מעבדה אחרות.
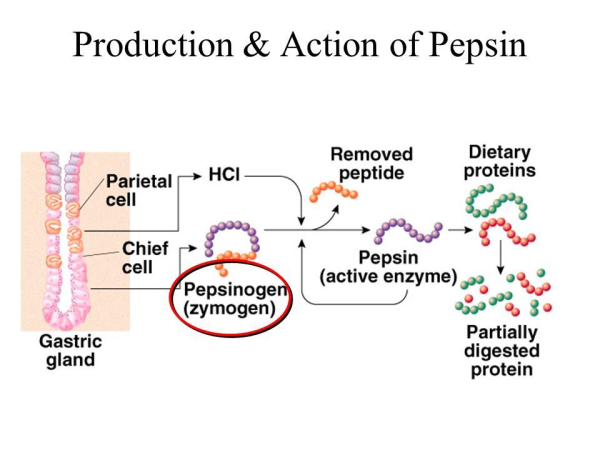
פפסין הוא אנדו-פפטידאז המבקע חלבונים לפפטידים קטנים ולחומצות אמינו. הוא אחד האנזימים מעכלי המזון במערכת העיכול של האדם ושל בעלי חיים רבים, בהם הוא מסייע בעיכול חלבונים במזון. פפסין נחשב ל-aspartic protease המשתמש בחומצה אספרטית קטליטית באתר הפעיל שלו (Fujinaga וחב' ב-Protein Sci משנת 1995). פפסין הוא אחד משלושת האנדו-פפטידזות העיקריות במערכת העיכול של האדם, כאשר השתיים האחרות הן טריפסין וכימוטריפסין. ישנם גם אקסו-פפטידזות המרחיקות חומצות אמינו אינדיבידואליות בשני הקצוות של של חלבונים (קרבוקסי-פפטידזות המיוצרות על ידי הפנקריאס, ואמינו-פפטידזות המופרשות על ידי המעי הדק). במהלך תהליך העיכול, אנזימים אלה משתפים פעולה לפירוק חלבונים לפפטידים ולחומצות אמינו, שיכולים להיספג בקלות על ידי המעי הדק (Hamuro וחב' ב-Rapid Commun Spectrometry משנת 2008). ספציפיות הביקוע של פפסין רחבה, כאשר מספר חומצות אמינו כגון טירוזין, פנילאלנין וטריפטופן מגבירים את הסתברות הביקוע. פפסינוגן, שהוא הזימוגן של פפסין (דהיינו הקדם-אנזים שלו) מופרש על ידי תאי chief בדופן הקיבה ועל ידי ערבוב עם HCl במיץ הקיבה משופעל פפסינוגן להפוך לפפסין. לפפסינוגן יש 44 חומצות אמינו יותר מאשר לאנזים הפעיל. פפסין מבקע את 44 חומצות האמינו מפפסינוגן ליצירת יותר פפסין. תאי chief הם תאים בדופן הקיבה המפרישים פפסינוגן. הם אחראיים על פירוק חלבונים בקיבה, כאשר הפפסינוגן מופרש כמולקולת קודמן. תאי chief מפרישים גם חומצה מלחית ותפקידם הוא לשמור על סביבה חומצית נמוכה בקיבה, מה שמגביר את פעילות האנזים המפרק חלבונים. חומצת המלח HCl מופרשת מהתאים הפרייטאליים בשולי הקיבה. ההורמון gastrin והעצב התועה (vagus) מגבירים את הפרשת פפסינוגן ו-HCl משולי הקיבה בעת עיכול המזון. פפסינוגן מתחלק ל-5 תת-קבוצות המבוססות על המבנה הראשוני שלהן:
- פפסינוגן A (הקרוי גם פפסינוגן I)
- פפסינוגן B,
- פפסינוגן C (הידוע גם כפפסינוגן II ו-progastricsin
- פרוכימוזין (הידוע גם כ-prorennin
- פפסינוגן F (הידוע גם כ-pregnancy-associated glycoprotein (לageyama ב-Cell Mol Life Sci משנת 2002)
היסטוריה
פפסין הוא אחד האנזימים הראשונים שהתגלו על ידי הפיזיולוג הגרמני Theodor Schwann בשנת 1836 (Florkin ב-Revue Médicale de Liège משנת 1957,ו-Asimov ב-Westport, Conn: Greenwood Press משנת 1980). בשנת 1929, פפסין הפך לאחד האנזימים הראשונים להיות מגובש, כאשר הביוכימאי ג'ון הווארד נורתרופ גיבש אותו לאחר דיאליזה, פילטרציה וקירור, ופרסם את גיבוש האמור ב-Science באותה שנה. פפסין זוהה כחומר החומצי שהיה מסוגל להתמיר סוגי מזון חנקני לחומר במים (Fruton ב-Quarterly Rev Biol משנת 2002).
פעילות ויציבות
פפסין פעיל ביותר בסביבות חומציות ב-pH בין 1.5 ל-2.5 (Piper ו-Fenton ב-Gut משנת 1965). בהתאם, האתר הראשוני לסינתזה ולפעילות של פפסין נמצא בקיבה. באדם, הריכוז של פפסין בקיבה הוא 0.1-1.0 מיליגרם/מ"ל (Zhu וחב' ב-J Med Microbiol . s006 ו-Brodkorb וחב' ב-Nature Protocol משנת 2019). פפסין אינו פעיל ב-pH של 6.5 ומעלה, עם זאת, פפסין אינו עובר דה-נטורציה מלאה או עובר אינאקטיבציה בלתי הפיכה עד pH של 8.0 (לJohnston וחב' ב-The Laryngoscope משנת 2007). לפיכך, פפסין בתמיסות עד pH 8.0, יכול לעבור רה-אקטיבציה על ידי החמצת התמיסות. היציבות של פפסין ב-pH גבוה היא בעלת אימפליקציות משמעותיות על מחלות המיוחסות ל-laryngopharyngeal reflux (לJohnston וחב' ב-Ann Otol, Rhinol Laryngol משנת 2006). פפסין נותר בגרון לאחר אירוע של רפלוקס של הקיבה. ב-pH הממוצע של ה-laryngopharynx שהוא 6.8, פפסין היה צריך להיות בלתי פעיל, אך יכול לעבור רה-אקטיבציה לאחר אירועי רפלוקס חומציים. פפסין הוא בעל ספציפיות ביקוע רחבה, והוא יעכל עד 20% מהקשרים האמידיים (Cox וחב' ב־Leninger principles biochem משנת 2008). שיירים בעמדות P1 ו-'P1, חשובים יותר בקביעת הביקוע של מצעים (Schechter ו-Berger ב-Biochem Biophys Res Commun משנת 1968). כללית, חומצות אמינו הידרופוביות בעמדות P1 ו-'P1, מגדילות את הסתברות הביקוע. פנילאלנין, לאוצין ומתיונין בעמדת P1, ופנילאלנין, טריפטופן וטירוזין בעמדת 'P1, הן בעלות הסבירות הגבוהה ביותר של ביקוע. לעומת זאת, ביקוע אינו מסתייע על ידי חומצות האמינו הטעונות חיובית, ליזין וארגינין בעמדת P1. פפסין מהווה אחת מהסיבות הראשוניות לנזק לרירית בעת הרפלוקס של החלק התחתון של הלוע והגרון (Goldberg וחב' ב-Gastroenterology משנת 196, ו-Lillemoe וחב' ב-Surgery משנת 1982). פפסין נותר בלוע (pH 6.8) לאחר אירוע של רפלוקס קיבתי. אמנם פפסין אינו פעיל בסביבה זו, הוא נותר יציב ועשוי לעבור רה-אקטיבציה באירועים של רפלוקס חומצי. פפסין עלול לגרום נזק לרירית הגרון במהלך רפלוקס חומצי חלש או ברפלוקס קיבתי לא-חומצי (Tamhanker וחב' ב-J Gastrointest Surg משנת 2004, Discuamura וחב' ב-Am J Gastroenterol משנת 2004, ו-Mainie וח' ב-Gut משנת 2006). בתנאים לא-חומציים (pH נויטרלי), פפסין מוחדר לתאים של דרכי האוויר העליונות כמו תת-הלוע והגרון בתהליך הידוע כאנדוציטוזה המתווכת על ידי קולטנים (Johnston וחב' ב-Ann Otol Rhinol Laryngol משנת 2007). הקולטן דרכו פפסין עובר אנדוציטוזה אינו ידוע. כאשר פפסין נטמע על ידי התאים, הוא נאגר בשלפוחיות תאיות בעלות pH נמוך, בהן הפעילות האנזימטית שלו נשמרת. פפסין נשמר בתוך התא למשך עד 24 שעות (Johnston וחב' ב-Ann Otology Rhinology Laryngology משנת 2010). ממצאים אלה ומחקר נוסף מצביעים על מעורבות פפסין בקרצינוגניות המיוחסת לרפלוקס קיבתי (Adams וחב' ב-Arch Otolaryngol–Head Neck Surg משנת 2000). פפסין בדרכי האוויר נחשב להיות סמן רגיש וספציפי לרפלוקס תת-לועי וגרוני (Knight וחב' ב-The Laryngoscope משנת 2005, ו-Samuels ו-Johnston ב-Ann Otology Rhinol Laryngol משנת 2010). נמשך מחקר שנועד לפתח תרפיה כנגד פפסין, וכלים אבחוניים של רפלוקס קיבתי. זמין אבחון לא-חודרני לזיהוי פפסין הקרוי Peptest, בעזרתו ניתן לקבוע נוכחות של פפסין בדגימות רוק (Bardhan וחב' ב-Int J Otolaryngol משנת 2012).
מעכבים
פפסין יכול להיות מעוכב בתנאי pH גבוה או על ידי תרכובות מעכבות. Pepstatin היא מולקולה עם משקל מולקולרי נמוך ומעכב פוטנציאלי של פרוטאזות חומציות עם קבוע דיסוסאציה (Ki) של בערך 10−10 מולר לפפסין. שייר ה-statyl של פפסטטין נראה אחראי לעיכוב של פפסין; Statine הוא אנלוג פוטנציאלי של פאזת ה-transition לצורך קטליזה על ידי פפסין ופרוטאזות חומציות אחרות. פפסטטין אינו נקשר קו-ולנטית לפפסין, ולפיכך העיכוב של פפסין על ידי פפסטטין הוא הפיך (Marciniszyn וחב' ב-Advn Exp Med Biol משנת 1977). מעכב נוסף, bis(-2-phenylethane (diazoacetyl), גורם לאינאקטיבציה של פפסין ב-pH 5.0, ריאקציה העוברת החשה בנוכחות Cu(II) (Husain וחב' ב-Proc Natl Acad Sci USA משנת 1971). פפסין של חזיר מעוכב על ידי pepsin inhibitor-3 (להלן PI-3) המיוצר על ידי כֶּרֶץ עגול במעי החזיר (Ascaris suum) (Ng וחב' ב-Nature Struct Biol משנת 2000). המעכב PI-3 נקשר לאתר הפעיל של פפסין תוך שימוש בשייר ה-N טרמינלי שלו, וכך הוא חוסם את הקישור למצע בשיירים 1–3 (או Gln-Phe-Leu) של הפפסין. הקצה ה-N-טרמינלי של PI-3 בקומפלקס PI-3:pepsin מנוהל על ידי קשרי מימן היוצרים שמונה גדילים של β-sheet, בהם שלושה גדילים נתרמים על ידי פפסין, וחמישה גדילים נתרמים על ידי האתר הפעיל PI-3. תוצר של עיכול חלבון על ידי פפסין מעכב את הריאקציה (Greenwell וחב' ב-Biochem J משנת 1969, ו-Samloff ו-O'dell ב-Am J Med משנת 1985).Sucralfate, תכשיר המשמש לטיפול בכיבי קיבה ובעוד מצבים הנגרמים על ידי פפסין, גם כן מעכב את פעילות פפסין (Kun ב-Microbial Biotechnology משנת 2006).
שימושים
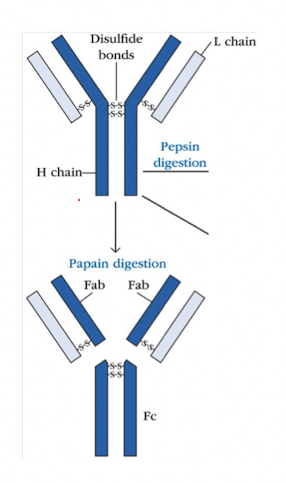
פפסין מסחרי ממוצה מהשכבה הגלנדולרית של קיבת חזירים. זהו מרכיב של אנזים הגבנה, הנמצא בקיבה של בעלי חיים מעלי גירה ומשמש בתעשיית החלב בתהליך ההגבנה, המשמש להחמיץ חלב במהלך הכנת גבינה. פפסין משמש במגוון של אפליקציות של הכנת מזון: לשנות ולספק איכויות הַצְלָפָה לחלבון סויה ולג'לטין (Smith ב-J General Physiol משנת 1933), לשנות חלבוני ירקות לשימוש במצרכים לא-חלביים, להפוך דגנים לא-מבושלים לדגנים אכילים, ולהכין הידרוליזטים של חלבונים מבעלי חיים ומצמחים ליצירת מאכלים ומשקאות טעימים. פפסין משמש בתעשיית העור להרחיק שיער ורקמה שארית, ולהרחיק כסף מפילמים פוטוגרפיים מורחקים על ידי עיכול של שכבת הג'לטין האוחזת את הכסף. פפסין היה היסטורית תוסף לגומי לעיסה שהוכן על ידי Edwin. Beeman. פפסין משמש לרוב להכנת מקטעים של F(ab')2 מנוגדנים. במבדקים אחדים, פפסין מועדף לשימוש בלעדי של חלק הקישור של אנטיגן (Fab) של הנוגדן. באפליקציות אלו, נוגדנים יכולים להיות מעוכלים אנזימטית ליצור את Fab או את מקטע F(ab')2 של הנוגדן. על מנת ליצור את מקטע F(ab')2, פפסין מבקע את השרשרות הכבדות של IgG ליד אזור הציר (hinge) (Falkenburg וחב' ב-J Immunol משנת 2017). אחד או יותר של הקשרים הדי-סולפידיים המחברים את השרשרות הכבדות באזור הציר משומרים, באופן ששני מקטעי Fab של הנוגדן נותרים קשורים יחד, כשהם יוצרים מולקולה דו-ולנטית המכילה שני אתרי קישור של הנוגדן, ולפיכך מוגדרים כ-F(ab')2. השרשרות הקלות נותרות שלמות ומחוברות לשרשרת הכבדה. המקטע Fc מעוכל לפפטידים קטנים. המקטעים של Fab נוצרים על ידי ביקוע של IgG על ידי papain במקום פפסין. Papain מבקע IgG מעל אזור הציר המכיל את הקשרים הדו-סולפידיים המחברים את השרשרות הכבדות, אך מתחת לאתר של הקשר הדו-סולפידי בין השרשרת הקלה והשרשרת הכבדה. זה יוצר שני מונו-ולנטים נפרדים (המכילים אתר קישור אחד של הנוגדן).
תכונות של פפסין, מבנה ושיטת מדידה
מיץ הקיבה של האדם מכיל 8 איזואנזימים של פפסין. חמשת הפפטידים המשתחררים בהתמרה של פפסינוגן לפפסין, נמצאו בעלי פעילות אנטי מיקרוביאלית כנגד Escherichia coli, פסאודומונאס וסטפילוקוקוס. בעוד שפפסינוגן יציב עד pH 10, פפסין יציב רק pH 7.0, ועובר דנטורציה מוחלטת ב-pH 8.0. מחלות רבות בתחום הנשימה והמזון יוחסו לנוכחות פפסין. לפיכך, המדידה של פפסין ברקמה ובשטיפה של איברים חלולים (lavage), ברוק או בליחה, עשויה להיות מדידה טובה לאבחון של מחלות רפלוקס. עם זאת, אין כרגע קונצנזוס בדבר הדרך הטובה ביותר לדגום או למדוד את רמת הפפסין. השיטה המקובלת של ELISA עם נוגדנים חד-שבטיים היא היעילה לזהות פפסין ברמת רגישות של 1–25 ננוגרם/מ"ל. הפפסינים הנוצרים לאחר פעילות פפסינוגן, מורכבים מ-1, 2, 3c ,3b ,3a, 4 ,6 ,5 ו-7, שניתנים להפרדה על ידי HPLC, או בשיטת אלקטרופורזה על ג'ל אגר (Etherington ו-Taylor ב-Nature משנת 1967, ו-Pearson וחב' ב-Digest Dis משנת 2010). פפסין 7 המבודד מרירית הקיבה נחשב כפרוטאזה הנעה באיטיות והוא נחשב כ־aspartate protease. עם זאת, פרקציה זו אינה פפסין אלא cathepsin E שהוא אנזים תוך-תאי (Samloff וחב' ב-Gastroenterology משנת 1987).
שפעול של פפסין והתפקוד של פפטידים משופעלים
מנגנון השפעול על ידי שינוי ב-pH ידוע היטב בפפסינים של חזיר ואדם (James ו-Sielecki ב-Nature משנת 1986). הפפטיד המשפעל, שהוא הקצה ה-N-טרמינלי של מולקולת פפסינוגן, המבוקע כאשר פפסין משופעל, נמצא בעל תכונות אנטי-מיקרוביאליות (Pane וחב' ב-ACS Synth Biol משנת 2018). לפפסינוגן אנושי יש רצף של 373 חומצות אמינו (Sogawa וחב' ב-J Biol Chem משנת 1983). בפפסין אנושי, הפפטיד המבוקע הוא בעל 47 חומצות אמינו והוא משתחרר לרוב כ-2 פפטידים המשפעלים את האנזים עם משקלים מולקולריים של 34-37 קילו-דלטון (Mills ו-Tang ב-J Biol Chem משנת 1967, ו-Roberts ו-Taylor ב-Biochem J משנת 1972). הביקוע מתרחש באזור של Leu23-Lys24-Asp25-Phe26, אך פפטידים באורך מלא גם כן יכולים להתגלות, בהופעת 5 פפטידים פוטנציאליים במיץ הקיבה, והם 1–23, 1–25, 24–47, 26–47 ו-1–47. ההבדל היחידי בין פפטידים אלה והפפטידים המקוריים של פפסינוגן, הוא שייר פרולין בקצה ה-N-טרמינלי, אם כי פרולין זה אינו משפיע על התכונות האנטי-מיקרוביאליות (Johnston וחב' ב-Ann Otol Rhinol Laryngol משנת 2010). הפפטיד 1–25 נמצא גם כן יעיל בעיכוב של Pseudomonas aeruginosa ושל Staphylococcus aureus.
הוראות לביצוע הבדיקה
יש לדגום הפרשות של צינור הנשימה או של דרכי האוויר בריאות לתוך מבחנת פלסטיק. יש לפקוק את המבחנה בחוזקה ולהקפיא מיידית. יש לשלוח למעבדה כדגימה קפואה.
יציבות הדגימה הקפואה - 30 יום.
ראו גם
המידע שבדף זה נכתב על ידי פרופ' בן-עמי סלע, המכון לכימיה פתולוגית, מרכז רפואי שיבא, תל-שומר;
החוג לגנטיקה מולקולארית וביוכימיה, פקולטה לרפואה, אוניברסיטת תל-אביב (יוצר הערך)


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק