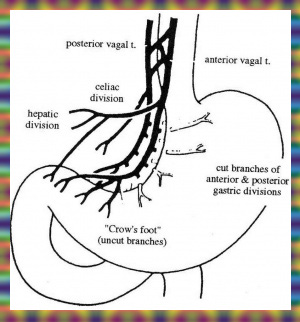
כיב עיכולי (פפטי) - Peptic ulcer
עקרונות בכירורגיה
מאת ד"ר צבי קויפמן
| עקרונות בכירורגיה | ||
|---|---|---|
| ||
| שם המחבר | ד"ר צבי קויפמן | |
| שם הפרק | כירורגיה של הקיבה והתריסריון | |
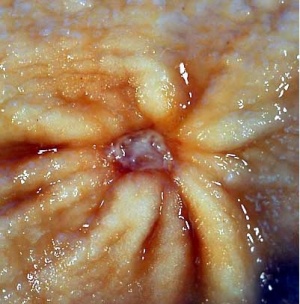
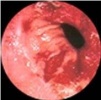
הכיב העיכולי (פפטי) הוא פצע במעי או בקיבה הנגרם עקב הפעילות העיכולית של החומצה והפפסין. כיב מוגדר כהרס מוקדי של הרירית, החודר את הרירית השרירית (מוסקולריס מוקוזה) של דופן המעי. לעומת זאת, בארוזיה (Erosion) הנזק הוא של הרירית ואינו עובר את הרירית השרירית (מוסקולריס מוקוזה) (תמונה 1.3).
הכיב העיכולי (פפטי) הוא אחת המחלות השכיחות באוכלוסייה המערבית. הוא יכול להופיע בוושט, בקיבה, בתריסריון, בתוך הסעיף על-שם מקל, במעי הדק ובהשקות לקיבה. הכיבים יכולים להיות חריפים או כרוניים.
הכיב הפפטי נוצר עקב הפרעה בשיווי המשקל בין המנגנונים המגינים של מערכת העיכול לבין אלה התוקפים - חומצה ופפסין. כאשר המנגנון התוקף גובר, מתחיל עיכול של רירית מערכת העיכול על-ידי הפפסין שנוצר מפפסינוגן, בסביבה החומצית של הקיבה. רירית הקיבה מוגנת על-ידי מערכת של תאים המסוגלים לנטרל את יוני המימן החודרים לרירית. כמו-כן מפרישה הרירית ריר בעל תכונות בסיסיות, המקשה על הזרימה החוזרת של יוני המימן לרירית ומנטרל את החומצה שבאה במגע אתו.
בחלקו הראשון מכיל התריסריון תאי רירית המפרישים ריר בסיסי, המקנה הגנה לתאים, בדומה לרירית מערת השוער (האנטרום). כמו-כן מפרישים תאיו ביקרבונט, המגן על הרירית על-ידי נטרול החומצה שבתמיסה. הגנה זו טובה יותר, ככל שזרימת הדם לקיבה ולתריסריון טובה יותר.
מאפיינים של הכיבים השונים
בחולי כיב התריסריון יש כמה גורמים מאפיינים או מסייעים להיווצרות הכיב. הסיבה להיווצרות הכיב קשורה במספר גורמים המאפיינים את חולי הכיב:
- שכיחות יתר של חיידקי HP על פני רירית הקיבה (ממצא הקיים ב-90% מהחולים).
- בחולים אלה ההפרשה הבסיסית הממוצעת של החומצה גבוהה מהתקין.
- בחולים אלה מספר התאים הפריאטליים כפול ואף יותר מאשר באוכלוסייה בלא כיב, וזאת באופן ראשוני או משני.
- תגובתם להפרשת גסטרין מהירה וחזקה יותר.
- עיכוב הפרשת הגסטרין מתרחש בערכי pH נמוכים יותר.
- התרוקנות הקיבה בחולי כיב מהירה יותר, ולכן העמסת החומצה על התריסריון היא גדולה יותר.
כיב הקיבה שכיח פחות מכיב התריסריון. השכיחות היחסית של כיב הקיבה ביחס לכיב התריסריון היא 10-5:1. כיב הקיבה שכיח בחולים בעלי רמות חומצה תקינות או אף נמוכות. גם בכיב הקיבה הוכח שנוכחות חיידקי HP מהווה גורם חשוב בהיווצרות הכיב (ל-80% מהחולים יש HP ברירית הקיבה). עיקר הפגיעה היא במנגנון ההגנה על רירית הקיבה. זרם חוזר (רפלוקס) של מיצי מרה ולבלב לאחר ארוחות חשיבות רבה מאוד בהתפתחות כיב הקיבה. בחולים אלה הודגם רפלוקס גדול יותר לאחר ארוחות, וכן במקצתם הודגם אי-תפקוד של השוער. מלחי המרה פוגעים ברירית הקיבה וחושפים אותה לתהליך עיכול על-ידי החומצה והפפסין. מכיוון שפעילות המרה ב- Alkaline gastritis היא מהשוער לעבר האנטרום והגוף, רוב הכיבים יימצאו באזור האנטרום בסביבה עם מיעוט חומצה. לפי Oi וחבריו, רוב הכיבים מופיעים בחלק הקריבני של האנטרום, ליד האינסיסורה אנגולריס (החרק הזויתי), באזור המעבר בין סוגי הרירית השונים, בצד הרירית שאינה מפרישה חומצה. הם גם טוענים שלתנועתיות הקיבה השפעה על זרימת הנוזל בקיבה על יצירת הכיב.
כיבים חדים נקראים גם בשמות אחרים: Cushing ulcer, Curling ulcer, Stress ulcer וכו', ולכולם מנגנון היווצרות דומה. כיבים אלה נוצרים על-ידי מטבוליטים או במנגנונים הפועלים על הקיבה כאיבר מטרה. עם התקדמות הרפואה יותר ויותר חולים במצבים קשים שורדים, ולפיכך שכיחות הופעת הכיבים עולה. הפגיעה ברירית הקיבה עקב דחק (Stress) מחבלת באיזון שבין החומצה והפפסין לבין מנגנון ההגנה. מנגנון ההגנה נפגע עקב פגיעה באספקת הדם, חמצון ועוד. פגיעה בקרום תאי האפיתל נגרמת עקב פגיעה במשאבת הנתרן-מימן. לפיכך חודרים יוני מימן לתוך התא, גורמים להריסתו ויוצרים כיבים. בחולים הלוקים בפגיעות מוחיות ובכיבים אפשר להדגים פעילות יתר של הואגוס, הגורמת להפרשת יתר של חומצה וגסטרין. נוכחות כמויות גדולות מאוד של חומצה מפריעה לתהליך הדיפוזיה החוזרת של החומצה, וגורמת להרס הרירית.
כיבים הנוצרים במעי הדק מקורם ב:
- הפרשה מרובה מאוד של חומצה בקיבה, כגון בתסמונת זולינגר-אליסון.
- הפרשת חומצה במעי הדק עקב קיומם של מוקדי רירית הדומה לרירית הקיבה.
- נזק לרירית המעי, עקב השקות בין הקיבה למעי הדק. כיבים אלה גורמים בדרך-כלל לכאבי בטן ולדימומים כרוניים או חדים ומסיביים.
תסמינים קליניים של כיב פפטי
- התסמינים הקליניים מתאפיינים בתכונות הבאות
- נטייה של מחלת הכיב להיות כרונית ותקופתית. ההתקפים מתמידים שבועות אחדים עד חודשים, וחולפים בעזרת טיפול תסמיני (סימפטומטי).
- התקפים עונתיים - השכיחות הגבוהה ביותר של הופעת התסמינים הקליניים או סיבוכי המחלה היא בעונות המעבר (אביב וסתיו).
- נטייה להופעה בזמן דחק (Stress).
- התסמינים הקליניים השכיחים הם
- כאב: הכאבים ממוקמים באפיגסטריום, בקו האמצע בין זיז עצם החזה (הקסיפואיד) לטבור. הכאב מתואר כשריפה, צביטה, כאבי רעב או גזים בבטן, המופיעים 3-1 שעות לאחר הארוחה. זמן זה, הוא הזמן שבו הפרשת החומצה גוברת על יכולת הקיבה לנטרלה. התסמין הקליני הבולט הוא הכאב. כאבי הרעב מוחמרים על-ידי סוגי אוכל מסוימים, אלכוהול ועישון, ומוקלים על-ידי סותרי חומצה או אוכל. הכאבים הם גליים, נמשכים כמה שעות וחולפים. באופן מובהק, כאבים גורמים לחולה להקיץ משנתו. הכאבים מלווים בצרבת, עקב רגורגיטציה של חומצה לוושט. אם הכאבים מתמידים, חדים, מקרינים לגב ואינם מגיבים לטיפול רגיל, אין מדובר לרוב בכיב רגיל, אלא בכיב החודר ללבלב. התגובה לטיפול התרופתי (הקלה בכאב) מופיעה שבועות לפני שהכיב נרפא.
- דימומים: 20% מהחולים הסובלים מכיב התריסריון מדממים. ברוב החולים הדימום מלווה בכאבים כמה ימים לפני תחילתו. דימום מסיבי אינו שכיח כסימן הראשון למחלת הכיב. 85%-90% מהדימומים נפסקים עצמונית. הסיכון לדימום חוזר עולה מ-25% לאחר 3 שנים, ל-33% לאחר 5 שנים, ול-50% לאחר 10 שנים מהדימום הראשון. דימום שלישי יתרחש ב- 60% מהחולים 5 שנים לאחר הדימום השני. דימום מסיבי נובע מחדירת הכיב ללבלב ועיכול עורק הקיבה-תריסריון (Gastroduodenal artery). הדימום מתבטא בהופעת שחרה (מלנה - צואה שחורה כזפת) והקאה דמית. שחרה יכולה להופיע לאחר דימום של 50 סמ"ק בלבד. הקאה דמית מעידה על דימום מסיבי. בדרך כלל חולים אלה שרויים בהלם תת-נפחי (היפוולמי), בזמן הגעתם לבית החולים. שליש ממקרי הדימום ממערכת העיכול העליונה מקורם בכיב התריסריון.
- התנקבות: התנקבות (פרפורציה) שכיחה ב-10%-5% מחולי כיב התריסריון. ב-2% מהחולים ההתנקבות היא הסימן הראשון לכיב. התנקבות מאופיינת בכאבי בטן פתאומיים, חדים וקשים, דמויי דקירת סכין. בחולים זקנים ותשושים כאבי הבטן בולטים פחות וסימני הגירוי הצפקי (פריטונאלי) מופיעים בשלב מאוחר יותר ואף הם בולטים פחות. לפעמים, עקב הדלקת נוצרות הידבקויות, המגבילות את התהליך, והכאבים יכולים לחלוף, ואולם חולים אלה ימשיכו לסבול מכאבי בטן ממוקמים ומתסמונת הכיב. לעתים הם מפתחים מורסה מקומית הדורשת ניקוז.
- חסימת השוער: חסימת השוער מופיעה ב-5%-4% מחולי הכיב. היא מאופיינת בהקאות בלא תוכן מרתי, פרויאקטיליות (Projectile) בכמות גדולה ובתוכן בלתי מעוכל. לאחר ההקאות החולה מרגיש הקלה. הוא יכול להמשיך לאכול, אך אחר כך שוב יקיא את האוכל שאכל בלא שיתעכל. תסמינים אחרים המתוארים הם: מלאות בבטן, כאבים, חוסר תיאבון וירידה במשקל.
שתי צורות חסימה מוכרות:- הצורה החריפה - עקב התלקחות הכיב נוצרת בצקת סביב השוער הגורמת לחסימתו. מצב זה חולף בדרך כלל כעבור ימים אחדים של טיפול בכיב.
- הצורה הכרונית - בה הכיב נרפא על-ידי צלקת הגורמת להיצרות השוער. היצרות פיברוטית (לייפתית) זו מתקדמת עד לחסימה שלמה של השוער. החולים סובלים מהתייבשות (דהידרציה) קשה ומהפרעות אלקטרוליטריות, בייחוד מהסוג של בססת מטבולית היפוכלורמית והיפוקלמית (Hypochloremic hypokalemic metabolic alkalosis) והיפונתרמיה.
התמונה בילדים אינה אופיינית ולא-תמיד פשוטה לאבחנה. גם בחולים הלוקים בכיב בשוער או בכיב לאחר בצל התריסריון (פוסט-בולברי) התמונה יכולה להיות ביזארית. הלוקים בכיב כזה לרוב לא יתלוננו על כאבים אופייניים ולא יגיבו לטיפול בסותרי חומצה.
אבחנה
גסטרוסקופיה (תצפית קיבה)
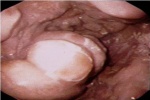
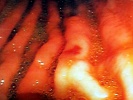
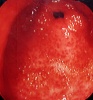
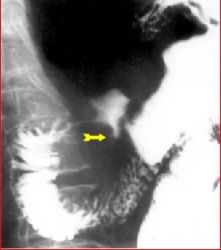
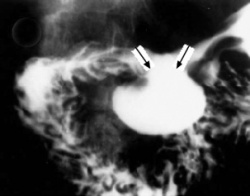
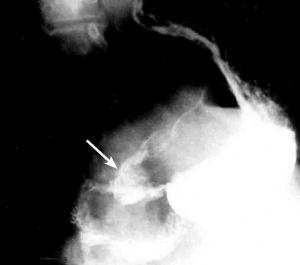
שיטת האבחנה העיקרית היא הגסטרוסקופיה המאפשרת לראות היטב את הכיב ומיקומו, ואת השינויים ברקמה שסביב לכיב. הדיוק האבחנתי של הגסטרוסקופיה הוא 95%. הגסטרוסקופיה מאפשרת לאבחן את מקור הדימומים הפעילים (תצלומים 3.3) וכן ליטול ביופסיות מממצאים חשודים ולקבל אבחנה היסטולוגית. הגסטרוסקופיה חשובה לאבחנה מבדלת בין דימום שמקורו בדליות הוושט (תמונה 4.3) לבין דימום שמקורו בקיבה או בתריסריון. כיב חוזר בקו ההשקה, קרעים ברירית (בתסמונת על-שם מלורי-וייס (Mallory-Weiss)) (תמונה 5.3), דלקת קיבה וארוזיות ניתנים לאבחנה ולהוכחה, בעיקר בעזרת הגסטרוסקופיה, ואין אפשרות להדגימם כראוי ברנטגן (תמונה 2.3 , 6.3).
ביופסיה והיסטופתולוגיה
ההוכחה המוחלטת לקיומו של חיידק ההליקובקטר במערכת העיכול היא על-ידי צפייה ישירה בו. ניתן לבצע זאת באמצעות גסטרוסקופיה ולקיחת דגימות רקמה. ניתן להסתכל במיקרוסקופ על דגימות אלו ולצפות באופן ישיר בחיידק. חסרונות השיטה היא בהיותה פולשנית ובמחירה.
בדיקת אוראז מהירה
לחיידק ההליקובקטר תכונה ביוכימית ייחודית - פרוק אוראה על-ידי אנזים האוראז. תכונה זו מנוצלת בבדיקה בה פיסת רקמה מוכנסת לתמיסה המכילה אוראה ומשנה את צבעה תוך מספר שעות כאשר האוראה מתפרקת על-ידי החיידק (תוצאה חיובית). כשהתוצאה שלילית, הסיכויים גבוהים שאכן אין חיידקים בדגימה הנבדקת; אולם כשהתוצאה חיובית, יש עדיין סיכוי שלא מדובר בחיידק. הגורמים המשפיעים על תוצאות הבדיקה הם בין השאר נטילת תרופות מסוימות, אזור נטילת הדגימה, כמות החיידקים הנמצאים ברקמה הנבדקת ועוד.
תרבית של החיידק
כאשר יש פיסת רקמה מהביופסיה, ניתן לנסות ולגדל ממנה במעבדה את החיידק. בדיקה זו מאפשרת לנו לזהות את קיומו של החיידק וכן לבדוק את רגישותו לתרופות אנטיביוטיות שונות. אך אליה וקוץ בה - קשה מאוד לגדל חיידק זה בתרבית והעלויות הן מרובות ולכן ברוב המקרים (למעט לנושאי מחקר) לא מבוצעת שיטה זו.
מבחן נשיפה על-ידי אוראה מסומנת ברדיו-אקטיביות
מבחן זה מבוסס על יכולתו של החיידק לפרק את החומר אוראה. החומר ניתן בשתיה וכאשר הוא מפורק על-ידי החיידק, ניתן לזהות אותו באוויר הננשף ובכך להוכיח את קיומו של החיידק.
צילום הקיבה והתריסריון בעזרת חומר ניגוד
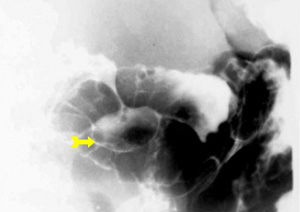
בליעת בריום תדגים את הכיב ב-80% מהחולים. זה יכול להיות כיב פעיל, או צלקת של כיב ישן. 95% מהכיבים הם בבצל התריסריון (בולבריים), ורק 5% מהם לאחר בצל התריסריון (פוסטבולבריים). מיעוטם ממוקמים בשוער (פילורוס). בצילום קשה למלא את הבצל מכיוון שהכיב מלווה בדלקת ובבצקת, ולפיכך ניתן לראות רק מילוי חלקי שלו. הדגמת המכתש (Crater) היא חשובה ביותר מכיוון שהיא מעידה על כיב פעיל. לעתים רואים את המכתש מוקף בהילה (Halo) של פגם מילוי, הנוצר עקב הבצקת שסביב הכיב.
הכיבים בצילום ממוקמים מלפנים, או מאחור, ונראים היטב חזיתית (En-face). כיבים לא פעילים גורמים לעווית וללייפת (הצטלקות) בדופן. בחולים הלוקים בכיבים כאלה ניתן לראות הרחבה של קפלי הרירית היוצאים כקרניים מהכיב - התכנסות קמטים. לעתים תיראה אסימטריה של הבצל (בולבוס), לפעמים סעיף מדומה(פסאודו דיברטיקולום), או עיוות של השוער (פילורוס) מלווה בהפרעות בהתרוקנות הקיבה.
ב-15% מהכיבים הפוסט-בולבריים (רובם נמצאים פרוקסימלית לפפילה), ניתן למצוא בנוסף גם כיבים בולברים - כיבים נושקים (Kissing ulcer). עם ריפוי הכיב, תיראה הפחתה בקוטר הכיב עד היעלמותו. בשלבים אלה תיראה בצילום צורה של עלה תלתן, כביטוי לצלקת מקומית ופיברוזיס באזור הכיב. אין די בהדגמת הפגם בצילום אחד, אלא יש להדגימו בכמה צילומים (תצלומים 4.3-1.3). מאז נכנסה הגסטרוסקופיה צילום הקיבה והתריסריון איבד מחשיבותו ולא מבוצע יותר כבדיקת שגרה.
תפקודי הקיבה
ברוב החולים לאבחון וטיפול בכיב התריסריון אין צורך כיום בתפקודי הקיבה, והם משמשים רק בחולים העמידים לטיפול. ניתן למצוא הפרשת חומצה רבה לאחר גירוי ב-Pentagastrin (PAO - יותר מ-15 מא"ק/ל'). בחולים שבהם ההפרשה קטנה מזו, האבחנה של כיב אינה סבירה. במחצית הגברים ובכל הנשים ניתן לראות הפרשה מרבית, בכמות גדולה מזו התקינה. מדידות pH במערת השוער (האנטרום) ובתריסריון הראו, שחולים הלוקים בכיב התריסריון הם בעלי pH נמוך יותר בתריסריון מאשר קבוצת ביקורת, ולעומת זאת, באנטרום הערכים זהים. בחולים הלוקים ביתר-גסטרין הפרשת החומצה היא גבוהה ביותר, לרוב יותר מ-45 מא"ק/ל'. רמות של יותר מ-60 מא"ק/ל' הן אבחנתיות ליתר-גסטרין. בחולים הלוקים בחוסר חומצת מלח (Achlorhydria) וכיב, הכיב הוא בדרך כלל ממאיר. תפקודי החומצה חשובים גם להערכת היעילות של כריתת הואגוסים כטיפול בכיב.
מדידות הגסטרין בדם מראות ערכים גבוהים בחולים הלוקים בגסטרינומה, באי-ספיקה כלייתית ובהיפרפלזיה של תאי G.
אבחנה מבדלת
בחולים עם כאבי בטן הדומים לאלה של כיב עיכולי (פפטי) יש לשלול:
- דלקת כרונית של כיס המרה.
- דלקת לבלב חדה.
- דלקת וושט (אזופגיטיס).
- בעיית עיכול תפקודית (Functional indigestion).
בחולים עם דמם מדרכי העיכול העליונות — המקור לדימום יכול להיות:
- 20% דלקת קיבה
- 10% מלורי-וייס
- 5% סיבות לא שכיחות (קרצינומה בקיבה, דלקת וושט, דם במרה, סעיף בתריסריון, גידול בתריסריון, מפרצת בעורק הטחול וכו')
- 55% כיב עיכולי
- 40% כיב בתריסריון
- 15% כיב בקיבה
- 10% דליות בוושט
בחולי דלקת הצפק עקב התנקבות הכיב יש לשלול:
- דלקת חריפה של כיס המרה.
- דלקת חדה של הלבלב.
- התנקבות כיס המרה.
- התנקבות המעי הדק.
- התנקבות הכרכשת (דלקת סעיף (דיברטיקוליטיס) או שאת וכו')
בחולים המקיאים עקב חסימת השוער יש לשלול מקור אחר להקאות, כגון:
- חסימת מעי.
- הקאות רפלקטוריות (תרופות, מחלות מערכת העצבים וכו')
- חסימות בתריסריון (שאתות, לבלב טבעתי וכו')
- שאת ממארת החוסמת את נהור הקיבה.
- סומטוסטטינומה.
טיפול
הטיפול התרופתי הפך לטיפול העיקרי בחולי כיב התריסריון ואילו ההוריות לטיפול הכירורגי הצטמצמו ביותר (טבלה 1.3)
- טבלה 1.3
- טיפול תרופתי בכיב פפטי
- נוגדי חומצה
- Alumag
- Maalox
- Magel
- Rekiv
- Silain-Gel
- חסמי H2
- אנטיכולינרגיים
- Pirenzepine (Ulcepin)
- Propantheline (Pro-Banthine)
- Oxyphencyclimine (Daricon)
- Atropine
- Chlordiazepoxide (Nirvaxal)
- Omeprazole
- Sucralfate
- Carbenoxolone (Biogastrone)
- Somatostatin
- טיפול בהליקובקטר
עקרון הטיפול הוא:
- להעלות את ה- pH של הקיבה ליותר מ-5.5, כדי לנטרל את הפיכת הפפסינוגן לפפסין.
- בחולי הליקובקטר חיובי - חיסול החיידק בקיבה.
הדיאטה היא על-פי המזון שטוב לחולה. רבים המקרים שבהם חלב מחמיר את הכאב, מכיוון שהוא מכיל כמויות של סידן, ולכן הוא מגרה הפרשת גסטרין. אין לאכול לפני השינה, אבל יש ליטול סותרי חומצה.
סותרי חומצה
טיפול של סותרי חומצה שעה ו-3 שעות לאחר הארוחה, וארוחה נוספת שעה אחר כך מביאים עמם ריפוי של הכיב ב-78% מהחולים, לעומת 45% בקבוצה שקיבלה אינבו. שיעור החזרות לאחר 6 חודשים זהה בשתי הקבוצות (25%).
תרופות אנטיכולינרגיות
להשגת אפקט טיפולי יש לתת את התרופות האנטיכולינרגיות במינון הגורם לסימנים משניים של התרופה, כגון יובש, טכיקרדיה, עצירות וכו'. רבים מהמטפלים אינם משתמשים בהן במסגרת הטיפול בכיב.
חוסמי היסטמין (H2 blockers)
תרופות אלה חוסמות את גירוי ההיסטמין להפרשת חומצה, חסימה ברירנית לקיבה. Cimetidine ו-Ranitidine הן דוגמאות לחוסמי H2: סימטידין (Cimetidine) (שם מסחרי: Tagamet) נספג דרך התריסריון והג'ג'ונום. הסימטידין מופרש דרך הכליות, בצורה לא-מפורקת. שיא הרמה בדם מושג בתוך 90-60 דקות. זמן מחצית החיים שלו הוא 120 דקות. טבלייה של 300 מ"ג מאפשרת רמה של 5.0 מיקרוגרם לסמ"ק למשך 4 שעות. רמה זו מפחיתה את הפרשת החומצה ב-50%. אם הסימטידין ניתן בזמן הארוחה, השיא מופיע בתוך 3-2 שעות, והוא מקביל לשיא הפרשת החומצה לאחר הארוחה.
כיום ההמלצה היא להשתמש במינון של 400 מ"ג פעמיים ביום, במתן דרך הפה, במצבים חדים, למשך חודש, ולהמשיך לאחר מכן במינון של 400 מ"ג לפני השינה. באחרונה הופיעו דיווחים בספרות, שלפיהם מתן רצוף של סימטידין בהזלפה רצופה לווריד, 50 מ"ג בשעה, במשך 24 שעות, קשור לשיעור גבוה יותר של הצלחות טיפוליות במצבים חדים.
במינון של 1.2-0.8 גרם ביום, במשך 4-3 שבועות, אפשר להשיג ריפוי של 70% מכיבי התריסריון. מחקר שהשווה את השפעת סותרי החומצה והסימטידין הראה, שבשניהם אפשר להשיג עד 80% ריפוי של כיב מוכח. ואולם בחולים הלוקים בכיבים כרוניים ובתסמונת ממושכת, התגובה הקלינית לסימטידין טובה יותר. ב-24% מהחולים הכיב חזר עוד בתקופת הטיפול, ב-43% מהחולים הכיב חזר בתוך 6 חודשים מגמר הטיפול, וב-70% לאחר שנה מתום הטיפול. הסימטידין לא שינה את המהלך הטבעי של מחלת הכיב. שיעור ההתנקבויות בתקופת הטיפול בסימטידין לעומת שיעור זה לפני כן נותר זהה.
השימוש בסימטידין בגסטרינומה יעיל. הוא מפחית את השלשולים ומקטין את עומס החומצה על רירית התריסריון. המנה הנדרשת היא 2.4-1.2 גרם ביום. לעתים, כדי להשיג השפעה יש להשתמש במנות גדולות מאוד - 9-3 גרם ביום. מהשוואת תוצאות הטיפול בכיבים חוזרים, בסימטידין או בכירורגיה, עולה שבתום שנה מתחילת הטיפול בסימטידין 90% מהחולים נרפאים, ואילו בקבוצה שנותחה 95% נרפאים. ואולם בקבוצה שטופלה תרופתית, בתוך שנה מהפסקת הטיפול 71% מהחולים סובלים מחזרת המחלה.
תופעות הלוואי הקשורות בטיפול בסימטידין הן:
- הפרעות נוירופסיכיאטריות - בלבול שכיח בעיקר בזקנים.
- ירידה במטבוליזם של תרופות בכבד - Coumadin, Diazepam (Valium), Propranolol (Deralin), Lidocaine וכו'
- הפרעות אנדוקריניות - הגדלת השד בזכר (גינקומסטיה), זוב חלב (גלקטוריאה), העדר זרע (אזוספרמיה), אין-אונות.
- הפרעות במערכת ההמטופויאטית - אגרנולוציטוזיס, מיעוט טסיות הדם (תרומבוציטופניה).
סיבוכים אחרים המדווחים הם: כאבי שרירים, שלשול קל, בחילות, פריחה, חום, נויטרופניה, דלקת לבלב חדה, הפרעות קצב וירידה בלחץ הדם בחולים המקבלים את התרופה לווריד באופן מהיר.
- מינון
- כיב פעיל
- 400 מ"ג פעמיים ביממה.
- 200 מ"ג ביום, ו-400 מ"ג לפני השינה.
- טיפול מונע
- 400 מ"ג לפני השינה.
רניטידין (Ranitidine) (שם מסחרי: Zantac) - שייך לקבוצת חוסמי ה-H2. להבדיל מסימטידין, הוא אינו מגרה הפרשת פרולקטין, הגורם להגדלת השד בזכר במשתמשים בסימטידין, וכן אינו מתחרה עם הטסטוסטרון, ולכן אינו מדכא את פעולתו, ולא גורם לאין-אונות והעדר זרע (אזוספרמיה). הוא אינו פוגע באנזימים המקרוזומלים בכבד או בתגובת הלימפוציטים, לא גורם לבלבול במבוגרים ולא מעלה את הקראטינין, כפי שקורה במטופלים בסימטידין. הרניטידין הוא מעכב חזק יותר של הפרשת החומצה ביחס לסימטידין. הוא מעכב גם את הפרשת הפפסין. שילוב של רניטידין עם אנטיכולינרגיקה יוצר חסימה שלמה של הפרשת החומצה. משך פעולתו ארוך יותר, כך שאת התרופה יש לקחת רק פעמיים ביממה.
זהירות יתר בשימוש בתרופה יש לנקוט בחולים עם תפקוד כלייתי לקוי (הפחתת המינון). יש לוודא שלחולה אין שאת ממארת בקיבה. התרופה מופרשת בחלב אם ולכן יש להיזהר מפני השימוש בתרופה בהיריון ובהנקה.
תופעות לוואי: כאב ראש, עצירות, בחילות, כאבי בטן, פריחה, ירידה במספר התאים הלבנים (לויקופניה), דלקת כבד ועלייה בטרנסאמינזות בנסיוב.
- מינון
- כיב פעיל - 150 מ"ג פעמיים ביממה.
- טיפול מונע - 150 מ"ג לפני השינה.
Famotidine (שם מסחרי: Gastro, Pepcid) - שייך אף הוא לקבוצת חוסמי ה-H2. הוא יותר פעיל מהסימטידין, וניתן לקחתו במינונים של 40 מ"ג פעם ביממה או 20 מ"ג פעמיים ביממה. תופעות הלוואי דומות לאלה של הרניטידין.
סוכראלפאט (Sucralfate) (שם מסחרי: Ulsanic) - דומה במבנה ל-Heparin, אבל בלא אפקט נוגד קרישה. מורכב מאוקטאסולפט סוכרוז ואלומיניום הידרוקסיד. ב- pH של הקיבה החומר עובר פולימריזציה, מולקולות האוקטאסולפט סוכרוז מתקשרות לחלבונים בעלי מטען חיובי כמו אלבומין, פיברינוגן ותאים מתים הנמצאים בבסיס הכיב, ויוצרים מעין משחה קשה המכסה את הכיב. הקשרים בין החומר לחלבון נמשכים לפחות שש שעות. מכיוון שאין ספיגה של החומר הרי תופעות הלוואי מעטות. המשחה הסמיכה שנוצרת מגינה על התאים מפני פעולת הפפסין, וכן מפעולת מלחי המרה. שחרור האלומיניום הידרוקסיד מנטרל את החומצה בסביבה.
במינון 1 גרם 4 פעמים ביממה, 92% מהחולים נרפאו בתוך 4 שבועות, בהשוואה לקבוצת הביקורת, שבה נרפאו 58% מהחולים. התרופה זקוקה לסביבה חומצית, ולכן יש להימנע מלתת אותה בשילוב עם סותרי חומצה אחרים. בעבודות משוות נמצא שהסוכראלפאט מעט פחות טוב מהסימטידין. עצירות מופיעה ב-2% מהחולים.
פרוסטגלנדינים - האנלוג של ה-PGE2, המתיל פרוסטגלנדין 15-152, נמצא בשימוש. הוא מעכב הפרשת חומצה ומגן על רירית הקיבה. עבודות מבוקרות ציינו ריפוי של הכיב ב-67% מהחולים אחרי 4 שבועות, לעומת 34% בקבוצת האינבו. שימושו העיקרי כיום הוא במניעת כיבים בחולים שנוטלים נוגדי דלקת לא סטרואידיים (NSAID).
תרופות מרגיעות טובות לטיפול במצב החד, אך לא כטיפול שגרתי. במקרים קשים יש להחדיר זונדה ולשאוב את מיצי הקיבה כדי להקל על הכאב.
אומפרזול (Omeprazole) (שם מסחרי: Losec) - תרופה חדישה יחסית לטיפול בכיב פפטי. יעילותה גבוהה מזו של הסימטידין. התרופה פועלת ישירות על משאבת המימן בתאים הפריאטליים ומשתקת אותה. בתוך 4 שבועות 99% מהכיבים נרפאים.
האומפרזול בולם את ה- H,K-ATPase (משאבת הפרוטון) הנמצא בתאים הפריאטליים בקרום האפיקלי. האומפרזול מתפרק לשתי קבוצות: (1) Sulphenic acid (2) Sulfenamide, המגיבים עם קבוצות Sulfehydryl-r של האנזים. כששתי הקבוצות נקשרות לאנזים, הן בולמות אותו וכך הן מפסיקות את פעולתה של משאבת המימן. האומפרזול מפחית את הפרשת החומצה עד 95% במינון של 30 מ"ג ביממה.
סיבוכים שדווחו הם: בחילות, שלשולים, כאבי בטן עוויתיים, כאבי ראש וסחרחורות, תפרחת בעור, ירידה במספר התאים הלבנים (לויקופניה) ופגיעה כבדית. המינון המקובל הוא 40-20 מ"ג פעם ביממה במשך 8 שבועות.
סומטוסטטין — הורמון המדכא את פעולת מערכת העיכול. הוא מפחית את זרימת הדם בקיבה, הפרשת חומצה והפרשת גסטרין, וכך מסייע לריפוי הכיב.
טיפול תרופתי בהליקובקטר
הטיפול התרופתי בהליקובקטר על-ידי תרופה יחידה אינו יעיל. הטיפול המומלץ בספרות הוא הטיפול המשולב המשולש, שכולל Bismuth sub salicylate (דה נול), Amoxycillin ו-Metronidazole. משך הטיפול הוא עד שבועיים. שיעור תופעות הלוואי המדווחות הוא 30%, ו-10%-5% מהחולים נאלצים להפסיק את הטיפול עקב תופעות הלוואי. מדווח על ההצלחה בטיפול באומפרזול (Losec) בשילוב עם אמוקסיצילין במשך שבועיים. טיפול זה גורם להכחדת החיידק ב-90% מהמקרים. השילוב של חוסמי ה-H2 מטרתו להפחית את החומציות וכך, לאפשר פעילות טובה יותר של האנטיביוטיקה הניתנת. צמצום משך הטיפול לשבוע לא הקטין את שיעורי ההצלחה בהכחדת החיידק.
הטיפול המומלץ באחרונה הוא טיפול ב-Tinidazole (פאסיגין 500x2) ובאומפרזול 20 מ"ג ביממה למשך שבוע. שיעור ההכחדה הוא 96% ושיעור ההיענות לטיפול הוא כמעט 100%.
השילוב המקובל הוא אומפרזול (Losec) 20 מ"ג פעמיים ביממה ואמוקסיצילין (Moxypen) 1 גרם פעמיים ביממה, או מטרונידזול 0.5 גרם פעמיים ביממה למשך שבועיים. ב-4% מהחולים בהם הוכחד החיידק הוא יופיע שוב ויגרום לתסמונת כיב חוזרת.
טיפול שמרני בחולה המדמם
בחולה המדמם יש לטפל בו-זמנית, הן במצבו ההמודינמי והן בכיב. לשם הערכת מצבו של החולה המדמם יש להעריך את מידת הדימום. הסתמנויותיו של דימום חמור בחולה הן:
- הקאת קרישי דם.
- Hematochezia (דם אדום בצואה).
- סיפור של התעלפויות.
- ירידה בלחץ הדם, טכיקרדיה והלם (חולה מתקבל למיון בהלם).
- ירידה ניכרת ברמת ההמטוקריט תוך שעות מתחילת הדימום.
- כאבים עזים בחזה או שינויים באק"ג של חולה במחלת לב כלילית (קורונרית).
- התפתחות אירוע מוחי (CVA) תוך כדי דימום.
סימנים אלו מעידים על תוצאות חמורות של הדימום, ולאו דווקא על דימום חמור בכמותו. עם קבלת החולה למיון, יש להעריך את כמות הדם שאיבד בעזרת הסיפור הקליני והסימנים שלעיל. יש להרכיב לחולה עירוי נוזלים, ובמקרים חמורים, או בזקנים - יש להרכיב CVP. מתחילים בהזלפת רינגר לקטט או תמיסת מלח (סאלין) דרך העירוי, ובהתאם לצורך - דם ופלסמה. אם החולה אינו נותן שתן עצמונית, יש להכניס צנתר לשלפוחית.
בחולים מדממים יש לבדוק את תפקודי הקרישה, ואם קיים ליקוי במנגנון הקרישה יש לתת לחולה פלזמה טריה, משקע קור (Cryoprecipitate) וטסיות (תרומבוציטים), בהתאם לליקוי במנגנון הקרישה.
יש להכניס זונדה לקיבה, לבצע שטיפות של תוכן הקיבה, ובתוך כך להתרשם מצבע הנוזל החוזר. דם טרי מעיד על דימום פעיל, ואילו דם ישן (Coffee ground) מעיד על דימום בעבר הקרוב. שטיפת הזונדה וריקון הקיבה מאפשרים התכווצות הקיבה, ובעקבות זאת הפסקת הדימום. קיבה מורחבת מאוד נוטה לדמם יותר. דם טרי המופיע שוב בזונדה לאחר ריקון הקיבה מעיד כי החולה ממשיך לדמם, או החל לדמם שוב, ולכך יש להתייחס ברצינות בהחלטה על המשך הטיפול.
בד בבד מטפלים בחולה בסותרי חומצה בכמות גדולה יחסית, עד להשגת נטרול החומצה בקיבה. יש המתחילים בטיפול בו-זמני בחוסמי H2 במינון גדול (סימטידין 1.6-1.2 גרם ביום). השימוש בסותרי החומצה חשוב, מכיוון שהעלאת ה-pH מפחיתה את הפיכת הפפסינוגן לפפסין (תהליך הנפסק ב-pH גבוה מ-5.5). נטרול החומצה משפר בצורה ניכרת את היצמדות הטסיות, ולכן את מנגנון הקרישה.
חולים אשר בטיפול אינטנסיבי אינם מפסיקים לדמם, ואינם מיוצבים מבחינה המודינמית, יש לנתח בדחיפות. בחולים שהפסיקו לדמם בטיפול שמרני, יש לבצע גסטרוסקופיה בתוך 12 שעות. בחולים שממשיכים לדמם ומועמדים לניתוח, יש לבצע את הגסטרוסקופיה לפני הניתוח, כדי למסור למנתח את המידע על מקור הדימום.
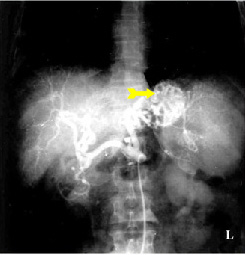
בחולים שמצבם הקשה כרוך בסיכון ניתוחי גבוה, ניתן לבצע ארטריוגרפיה ברירנית של עורקי הקיבה, לזהות את מקור הדימום, ודרך צנתר האנגיו להכניס חומר מטרש כמו דם קרוש, Histoacryl וכו', ולהזריקו לעורק כדי שיסתום את כלי הדם המדמם ויעצור את הדימום עד לייצוב החולה והכנתו לניתוח (תצלום 7.3).
בחולים מדממים אפשר גם לנסות לעצור את הדימום דרך האנדוסקופ, על-ידי קרישה (קואגולציה) בעזרת חום או לייזר, או הזרקת Epinephrine (Adrenaline) סביב הכיב.
טיפול שמרני בחולים הלוקים בחסימת השוער
החולים הלוקים בחסימת השוער סובלים מהקאות, מהתייבשות ובססת מטבולית עקב איבוד יוני מימן, כלור ואשלגן מהקיבה ואיבוד נוסף של אשלגן ומימן דרך הכליות. הטיפול חייב לכלול טיפול אינטנסיבי בנוזלים, בעיקר תמיסת מלחה (סליין) עם אשלגן כלוריד. אם אין אפשרות לתקן את הבססת (במקרים נדירים), יש להשתמש בחומצה הידרוכלורית.
ניקוז הקיבה בעזרת צנתר רחב ושטיפת הקיבה מרוקנים את הקיבה ומקטינים אותה, גורמים להפחתת הבצקת בדופנות ומפחיתים את עוצמת החסימה.
הפרשה מרתית המופיעה דרך הזונדה לאחר כמה ימים מעידה כי החולה סבל מחסימה חדה, הניתנת לטיפול שמרני. כדי לוודא שהשוער פתוח, יש לבצע גסטרוסקופיה, שממנה אפשר ללמוד גם על גורם החסימה.
חולים עם חסימות כרוניות, הם חולים ירודים וקטבוליים. בחולה במצב של תת-תזונה קשה יש לטפל בהזנה כוללנית תוך-ורידית (TPN), כהכנה לניתוח.
הוראות לטיפול כירורגי
התפתחויות בטיפול השמרני-תרופתי בכיב התריסריון גרמו לירידה דרמטית במספר החולים הזקוקים לניתוח עקב מחלה זו. אם בעבר 50% מהחולים נותחו עקב כשלון הטיפול השמרני, הגדרה זו נעלמה כמעט לגמרי וההוריות שנותרו לטיפול כירורגי בכיב קשורות לסבוכי הכיב. גם באלו ניכרת ירידה משמעותית במספר החולים שהזדקקו לניתוח כטיפול במחלת הכיב שלהם.
דימום
דימום הוא אחד הסיבוכים השכיחים והמסוכנים של הכיב הפפטי. 40% ממקרי המוות עקב כיב עיכולי (פפטי) קשורים לדימום מכיב. הדימומים המסיביים נובעים מעיכול כלי הדם הגדולים, כגון עורק הקיבה-תריסריון (Gastroduodenal artery), על-ידי חומצה ופפסין. אמנם ב-90% מהחולים הדימום נפסק עצמונית, אך הוא יכול לחזור שוב לאחר תקופה. הסתמנויותיו של הדימום:
- שחרה (מלנה) או דם אדום בדימומים חריפים מאוד.
- הקאה דמית (המטמזיס) מופיעה כאשר מקור הדימום הוא מעל לטריץ.
התמותה הניתוחית בזמן דימום אקטיבי גבוהה מאשר בניתוחים מתוכננים (אלקטיביים), ולכן יש להשתדל להפסיק את הדימום על-ידי טיפול שמרני, ורק לאחר ייצוב החולה לנתחו בצורה מתוכננת. כ-10% מהחולים המדממים יגיעו לניתוח דחוף, למרות הניסיונות לטיפול שמרני. הטיפול בחולה המדמם חייב להיות אינטנסיבי ולכלול עירוי מרכזי, צנתר לשלפוחית למדידת כמות השתן, צנתר לקיבה לשטיפות ולמדידות חוזרות של כמות הדימום וטיבו, ואבחון אנדוסקופי מהיר של מקור הדימום. ב-80% מהחולים המדממים אפשר לזהות את המקור באנדוסקופיה. השאלה הקשה היא מי מהחולים יזדקק לטיפול ניתוחי דחוף או לניתוח עוד באותו אשפוז.
- יש כמה הסתמנויות קליניות המסייעות בהערכת החולים המדממים. 4 ההסתמנויות הבאות מעידות על דימום קשה, ובחולים אלה יש לשקול ניתוח באותו אשפוז
- איבוד דם בכמות של 2000-1500 סמ"ק ב-24 השעות הראשונות (הערכה לפי סיפור החולה ותפוקת הזונדה).
- ירידה של ההמטוקריט לפחות מ-25 כעבור כמה שעות.
- איבוד דם הגורם לחולה להתעלף.
- איבוד דם הדורש החזרה של יותר מ-500 סמ"ק דם ל-8 שעות, כדי לשמור על סימני חיים יציבים, לאחר הייצוב הראשוני.
- הקריטריונים להיכללות החולה בקבוצות בעלות סיכון גבוה לדמם מחודש או שהדימום הראשון מסכן אותו
- הישנות הדימום באותו אשפוז (60% ידממו פעם נוספת — הוראה יחסית).
- ממצאים אנדוסקופיים מסייעים (כלי דם הנראה בבסיס הכיב, דימום פעיל וכו').
- גיל מבוגר ודימום מסיבי, עד כדי הסתבכות בהלם תת-נפחי (היפוולמי), באיסכמיה של שריר הלב, באירוע מוחי או בעיוורון.
- טיפול כרוני בתרופות יוצרות כיבים (אולצרוגניות) ודימום בעבר.
- מחלות מערכתיות קשות.
- סוג דם נדיר.
כל החולים המקיימים לפחות אחד מהקריטריונים שלעיל ינותחו לאחר הדימום, באותו אשפוז, שמא לא יוכלו לעמוד בניתוח דחוף לכשידממו שוב.
- גורמים נוספים המשפיעים על ההחלטה לנתח חולים מדממים הם
- מחלת טרשת עורקים (ארטריוסקלרוטית) בולטת.
- דפורמציה קשה שהתבררה בגסטרוסקופיה.
- דימום בזמן הגסטרוסקופיה.
- כלי דם הבולט לתוך הכיב.
- דימום שני באותו אשפוז.
- גיל מבוגר.
- סבל רב ממחלת הכיב ודימום.
בחולים הלוקים בטרשת עורקים בולטת, התכווצות כלי הדם לקויה ולכן הסיכוי שמנגנון זה יגרום להפסקת הדימום הוא קלוש. הצטלקות קשה סביב הכיב אינה מאפשרת לרקמה להתכווץ סביב הכיב, ופוגעת במנגנון הסיוע לעצירת הדימום. לכן חולים אלה נוטים להמשיך ולדמם. בעבודות רבות נמצא שחולים שבהם נראה כלי דם בולט בכיב, הם חולים שלא הפסיקו לדמם או חולים שבהם שכיחות הדימום השני באותו אשפוז היתה גבוהה. חולים הסובלים מכיב אחורי נוטים יותר לדימומים מאשר חולים בעלי כיבים קדמיים. עוצמת הדימום חזקה יותר בכיבים אחוריים. הניסיון לערות מנות רבות של דם לייצוב החולה בתקווה שיפסיק לדמם עצמונית הוא מסוכן, שכן טיפול כזה גורם לדילול גורמי הקרישה בדם, ומחמיר את מצב הדחק (סטרס) הקרדיו-וסקולרי של החולה.
התנקבות
התנקבות היא קטסטרופה בטנית, הנובעת מחדירת הכיב לכל עומק דופן התריסריון, מלווה בשפיכת תוכן התריסריון, הכולל מיצים מהמרה, ומהלבלב וחומצה, לחלל הצפקי. תוכן זה גורם לדלקת צפק כימית ולאיבוד נוזלים רב, הגורמים להתדרדרות החולה עד להלם היפוולמי. חולים אלה מתלוננים על כאבי בטן חדים, בעיקר ברום הבטן, ואולם הכאבים יכולים להופיע בכל הבטן, או אף בבטן ימנית תחתונה, והם הולכים ומחמירים. לעתים התמונה הקלינית אינה ברורה, בייחוד בחולים שבהם התרחשה התנקבות הכיב ל-Lesser sac. בחולים אלה אין תמונה צפקית ברורה.
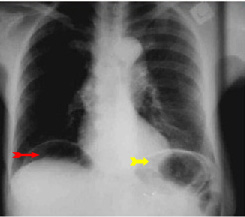
בצילום חזה ניתן לראות אוויר חופשי מתחת לסרעפות (תצלום 6.3). בבליעת בריום ניתן לראות דלף של חומר מחוץ לקיבה אם ההתנקבות היא אחור-צפקית (תצלום 7.3).
ההוריה לניתוח חולים עם התנקבות הכיב היא חד-משמעית. בדרך כלל הניתוח חייב להתבצע בדחיפות, בתוך שעות ספורות מתחילת הטיפול התומך.
חסימת השוער
יש שני סוגי חסימה של השוער:
- חסימה חריפה - בצקת עקב כיב פעיל גורמת לחסימת השוער. חסימה זו מגיבה היטב לטיפול שמרני על-ידי צנתר קיבתי במשך ימים מספר. חסימות חריפות חוזרות הן בבחינת הוריה לניתוח.
- חסימה כרונית - חסימה זו נגרמת על-ידי לייפת (הצטלקות) הכיב לאחר חודשים של חסימות חלקיות וגורמת להתרחבות ניכרת של הקיבה.
חולים הלוקים בחסימה כרונית של השוער הם המועמדים לניתוח. כדי לאמוד את דרגת החסימה, יש המבצעים מבחן על-ידי הזלפה של 750 סמ"ק תמיסת מלח (סליין), סגירת הצנתר ל-30 דקות, ולאחר מכן שאיבה דרך הצנתר. אם יוצאים יותר מ-400 סמ"ק של נוזל, יש חסימה מוחלטת. אם מבחן זה נשאר חיובי לאחר 3 ימים של טיפול שמרני, יש להציע לחולה טיפול ניתוחי.
כמה עבודות בשנים האחרונות הראו ש-50% מהחולים שאובחנה בהם חסימה חדה של השוער שחלפה, יופיעו בתוך שנתיים עם חסימה כרונית, ולכן אם יש מאורעות חוזרים של חסימה חדה חולפת, יש צורך לנתח את החולה.
חוסר תגובה לטיפול שמרני
ההגדרה של חוסר תגובה לטיפול שמרני קשה ביותר ואינה קבועה. חולים אלה בדרך כלל אינם נהנים מחייהם, אינם עובדים ואינם מתפקדים. הם אינם מגיבים לטיפול תרופתי, ולעתים אף מסתבכים בדימומים ובהתנקבויות. ההגדרה המובהקת של חוסר תגובה לטיפול שמרני היא: ניסיון טיפולי תרופתי במגוון התרופות החדשות והיעילות בטיפול בכיב במשך 6 חודשים לפחות, ושלאחריו מתמידים סימני הכיב והחולה נותר בסבלו.
חולים הכלולים בהגדרה של כישלון הטיפול השמרני הם אלה:
- החוזרים כמה פעמים בשנה עם תסמונת הכיב למרות הטיפול.
- הסובלים מכיב אחורי עמוק הנמצא בגסטרוסקופיה עם קליניקה מתאימה.
- הנזקקים לניתוח.
- הסובלים ממחלות נלוות.
- הלוקים בתסמינים של כיב התריסריון ומחלות כירורגיות אחרות נוספות הדורשות טיפול כירורגי (אבני כיס מרה, בקע סרעפתי וכו').
- שאינם מתפקדים ואינם עובדים או נעדרים רבות מעבודתם עקב תסמיני הכיב.
הוריה זו שהייתה בעבר הוריה שכיחה לטיפול כירורגי בכיב בתריסריון הפכה בשנים האחרונות לנדירה ביותר.
הטיפול הכירורגי בכיב
מטרת הטיפול הכירורגי היא להפחית את הפרשת החומצה בקיבה. לצורך זה תוארו כמה ניתוחים:
כריתת קיבה תת-שלמה
כדי להפחית את הפרשת החומצה מהקיבה יש לסלק את הרקמה המפרישה חומצה, כלומר את מסת התאים הפריאטליים. לצורך משימה זו כורתים 75% מהקיבה. כריתה זו כרוכה בירידה של 60%-80% מהפרשת החומצה בתגובה ל-Pentagastrin.
הגישה לניתוח זה היא דרך חתך אמצעי בבטן העליונה. לאחר פתיחת הבטן וסיור, כולל זיהוי הכיב ומיקומו, מפרידים את הקיבה מרצועת הקיבה והמעי הגס (הליגמנט הגסטרוקולי) ורצועת הקיבה והכבד (הליגמנט הגסטרוהפטי), וקושרים את כלי הדם הגדולים של הקיבה (Right gastric artery, Left gastric artery, Left gastroepiploic artery). גדם הקיבה שיישאר ניזון מה-Left gastroepiploic artery וה-Short gastric artery ומכלי הדם היורדים מהוושט. לאחר הפרדת הקיבה מנתקים אותה מהתריסריון. יש להקפיד על ביצוע הכריתה מעבר לשוער (פילורוס), שכן השארת רירית של האנטרום, אשר אינה נחשפת לחומצה (אצידיפיקציה) גורמת להפרשת יתר של גסטרין, וזה גורם להפרשת יתר של חומצה, ולפיכך לכיבים חוזרים בקו ההשקה בין הקיבה למעי.
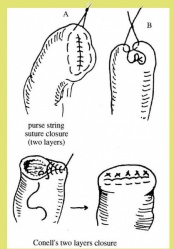
הטכניקה לסגירת גדם התריסריון יכולה להיות ידנית כמתואר באיור 3. 5 א או בעזרת מכלב היוצר שתי שורות של סיכות לרוחב התריסריון. מתוארת באיור 7.3 א. יש לציין, שלעתים יש קושי טכני לסגור את התריסריון. לעתים יש צורך לסגור את הגדם על נקז המוכנס לתריסריון (Tube duodenostomy), כדי למנוע לחץ על קו התפרים, ובכך למנוע את התבקעות קו התפרים.
כריתת הקיבה מתבצעת מתחת לגובה פי הקיבה (הקרדיה) במאונך לעקומה הקטנה. בשיטה זו נכרתים כ-75% מהקיבה. הרחקת כמות כזו של רקמת קיבה יש בה כדי להפחית את הפרשת החומצה במידה ניכרת (80%-60%). שחזור המשך הקיבה המעי יכול להתבצע בשיטות שונות המאוירות בהמשך הפרק (איור 6.3 ).
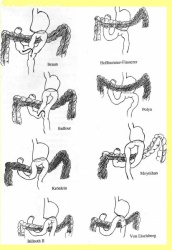
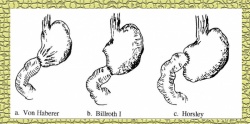
עקרונית, ניתן לבצע השקה חוזרת בין התריסריון לקיבה (Billroth 1 - Gastrodoudenostomy - ואחרים) (איור 7.3, 8.3), או השקה בין לולאת מעי הסמוכה לטריץ לבין גדם הקיבה (Billroth 2 - Gastroenterostomy - ואחרים). השקה זו יכולה להתבצע לפני הכרכשת הרוחבית (Antecolic), או מאחורי הכרכשת (Retrocolic) (איור 6.3).
הגישה מאחורי המעי הגס (רטרוקולית) בניתוחי כיב עדיפה, מאחר שהיא קשורה בפחות סיבוכים לאחר הניתוח. יש הטוענים שהשכיחות של כיב חוזר, לאחר השקת קיבה לתריסריון (גסטרודאודנוסטומיה - Billroth 1) היא כפולה מזו שלאחר השקת קיבה למעי (גסטרואנטרוסטומיה - Billroth 2), ולכן האחרונה מקובלת יותר.
ניתוח זה כרוך בשיעור תמותה מדווח של 8%-0.5%, בממוצע 4%-3%, וכן בשיעור של 50%-30% סיבוכים בתר-ניתוחיים. לכן פחת השימוש בניתוחים אלה לטיפול בכיב התריסריון, וכמעט פסק לגמרי, ובמקומם משתמשים בניתוחים שונים לכריתת הוואגוסים (עצבי התועה).
ואגוטומיה (כריתת עצב התועה) וניקוז
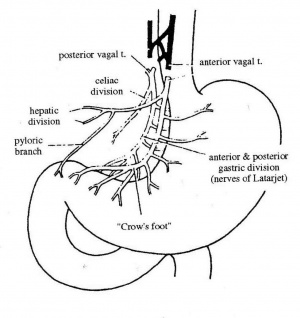
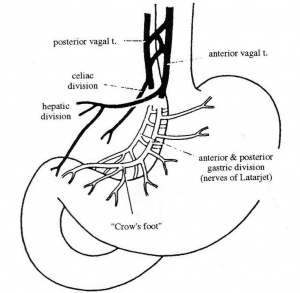
הוואגוטומיה מקטינה את הפרשת האצטילכולין בקיבה, ועל-ידי כך מקטינה את הפרשת החומצה ב-70%-60%. הוואגוסים תוארו מבחינה אנטומית בתחילת פרק זה.
ואגוטומיה שלמה (Truncal vagotomy)
הגישה לביצוע הוואגוטומיה השלמה היא דרך חתך אמצעי עליון. כדי לחשוף את ענפי עצב התועה על הוושט יש לשחרר את ה- Triangular ligament השמאלי של הכבד, מכיוון שקצה האונה השמאלית של הכבד מכסה על ההיאטוס והקטע העליון של הוושט הבטני. לאחר דחיקת קצה האונה השמאלית ימינה, פותחים את הצפק שבין הוושט לכבד, במטרה לחשוף את הוושט. בשלב זה מותחים את הקיבה כלפי מטה, ובתוך כך גם את הוושט, ומעבירים את האצבע על פני הדופן הקדמית של הוושט. הענף הקדמי של עצב התועה נמוש כחבל דק על פני הדופן הקדמית של הוושט. מבודדים אותו, ולאחר מכן כורתים אותו קרוב להיאטוס. את הענף האחורי מזהים בשיטה דומה, אלא שהפעם האצבע מוכנסת מימין לוושט או מאחורי הוושט. הענף האחורי נמוש כחבל עבה יותר מהקדמי. לאחר חשיפתו, נכרת הענף האחורי של עצב התועה. שני הענפים נשלחים לזיהוי היסטולוגי (איור 9.3).
עקב שינויים אנטומיים במיקומו לא תמיד קל למצוא את הענף האחורי. לפעמים מוצאים את הענף האחורי חבוי במעטפת החיצונית (אדונטיציה) של הוותין (Aorta). כישלון הוואגוטומיה נובע מוואגוטומיה חלקית, כלומר כישלון כריתת אחד הענפים עקב זיהוי מוטעה, קושי אנטומי במציאת אחד הענפים, או קיומם של ענפים קטנים, המעצבבים את הקיבה, היוצאים מעצב התועה מעל גובה הכריתה. ככל שהוואגוטומיה מתבצעת קרוב יותר להיאטוס, כך הסיכוי לוואגוטומיה חלקית קטן יותר, מכיוון שהתפצלויות בגובה זה נדירות יותר.
ואגוטומיה ברירנית (Selective vagotomy)
כדי להקטין את שכיחות תופעות הלוואי הקשורות בכריתת ענפי עצב התועה, כגון תסמונת ההצפה, שלשולים ואבני כיס מרה, הוצע לבצע את הוואגוטומיה כך שהענפים היוצאים מעצב התועה לקיבה ייכרתו, ואילו הענפים למקלעת הכבדית ולמקלעת הצליאק יישארו.
טכנית, הגישה דומה לזו של הוואגוטומיה השלמה. בניתוח זה חושפים את הענף הקדמי של עצב התועה ומזהים את הענף המגיע לכבד, מתחת לעלה הקדמי של הצפק שבין הוושט לכבד, בגובה החיבור הוושטי-קיבתי (אזופגוגסטרי). את הענף הקדמי כורתים מתחת ליציאת הענף הכבדי. שיטה דומה ננקטת לגבי הענף האחורי, והוא נכרת מתחת ליציאת הענף לצליאק. לאחר מכן יש לכרות את הענפים המגיעים לקרדיה ולפונדוס היוצאים מעל גובה כריתת עצב התועה (איור 10.3).
עבודות שפורסמו בשנים האחרונות לא הוכיחו את העדיפות התיאורטית של שיטה זו. שיעור תופעות הלוואי בחולים שבוצעה בהם כריתה ברירנית של ענפי עצב התועה אינו שונה מהשיעור באלה שבוצעה בהם כריתה שלמה.
בשני ניתוחים אלה כורתים גם את הענפים המעצבבים את שוער הקיבה, ולכן ב-70%-60% מהחולים, לאחר כריתת עצב התועה, השוער נותר מכווץ ואינו נפתח. כהשלמה לניתוחים אלה, יש להוסיף ניתוח לניקוז הקיבה, שבעצם אינו קשור לטיפול בכיב עצמו, אלא הוא בבחינת מענה לסיבוך של טיפול בוואגוטומיה.
הוצעו כמה שיטות לניקוז הקיבה:
1. Gastroenterostomy - הגסטרואנטרוסטומיה (השקת קיבה למעי) היתה אחת השיטות הראשונות שתוארו. בשיטה זו מבצעים השקה בין הקיבה ללולאת מעי דק הקרובה לטריץ. מבצעים את ההשקה במקום הנמוך ביותר בקיבה, כדי לנצל את כוח הכובד כמכשיר עזר בניקוז הקיבה. הסיבה לכך נעוצה בפגיעה בתנועתיות הקיבה הנובעת מהוואגוטומיה. יש מנתחים המעדיפים לבצע את ההשקה באזור האנטרום כדי למנוע עמדון של המעי (סטזיס אנטרלי), ולכן מבצעים את ההשקה בקרבת השוער. באופן עקרוני, ההשקה מתבצעת מאחורי הכרכשת (Colon) הרוחבית (Retrocolic) (איור 11.3).
2. Pyloroplasty - השיטה המקובלת יותר לביצוע ניקוז של הקיבה. תוארו כמה שיטות לביצוע הניתוח:
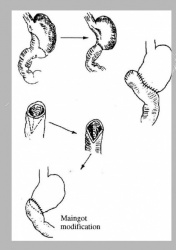
2.1 טכניקה אחת היא לפי Heinecke- Mickulicz, ומבוססת על חיתוך השוער לרוחבו לכל עובי הדופן. פעולה זו מבטלת למעשה את תפקוד השוער. כדי לא להצר אותו שוב, נעשה שיחזור על ידי תפירת הפתח הנוצר לאורכו (איור 12.3) . התפירה מחדש מתבצעת בשתי שכבות או בשכבה אחת לפי Weinberg. לאחר הניתוח השוער נותר פתוח, ונוזל הקיבה והמזון עוברים באופן חופשי לתריסריון.
2.2 פילורופלסטיקה לפי Finney היא למעשה גסטרודאודנוסטומיה דרך השוער. בניתוח זה, לאחר תפירת התריסריון לקיבה מגובה השוער ומטה, לאורך כ- 7 ס"מ, חותכים את הדופן מעל קו התפרים בצורת פרסה כשזרוע אחת שלה בקיבה והאחרת בתריסריון (איור 13.3). לאחר מכן תופרים את הדופן הקדמית של הקיבה לתריסריון. שיטה זו יוצרת פתח רחב בין הקיבה לתריסריון, המאפשרת מעבר חופשי ביניהם.
2.3 שיטת הניקוז לפי Jaboulay היא גסטרודאודנוסטומיה ממש בין החלק הראשון של התריסריון לבין הקיבה, לפני השוער, מבלי לפגוע השוער. שיטה זו מקובלת פחות (איור 14.3)
ואגוטומיה על-ברירנית (Supra-selective vagotomy)
אחת הסיבות לשיעור הגבוה יחסית של תופעות לוואי שלאחר ואגוטומיה וניקוז היא הרס מנגנון השוער. קביעה זו הביאה לסברה, שניתן לבצע ניתוח פיזיולוגי הכרוך בהפחתה בהפרשת החומצה ובתוך כך לשמור על האנטומיה של הקיבה.
לניתוח זה שמות אחדים: Supra-selective vagotomy, Parietal cell vagotomy, Proximal gastric vagotomy.
העיקרון בניתוח זה הוא כריתה של סיבי הוואגוס המעצבבים את הפונדוס וגוף הקיבה, שבהם נמצאת הרקמה המפרישה חומצה, והשארת העצבוב לאנטרום ולשוער. חשוב לשמר את עצבוב האנטרום, מכיוון שיש תלות פיזיולוגית בין התכווצות האנטרום לפתיחת השוער. הגישה הניתוחית זהה לזו של הוואגוטומיה השלמה. לאחר פתיחת הבטן, מזהים את העצב על-שם לטרזיה ואת רגל העורב שבסופו. החל מהענף האחרון של אותה רגל-עורב, מפרידים את רצועת הקיבה והכבד (הליגמנט ההפטוגסטרי) מעל העקומה הקטנה של הקיבה, ובתוך כך, כורתים את הסיבים המגיעים מהעצב על-שם לטרזיה, הקדמי והאחורי, לגוף הקיבה ולפונדוס (קרקעית הקיבה). באזור הוושטי-קיבתי (אזופגוגסטרי) ממשיכים לכרות את סיבי הוואגוס לאורך הוושט עד לגובה של כ-7 ס"מ מהחיבור הוושטי-קיבתי(איור 15.3).
בסיום הניתוח העקומה הקטנה והוושט חשופים. בזמן הפרדת הוואגוס האחורי יש להקפיד לנתק את ה-Criminal nerve of Grazi, היוצא כ-2 ס"מ מעל החיבור האזופגוגסטרי ומעצבב את כיפת הקיבה. אין צורך להוסיף ניקוז לקיבה שכן העצבוב לשוער נשאר. זו הסיבה ששכיחות תופעות הלוואי לאחר ניתוח זה היא נמוכה יחסית לשיטות הקודמות שתוארו.
ניתוחים לכריתת עצבי התועה לסוגיהם השונים עם חיתוך שריר השוער (פילורומיוטומיה) לניקוז הקיבה תוארו גם בגישה לפרוסקופית, אולם מיעוט ההוריות לניתוח ולכן מיעוט הניתוחים, לא מאפשרת לדווח על ניסיון מצטבר אלא בקליניקות מיוחדות.
ואגוטומיה ואנטרקטומיה (כריתת עצב התועה וכריתת מערת השוער - Vagotomy and Antrectomy)
הפחתת הפרשות החומצה לאחר ואגוטומיה היא בשיעור של כ-60%. הפחתה זו בהפרשת החומצה בחולים בעלי הפרשה מוגברת מאוד של חומצה, תשאיר אותם עם ערכי חומצה גבוהים יחסית, וסיכון של כיבים חוזרים. בחולים אלה יש הממליצים לנקוט שיטה ניתוחית, אשר תפחית במידה רבה יותר את הפרשת החומצה, על-ידי ביצוע ואגוטומיה ובנוסף כריתת האנטרום, כדי לסלק את המקור להפרשת הגסטרין. בניתוח זה מחסלים את רוב המערכת המגרה הפרשת חומצה. השיטה הניתוחית זהה לזו שתוארה בוואגוטומיה שלמה ובכריתת הקיבה, אבל באנטרקטומיה כריתת הקיבה היא מוגבלת יותר, וכוללת את קטע הקיבה מהאינסיסורה אנגולריס, בקו היורד כלפי מטה בזווית של 45 מעלות (איור 6.3). השחזור יכול להתבצע על-ידי גסטרודאודנוסטומיה או גסטרואנטרוסטומיה, בשיטות שכבר תוארו. יש מנתחים המשלבים כריתה ברירנית של ענפי עצב התועה עם אנטרקטומיה.
בשנים האחרונות הוכנסו לשימוש קליני שיטות להערכה של מידת הסיכון הניתוחי בחולים המועמדים לטיפול כירורגי בהתחשב במצבם הפיזיולוגי ובגילם (Scoring system). החולים הלוקים בדימום חד או בהתנקבות הכיב נחלקים ל-3 קבוצות:
- חולים בדרגת סיכון נמוכה, בלא עבר עם מחלות ובמצב פיזיולוגי טוב, שבהם הסיכון הניתוחי הוא קטן.
- חולים בדרגת סיכון בינונית, שבהם יש הפרעה תפקודית באחת המערכות (לב וכלי דם, כליות, נשימה וכו') ושבהם הסיכון בניתוח הוא גבוה יותר.
- חולים הלוקים בהפרעה תפקודית ניכרת, בני גיל מתקדם. אלה חולים אשר מצבם קריטי וסיכוייהם לעמוד בניתוח אינם גבוהים ובהם יש לבצע פעולות להצלת חיים בלבד.
הגישה הניתוחית לחולים אלה צריכה להתחשב בדרגת הסיכון שבה נתון החולה. יש להבהיר לחולה ולמשפחתו מה רמת הסיכון הכרוכה בהתערבות כירורגית לעומת רמת הסיכון בלא התערבות שכזו, ולשתפם בהחלטה על סוג הטיפול שיקבל החולה.
טיפול כירורגי בחולה מדמם
בחולים הלוקים בדימום קשה מכיב עיכולי יש לבצע תחילה גסטרוסקופיה אבחנתית ועצירת דמם (המוסטזה) אנדוסקופית. אם דרך זו לא הועילה להפסקת הדימום, יש לנקוט ניתוח חירום להפסקת הדימום.
תחילה יש לפתוח את התריסריון, לזהות את מקור הדימום ולתפור את הכיב. גם במקרים שבהם הכיב אינו מדמם בזמן הניתוח, יש לתופרו. בחולים הלוקים בכיב נמוך (לאחר בצל התריסריון - פוסטבולברי) יש להקפיד שהתפרים יהיו שטחיים כדי שלא לפגוע בצינור המרה המשותף העובר בסמוך. בגמר תפירת הכיב יש ללחוץ על כיס המרה ולוודא שמרה יוצאת מהפפילה, כדי לוודא שצינור המרה לא נתפר.
אם מצבו של החולה מאפשר זאת, יש להמשיך בניתוח דפיניטיבי. בחולים בדרגת סיכון נמוכה אפשר לבצע ואגוטומיה על-ברירנית. במקרים אלה יש לבצע מראש דאודנוטומיה שלא דרך השוער. בחולים אלה או בבעלי סיכון בינוני אפשר לבצע דאודנוטומיה דרך השוער ולתקנו בצורת פילורופלסטיקה לאחר תפירת בסיס בכיב המדמם, ולאחר מכן להוסיף ואגוטומיה שלמה או ברירנית. בחולים במצב קשה יש לשקול ביצוע תפירת הכיב בלבד ולטפל בהם לאחר מכן על-ידי חוסמי H2 או Omeprazole. כריתת קיבה במצבים אלה היא ניתוח מיותר הכרוך בסיכון גבוה. בחולים מדממים הלוקים בהיצרות השוער או בכיב בשוער או בחולים שבהם יש קושי טכני בביצוע פילורופלסטיקה, רצוי להוסיף גסטרואנטרוסטומיה כדי לשפר את ניקוז הקיבה. בחולים המדממים מכיב פפטי בקיבה אפשר לעצור את הדימום על-ידי פתיחת קיבה קדמית ותפירת הכיב. בחולים בסיכון קל או בינוני ניתן לבצע ניתוח דפיניטיבי בהתאם למקום הכיב - כריתת קיבה הכוללת את הכיב, או כריתת מקום הכיב, ואגוטומיה וניקוז. בחולים במצב קשה ניתן להסתפק בתפירת הכיב. בחולים הסובלים מכיב שבהם אין אפשרות לזהות בניתוח את מקור הדימום בתריסריון או בקיבה יש לבצע ואגוטומיה וניקוז באחת השיטות שהוזכרו לעיל.
כיום, כאשר טיפול תרופתי נותן מענה טוב למחלת הכיב ברוב החולים וניתן להוריד את הפרשת החומצה בצורה משמעותית בעזרת תרופות, התעורר הספק בצורך לבצע ואגוטומיה כחלק מהטיפול בכיב המדמם. אין ספק שחולים שהדימום מהווה תסמין ראשון למחלת הכיב שלהם לא זקוקים לוואגוטומיה. לעומתם, בחולים עם מחלה כרונית קשה שלא הגיבו לטיפול בצורה טובה יש לשקול ביצוע ואגוטומיה. רוב המנתחים כיום אינם מוסיפים ואגוטומיה לטיפול הכירורגי בחולה המדמם.
טיפול כירורגי בהתנקבות הכיב
בחולים שבהם ההוריה לניתוח היא התנקבות הכיב, אפשר לבצע בניתוח סגירה של הנקב על-ידי תפירתו וכיסויו באומנטום (ניתוח על-שם גרהם - Grahm), או טיפול דפיניטיבי בכיב, על-ידי ואגוטומיה ופילורופלסטיקה העוברת דרך הכיב, ובתוך כך כריתת הכיב. במקרים קשים, שבהם יש זיהום מפושט, ודופן התריסריון נקרעת בקלות, כגון בחולים שהגיעו מאוחר לטיפול רפואי, יבוצע הניתוח על-שם גרהם. חולים שבהם ההתנקבות היתה התסמין הראשון לכיב התריסריון, ונותחו בניתוח על-שם גרהם - 72% מהם יישארו אי-תסמיניים (אסימפטומטיים) לאחר הניתוח, לעומת 23% מהחולים שבהם ההתנקבות לוותה בתמונה קלינית קודמת של כיב. לכן בחולים אי-תסמיניים אפשר לבצע את הניתוח על-שם גרהם, בלא צורך בוואגוטומיה. חולים הלוקים בהתנקבות הכיב שלא טופלו במשך כ-6 שעות, ולהם זיהום ניכר בבטן ינותחו אף הם בניתוח על-שם גרהם.
לאחר גמר הטיפול בכיב חייבים לשטוף את החלל הצפקי, כדי לסלק ממנו את הזיהום שנבע מחדירת הנוזלים ממערכת העיכול בזמן ההתנקבות. במצבים קשים, יש לבצע שטיפה ממושכת של הצפק, במשך 48-24 שעות דרך נקזים (ר' פרק "הצפק").
בחולים במצב קריטי יש מקום לנסות טיפול שמרני. להשלמת הבירור ניתן לבצע הדמיה בעזרת חומר ניגוד שנספג. אם לא הודגמה התנקבות חופשית לחלל הצפק, יטופל החולה באנטיביוטיקה, בניקוז הקיבה על-ידי זונדה ובחוסמי H2. ההוריה לניתוח קיימת בחולים שבהם הודגם דלף פעיל לחלל הצפק או בכאלה שלא הגיבו לטיפול שמרני.
בחולים הלוקים בהתנקבות של כיב ענק הסגירה הפשוטה אינה אפשרית, ולכן יש צורך לשקול כריתת האנטרום וואגוטומיה. בנוכחות כיב ענק סגירת התריסריון יכולה להיות בעייתית, ולכן ניתן להוסיף דאודנוסטומיה צדדית או היוצאת דרך קו התפרים, כפי שתואר לעיל. פתרון אחר הוא לבצע השקה לפי בילרות' 1 עם גדם התריסריון הבריא.
טיפול ניתוחי בחסימת השוער
בחולים הלוקים בחסימת השוער, הקיבה היא רפה (אטונית) ומכילה כמות גדולה של שרידי אוכל, ולכן יש לנקז את הקיבה לפני הניתוח. יש חשיבות להכנת החולה לפני הניתוח על-ידי שאיבה טובה של תוכן הקיבה, מכיוון שרקמת קיבה בצקתית, כזו המצויה בחולה הלוקה בחסימה, נרפאת שלא כהלכה.
בחולים שבהם ההוריה לניתוח היא חסימת השוער, ניתן למצוא בדרך כלל בניתוח קיבה אטונית גדולה מאוד. הדבר נכון במיוחד בחולים הלוקים בחסימה ממושכת, שקיבתם נוקזה לפרק זמן קצר לפני הניתוח. הניתוח כולל ואגוטומיה, ואחת משיטות הניקוז: גסטרואנטרוסטומיה, אנטרקטומיה או פילורופלסטיקה. מכיוון שבמקצת החולים הקיבה אטונית וגדולה, יש מנתחים המעדיפים לבצע אנטרקטומיה או גסטרואנטרוסטומיה כשיטת ניקוז שגרתית בחולים אלה. בספרות הופיעו דיווחים על הרחבות מכניות של השוער וכריתה על-ברירנית של ענפי עצב התועה.
ניתוחים שכללו כריתה על-ברירנית של ענפי עצב התועה והרחבות של השוער הניבו תוצאות לקויות, ולכן הוחלפו בכריתה על-ברירנית של ענפי עצב התועה ובפילורופלסטיקה. יתרון הניתוח הזה הוא בהיותו משמר את פעולת האנטרום, ולכן מקטין את שכיחות תופעות הלוואי. בחולים בעלי קיבה אטונית מאוד כריתת הקיבה היא הניתוח המועדף.
| שיעור חזרת כיב הקיבה | שיעור התחלואה | שיעור התמותה הניתוחית | |
|---|---|---|---|
| כריתה על-ברירנית של עצב התועה | 0.5% | 5% | 20%-15% |
| כריתת ענפי עצב התועה וניקוז | 1% | 10% | 7% |
| כריתת ענפי עצב התועה ואנטרקטומיה | 2% | 12% | 1% |
| כריתת קיבה | 3% | 15% | 3% |
יש לזכור שחולים לאחר ניתוח זקוקים להמשך שאיבה במשך כמה ימים, עד אשר הקיבה רוכשת שוב את הטונוס התקין ומתרוקנת היטב. יש מנתחים הממליצים לבצע גסטרוסטומיה בכל חולה שנותח עקב חסימת השוער.
הערכת שלמות הוואגוטומיה
בחולים שבהם כריתת ענפי העצב התועה אינה שלמה, שכיחות הכיבים החוזרים גבוהה.
מבחן הולנדר
המבחן על-שם הולנדר נועד לאבחן בחולים ואגוטומיה חלקית. מבחן זה מבוסס על התגובה הוואגאלית הנגרמת עקב היפוגליקמיה. במבחן זה נותנים לחולה Insulin (במינון של יחידה לק"ג), עד להשגת תמונה קלינית של היפוגליקמיה, ומודדים את כמות החומצה המופרשת בעקבות תגובה זו, על-ידי שאיבה דרך זונדה.
בנוכחות לפחות 3 מהממצאים הבאים, ייקבע מבחן חיובי:
- עליית נפח של 10 מ"ל ויותר בכל 30 דקות.
- הפרשה בסיסית של 2 מא"ק/ל'/שעה.
- הפרשה של 20 מא"ק/ל' כל 30 דקות.
- עלייה מוקדמת (בשעה הראשונה).
- הפרשה הגדולה פי 2 מההפרשה הבסיסית.
כ-25%-10% מהחולים עם מבחן חיובי יפתחו כיב חוזר. ל-60% מהחולים שפיתחו כיב חוזר - המבחן חיובי. 2% מהחולים עם מבחן שלילי יפתחו כיב חוזר. אין לבצע את המבחן בחולים הלוקים במחלות קרדיווסקולריות, בחולים זקנים או בחולים לאחר אירוע מוחי (CVA).
מבחן אכילה מדומה - Sham-Feeding test
מבחן אחר, שנכנס לשימוש בשנים האחרונות והפך למבחן סטנדרטי בכמה מרכזים, הוא Sham-Feeding test. החולה מתבקש ללעוס ארוחה סטנדרטית בלי לבלוע אותה. האכילה מגרה את עצב התועה, ואם אינו נכרת בשלמותו, הוא יגרום להפרשת חומצה, אותה ניתן לאסוף ולמדוד בעזרת צנתר שממקמים בקיבה.
ראו גם
- לנושא הקודם: פיזיולוגיה של הקיבה והתריסריון - Gastric and duodenal physiology
- לנושא הבא: כיב התריסריון - Duodenal ulcer
- לתוכן העניינים של הפרק
- לתוכן העניינים של הספר
- לפרק הקודם: כירורגיה של הצפק
- לפרק הבא: כירורגיה של המעי הדק
המידע שבדף זה נכתב על ידי ד"ר צבי קויפמן, מומחה בכירורגיה, מנהל היחידה לבריאות השד, מרכז רפואי מאיר, כפר סבא


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק