הבדלים בין גרסאות בדף "תסמונת גדילת יתר - Overgrowth syndrome"
ביאנקה סטרלצין (שיחה | תרומות) |
ביאנקה סטרלצין (שיחה | תרומות) |
||
| שורה 20: | שורה 20: | ||
בעשור האחרון הצטבר מידע המאפשר לנו לזהות את הגורמים הגנטיים לחלק מהמצבים של גדילת יתר. מידע זה נותן בידינו כלים אבחנתיים מצד אחד ומאפשר הבנה מעמיקה יותר של התהליכים העומדים בבסיס הפתולוגי של מצבים אלה, מצד שני. אין ספק, שהבנת התהליכים האלה תאפשר, בסופו של דבר, טיפול טוב יותר במטופלים. למשל, הומוציסטינוריה (Homocystinuria) היא מחלה נסגנית (Recessive) הנגרמת בשל חסר אנזימטי של ציסטתיון בתא סינתאז (Cystathionin beta-synthase) וקשורה בקומה גבוהה ובמראה מרפנואידי (Marphanoid) (וכן במעורבות רב מערכתית). לאחרונה נמצא כי עלייה ברמת [[הומוציסטאין]] אצל מטופלים עם הומוציסטינוריה גורמת חיזור של קשרי דיסולפיד באזור ה-cbEGF של הגן פיברילין 1 (Fibrillin 1) הקשור ב[[תסמונת מרפן]]. לנוכח ההבנה של התהליכים המולקולריים במחלה זו, קיימות אפשרויות טיפוליות הכוללות מתן [[Betaine]], מתן [[פירידוקסין]] (ויטמין B6) והגבלת כמות המתיונין (Methionine) ב[[דיאטה]]. בעבודה מבוקרת נמצא הבדל בגובה הממוצע בין הילדים המטפולים לאלה שאינם מטופלים . | בעשור האחרון הצטבר מידע המאפשר לנו לזהות את הגורמים הגנטיים לחלק מהמצבים של גדילת יתר. מידע זה נותן בידינו כלים אבחנתיים מצד אחד ומאפשר הבנה מעמיקה יותר של התהליכים העומדים בבסיס הפתולוגי של מצבים אלה, מצד שני. אין ספק, שהבנת התהליכים האלה תאפשר, בסופו של דבר, טיפול טוב יותר במטופלים. למשל, הומוציסטינוריה (Homocystinuria) היא מחלה נסגנית (Recessive) הנגרמת בשל חסר אנזימטי של ציסטתיון בתא סינתאז (Cystathionin beta-synthase) וקשורה בקומה גבוהה ובמראה מרפנואידי (Marphanoid) (וכן במעורבות רב מערכתית). לאחרונה נמצא כי עלייה ברמת [[הומוציסטאין]] אצל מטופלים עם הומוציסטינוריה גורמת חיזור של קשרי דיסולפיד באזור ה-cbEGF של הגן פיברילין 1 (Fibrillin 1) הקשור ב[[תסמונת מרפן]]. לנוכח ההבנה של התהליכים המולקולריים במחלה זו, קיימות אפשרויות טיפוליות הכוללות מתן [[Betaine]], מתן [[פירידוקסין]] (ויטמין B6) והגבלת כמות המתיונין (Methionine) ב[[דיאטה]]. בעבודה מבוקרת נמצא הבדל בגובה הממוצע בין הילדים המטפולים לאלה שאינם מטופלים . | ||
| − | + | גילוי הבסיס הגנטי של התסמונות השונות מקנה הבנה טובה יותר של התהליכים הביולוגיים התורמים לגדילה התקינה והבלתי תקינה של השלד, מאפשר מעקב נכון ולעתים גם טיפולים מתאימים יותר למטופלים ומקנה את האפשרות לתת ייעוץ גנטי מדויק למשפחות. לא תמיד האבחון המולקולרי (ברמת הגן) נותן כלים נוחים לסיווג. למשל, מוטציה בגן FGFR3 גורמת, מצד אחד, לסוגים שונים של [[גמדות]]/קומה נמוכה (Achondroplasia או Hypochondroplasia) ומצד שני, מוטציה באותו גן באזור שונה ובמנגנון אחר גורמת לתסמונת גדילת יתר CATSHL {{כ}} (Camptodactyly, Tall stature, and Hearing Loss). כמו כן, לעתים יש יותר מגן אחד הגורם לאותו חזותי (Phenotype), מצב המוכר כאי אחידות גנטית. למשל, תסמונת מרפן יכולה להיות קשורה בגן FBN1, אבל גם בגנים TGFBR2 ו-TGFBR1. | |
| − | + | יש מקום לחשוב על בעיות אנדוקריניות באבחנה מבדלת של קומה גבוהה וגדילה מואצת. בנוסף, עוברים או תינוקות גדולים נולדים לאם סוכרתית לא מאוזנת במהלך ההיריון. {{הפניה לערך מורחב|סוכרת הריון – Gestational diabetes}} | |
== קליניקה == | == קליניקה == | ||
גרסה מ־20:06, 20 באוקטובר 2012
ערך זה נמצא בבדיקה ועריכה על ידי מערכת ויקירפואה, וייתכן כי הוא לא ערוך ומוגה.
| תסמונuת גדילת יתר | ||
|---|---|---|
| Overgrowth syndromes | ||
| 250px | ||
סינדרום Sotos
| ||
| יוצר הערך | ד"ר חנה וינקלר, ד"ר עמיהוד זינגר 
|
|
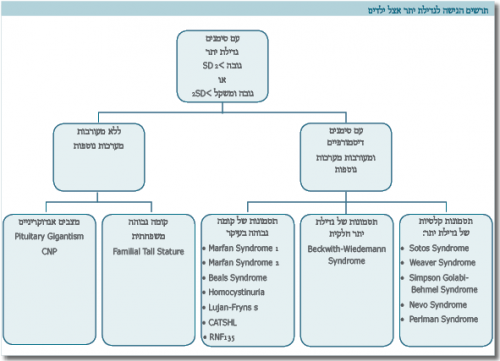
תסמונות של גדילת יתר בילדים הן קבוצה לא אחידה ומגוונת של מצבים המאופיינים בגדילה של איברי גוף או בגדילה כללית מעל 2 סטיות תקן לגיל. קבוצת המחלות הקשורה בגדילת יתר מגוונת הן מבחינת המעורבות הנוספת של מערכות גוף פגועות והן מבחינה הגנים המעורבים. עם ההתקדמות בתחום הגנטי וגילוי הגנים השונים ניתנת כיום האפשרות לאישור מדויק כאשר קיים חשד קליני לאחת התסמונות. הבנת התהליכים הגנטיים והביולוגיים המשפיעים על התמונה הקלינית, היא כל העת גורם לשינוי בגישה למטופלים. ייתכן כי בעתיד הבנה זו תאפשר מתן טיפולים גנטיים או רפואיים טובים יותר למטופלים אלה.
אפידמיולוגיה
אטיולוגיה
הגדילה לגובה היא תהליך מורכב התלוי בגורמים גנטיים, תזונתיים, הורמונליים וסביבתיים (כמו מחלות מתמשכות, טיפולי קרינה וכד'). שינוי באחד הגורמים המשפיעים על הגדילה, עלול לגרום האטה בגדילה וקומה נמוכה. נדיר יותר ששינוי כזה יגרום גדילה מואצת. זיהוי של מצבים של גדילה מואצת חשוב לא פחות מזיהוי של מצבים של האטה בגדילה, כי הוא קשור לעתים קרובות במעורבות של מערכות גוף שונות, ומחייב התייחסות טיפולית וייעוץ מתאים של הרופא המטפל בנוגע לפרוגנוזה ולהשלכות על המשפחה.
בעשור האחרון הצטבר מידע המאפשר לנו לזהות את הגורמים הגנטיים לחלק מהמצבים של גדילת יתר. מידע זה נותן בידינו כלים אבחנתיים מצד אחד ומאפשר הבנה מעמיקה יותר של התהליכים העומדים בבסיס הפתולוגי של מצבים אלה, מצד שני. אין ספק, שהבנת התהליכים האלה תאפשר, בסופו של דבר, טיפול טוב יותר במטופלים. למשל, הומוציסטינוריה (Homocystinuria) היא מחלה נסגנית (Recessive) הנגרמת בשל חסר אנזימטי של ציסטתיון בתא סינתאז (Cystathionin beta-synthase) וקשורה בקומה גבוהה ובמראה מרפנואידי (Marphanoid) (וכן במעורבות רב מערכתית). לאחרונה נמצא כי עלייה ברמת הומוציסטאין אצל מטופלים עם הומוציסטינוריה גורמת חיזור של קשרי דיסולפיד באזור ה-cbEGF של הגן פיברילין 1 (Fibrillin 1) הקשור בתסמונת מרפן. לנוכח ההבנה של התהליכים המולקולריים במחלה זו, קיימות אפשרויות טיפוליות הכוללות מתן Betaine, מתן פירידוקסין (ויטמין B6) והגבלת כמות המתיונין (Methionine) בדיאטה. בעבודה מבוקרת נמצא הבדל בגובה הממוצע בין הילדים המטפולים לאלה שאינם מטופלים .
גילוי הבסיס הגנטי של התסמונות השונות מקנה הבנה טובה יותר של התהליכים הביולוגיים התורמים לגדילה התקינה והבלתי תקינה של השלד, מאפשר מעקב נכון ולעתים גם טיפולים מתאימים יותר למטופלים ומקנה את האפשרות לתת ייעוץ גנטי מדויק למשפחות. לא תמיד האבחון המולקולרי (ברמת הגן) נותן כלים נוחים לסיווג. למשל, מוטציה בגן FGFR3 גורמת, מצד אחד, לסוגים שונים של גמדות/קומה נמוכה (Achondroplasia או Hypochondroplasia) ומצד שני, מוטציה באותו גן באזור שונה ובמנגנון אחר גורמת לתסמונת גדילת יתר CATSHL (Camptodactyly, Tall stature, and Hearing Loss). כמו כן, לעתים יש יותר מגן אחד הגורם לאותו חזותי (Phenotype), מצב המוכר כאי אחידות גנטית. למשל, תסמונת מרפן יכולה להיות קשורה בגן FBN1, אבל גם בגנים TGFBR2 ו-TGFBR1.
יש מקום לחשוב על בעיות אנדוקריניות באבחנה מבדלת של קומה גבוהה וגדילה מואצת. בנוסף, עוברים או תינוקות גדולים נולדים לאם סוכרתית לא מאוזנת במהלך ההיריון.
ערך מורחב – סוכרת הריון – Gestational diabetes
קליניקה
ילדים אשר להם תסמונת של גדילת יתר, יכולים להיות גדולים במשקל, בגובה ובהיקף ראש (או בחלק מהמדדים האלה) עוד בחיים התוך-רחמיים ומיד לאחר הלידה או שהם נולדים עם מדדי גדילה תקינים וחוצים את עקומות הגדילה הרגילות בחודשים הראשונים לחייהם.
התסמונות הקשורות בגדילת יתר, המוכרות לנו כיום, מאופיינות במעורבות רב מערכתית הכוללת לעתים גם סיכון יתר לגידולים שונים ולעתים קשורה בבעיות קוגניטיביות שונות. חשוב להכיר את התסמונות השונות כדי לאפשר לילדים אלה מעקב נכון וטיפולים במסגרות מתאימות, כדי לתת ייעוץ גנטי למשפחה בנוגע להריונות נוספים בעתיד וכן כדי לתת הסבר למטפלים ולמשפחות לגבי הפרוגנוזה של המצבים השונים. בחלק גדול של המצבים הגורם ידוע, וניתן לאשר את האבחנה באמצעות בדיקות.
ישנם בנוסף מצבים הקשורים בענקות ראש (Macrocephaly) כממצא עיקרי ותסמונות הנובעות משינויים כרומוזומליים, כגון: תסמונת קליינפלטר או תסמונת הקשורה בקריוטיפ 47 ,תסמונת ה-X המשולש.
אבחנה
האבחנה ההתחלתית נקבעת על סמך מדידות האורך בעת ההיריון או מדידות הגובה לאחר הלידה. אנחנו מגדירים קומה גבוהה כאשר התוצאה המתקבלת היא מעל 2 סטיות תקן, לגיל, למין ולמוצא האתני. בהיעדר סימנים לשינויים מבניים (Dysmorphic) ומעורבות של מערכות אחרות זולת השלד, יש לשלול תבנית משפחתית. בעת הבדיקה יש למדוד משקל, היקף ראש, לציין סימנים של שינויים מבניים ולבחון מעורבות של מערכות נוספות, כמו: עיניים, לב, טחול, כבד, כליות ומערכת השתן, מערכת העצבים (בעיות התפתחות). כמו כן, יש לשקול ביצוע בירור של המערכת ההורמונלית לשלילת מצבים אנדוקריניים נדירים (טבלה 1).
טיפול
חשוב להדגיש את המעקבים הנדרשים והטיפולים הקיימים במצבים השונים כיום, הדורשים התייחסות של הרופא המטפל וההתייחסות לייעוץ הגנטי בהתאם לאופן ההורשה והמנגנון הגנטי בבסיס המחלות השונות.
פרוגנוזה
תסמונות קלסיות של גדילת יתר
תסמונת ע"ש Sotos
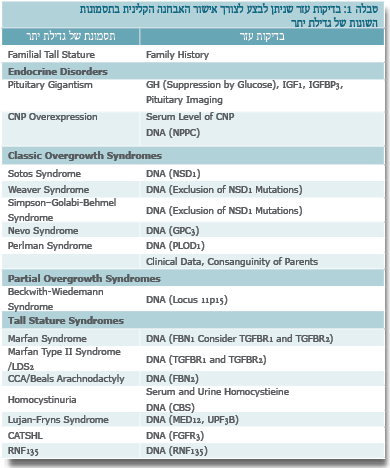
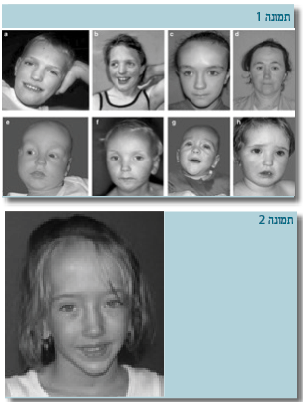
תסמונת ע"ש Sotos (MIM 117550) עוברת בתבנית הורשה אוטוזומלית דומיננטית. השכיחות שלה באוכלוסייה היא 1:15,000 לידות. התסמונת כוללת היקף ראש ו/או קומה גבוהה יותר מ-2 סטיות תקן לגיל ולמין, גיל עצמות מתקדם ובעיות התפתחות. יש לציין כי ברוב המקרים הקומה הסופית של הלוקים בתסמונת היא בטווח הנורמה. כמו כן, למטופלים סימנים דיסמורפיים אופייניים הכוללים מצח גבוה ורחב, מפתח עיניים הנוטה כלפי מטה, סנטר בולט והיפרטלוריזם (מרחק גדול מהרגיל בין העיניים). מראה הפנים האופייני הוא הממצא האבחנתי הקליני הקיים כמעט בכל המקרים. בעיות נלוות נוספות כוללות אפילפסיה, ממצאים במוח בבדיקת MRI, בעיות התנהגות, מומים בלב ובמערכת הגניטואורינרית וסקוליוזיס.
הגורם הגנטי למחלה הוא מצב של Haploinsufficiency בגן המקודד ל- NSD1 (Nuclear Receptor SET Domainprotein 1) אשר נמצא על כרומוזום 5q35. Haploinsufficiency הוא מצב שבו נשא של מוטציה בעותק אחד של הגן יבטא את המחלה מפני שכמות התוצר של העותק האחר והתקין של הגן אינה מספיקה לתפקוד נורמלי). ב-90%-60% של המקרים נמצא מוטציה בגן זה. מרבית המקרים קשורים במוטציות חדשות (de novo), אולם תוארו משפחות שבהן המוטציה עברה מדוד לדור בתורשה דומיננטית. אף שגדילת יתר היא קריטריון עיקרי בתסמונת זו, תוארו מקרים עם מוטציות בגן NSD1 אשר להם קומה רגילה והיקף ראש בגדר הנורמה.
ההשערה היא כי הביטוי חמור יותר כאשר מדובר בחסר חלקי או מלא של הגן (Microdeletion) לעומת מצבים הנגרמים ממוטציה נקודתית, לפיכך במצבים המשפחתיים, שבהם התמונה הקלינית לרוב קלה יותר, אופייני למצוא מוטציה נקודתית.
לפי הספרות העדכנית, לילדים הלוקים בתסמונת Sotos סיכון מוגבר של 3%-2% ללקות בגידולים שונים. תוארו מקרים של גידולים, כגון: Sacrococcygeal Teratoma, גידולים סרטניים, כגון: נוירובלסטומה והפטובלסטומה, וכן מקרים של לויקמיה לימפובלסטית חריפה (ALL) ו-T Cell Lymphoma. עדיין לא ברור אם מצב סיכון זה מחייב מעקב מיוחד בילדים עם תסמונת Sotos.
תסמונת Weave
התסמונת ע"ש Weaver (MIM 277590) היא תסמונת נדירה, ועד היום תוארו פחות ממאה מקרים. התסמונת מאופיינת בגדילת יתר המתחילה בחיים העובריים (Intra Uterine) ונמשכת לאחר הלידה. למטופלים מבנה פנים דיסמורפי הדומה ללוקים בתסמונת Sotos, אולם ללא הסנטר הבולט והרחב. בחולי Weaver הסנטר קטן, לעתים נסוג (Retrognatia) ואופייני קמט רוחבי בעור (Horizontal Crease) בין הסנטר לשפה התחתונה. כמו כן, קיים מרחק גדול בין העיניים (היפרטלוריזם) ואפרכסות אוזניים גדולות. לרובם קול נמוך וצרוד, בקע טבורי, שינויים אופייניים בשלד הכוללים גיל עצמות מתקדם, שינויים במבנה ובמנח האצבעות (קמפטודקטיליה), תנועתיות לא מלאה של המפרקים (Contracture) וכן ציפורניים שקועות. היות וקיימת חפיפה קלינית בין תסמונת זו לתסמונת ע"ש Sotos, בחלק מהחולים נבדק הגן NSD1 ואכן נמצאה בו מוטציה. אולם, ההנחה היא כי תסמונת Weaver היא תסמונת נפרדת אשר הגן האחראי לה עדיין לא אותר.
תסמונת SGBS (Simpson-Golabi-Behmel)
תסמונת SGBS (Simpson-Golabi-Behmel) (MIM 312870) נמנית עם התסמונות הנמצאות בתאחיזה לכרומוזום X. מאפייני התסמונת כוללים גדילת יתר המתחילה בחיים העובריים (Intra Uterine), ונמשכת לאחר הלידה, מראה פנים "גס", אף קצר עם נחיריים גדולים, אפרכסות נמוכות ומסובבות לאחור, מרחק גדול בין העיניים (היפרטלוריזם) וכן נטייה כלפי מטה של הזוויות החיצוניות של ארובות העיניים. נוסף על כך, ניתן למצוא מעורבות של מערכות גוף שונות, כגון: מומי לב, מומים בשלד (אצבע נוספת - פולידקטיליה), מומים בכליות ובדרכי השתן, חיך שסוע, בקע טבורי ומפשעתי ומומים נוספים. לרוב החולים בעיות התפתחותיות ובעיקר איחור שפתי ומוטורי. חשוב לציין כי קיים סיכון יתר לגידולים בתסמונת זו, בעיקר גידול בכליות ע"ש Wilms וכן הפטובלסטומה ונפרובלסטומה (תסמונת ע"ש BWS נמצאת באבחנה מבדלת, אולם קיימים כאמור הבדלים בין שתי התסמונות הן במאפיינים הקליניים והן בדרך ההורשה). התמונה הקלינית מתבטאת לעתים בצורה קלה גם אצל האמהות הנשאיות. הגן לתסמונת התגלה והוא נמצא על הזרוע הארוכה של כרומוזום X, ומקודד לחלבון GPC3 Glypican 3) ) . ב-70%-40% מהמקרים ניתן למצוא מוטציות בגן זה. תוארה גם תסמונת Type II SGBS אשר בה נמצא מאפיינים של SGBS1 ללא גדילת יתר והיא קשורה לגן אחר. המנגנון של גדילת היתר בתסמונת SGBS קשור ככל הנראה לתפקיד הגן ברגולציה של פקטורי גדילה שונים.
תסמונת ע"ש Nevo/Ehlers-Danlos Type VIA
תסמונת Nevo (MIM 601451) היא תסמונת נדירה המועברת בתורשה רצסיבית וכוללת קומה גבוהה עוד בחיים העובריים, קיפוסקוליוזיס, שינויים בכפות הרגליים, היפוטוניה כללית, גמישות יתר של המפרקים הגדולים, בצקת של כפות הידיים והרגליים ואצבעות פוזיפורמיות (הולכות ומתחדדות כלפי הקצה). התסמונת נגרמת בשל מוטציה בגן PLOD1 המקודד לאנזים Procollagen-Lysine 1,2-Oxoglutarate5-Dioxygenase 1.
יש לציין כי מוטציה בגן PLOD1 יכולה לגרום ל-EDS VIA (Ehlers Danlos Type VIA). לתסמונת זאת (EDS V1A) מאפיינים דומים ללא קומה גבוהה.
תסמונת ע"ש Perlman
התסמונת ע"ש Perlman או ,Renal Hamartomas Nephroblastomatosis and Fetal Gigantism (MIM 267000) היא תסמונת רצסיבית נדירה, המתאפיינת בריבוי מי שפיר בעת ההיריון, גדילת יתר מיד לאחר הלידה, שינויים בכליות, הכוללים: כליות מוגדלות, Nephro-Blastomatosis, דיספלזיה של הכליות ונטייה לפתח גידול ע"ש Wilms בכליות. קיים מראה פנים אופייני, פנים עגולות ומלאות, גשר אף נמוך, מראה היפוטוני עם פה פעור ושפה עליונה בולטת וכן סנטר נסוג מעט. התמותה גבוהה ובדרך כלל בגיל צעיר. יש לעתים הגדלה של כבד וטחול, היפר-אינסוליניזם ומיימת. הגורם התורשתי אינו ידוע.
תסמונת ע"ש Beckwith-Wiedemann
התסמונת ע"ש Beckwith-Wiedemann (MIM 130650) היא ברוב במקרים ספורדית. שכיחותה באוכלוסייה 1:13,700. היא מתאפיינת בממדי גוף גדולים (מאקרוזומיה), לשון גדולה (מאקרוגלוסיה), טחול וכבד מוגדלים (Visceromegaly) וכן נטיית יתר לגידולים שונים. סימנים דיסמורפיים נוספים ומעורבות מערכות גוף שונות מתוארים בטבלה 2. ברוב המקרים ההתפתחות של ילדים אלה היא תקינה. האבחנה מסתמכת על קריטריונים קליניים המתוארים בטבלה. המעקב כולל טיפול בהיפוגליקמיה לאחר הלידה, טיפולים הקשורים בבעיות משניות ללשון הגדולה (בעיות נשימה האכלה ודיבור), ובדיקות תקופתיות של אולטרה-סאונד ורמת AFP בדם שנועדות לגילוי מוקדם של גידולים.
בממוצע, המשקל והאורך אצל מטופלים עם BWS הוא בערכים הנמצאים מעל אחוזון 95 מיד לאחר הלידה ועד לבגרות. בהמשך הערכים הופכים לתקינים. יש לציין כי לחלק מהמטופלים גיל עצמות מתקדם לעומת הגיל עד גיל 4 שנים לערך.
המנגנון הגנטי קשור בהחתמה גנומית, אך הבסיס המולקולרי לתופעות השונות, כולל גדילת יתר, אינו נהיר לחלוטין. ידוע על מעורבות של גנים הקשורים בגדילה והפעלתם הבלתי תקינה אשר הוכחה במהלך השנים האחרונות. מדובר בקבוצת גנים הממוקמת על כרומוזום 11p15 הכוללת גם את הגן IGF2 (Insulin Growth Factor 2).
באופן נורמלי הגנים מתבטאים בשני האללים, זה הנתרם מהצד האבהי וזה מהצד האמהי. במצבים שבהם קיימת החתמה גנטית, המנגנון שונה. באזור הקשור לתסמונת BWS על כרומוזום 11p15, קיימת החתמה גנטית, ולכן הגנים באזור אינם מתבטאים משני האללים. במקום זה חלקם מתבטאים מהאלל האבהי (IGF2 ו(KCNQ10T1- וחלקם מהאלל האמהי (H19 ,CDKN1C ו-KCNQ1). שינויים בתבנית ההחתמה הגנומית יכולים לקרות מסיבות רבות, למשל: בשל חסר ב-DNA באזור האמור להתבטא (כגון: H19 באלל האמהי) או בשל מוטציה במרכז ההחתמה האמור לשלוט בתבנית מתילציה נכונה. גדילת היתר וכן נטיית היתר לגידולים יוחסו לגנים השונים המעורבים במנגנון מורכב זה. גן שנחקר רבות ויוחס לו תפקיד בגדילת יתר בתסמונת זו הוא IGF2, אשר נמצא תחת אותה מערכת בקרה של החתמה גנומית, כמו H19 (12), אולם גם נושא זה אינו חד-משמעי.
תסמונות הקשורות בקומה גבוהה
;תסמונת MFS (Marfan)
{{הפניה לערך מורחב|ערך=תסמונת מרפן - Marfan syndrome
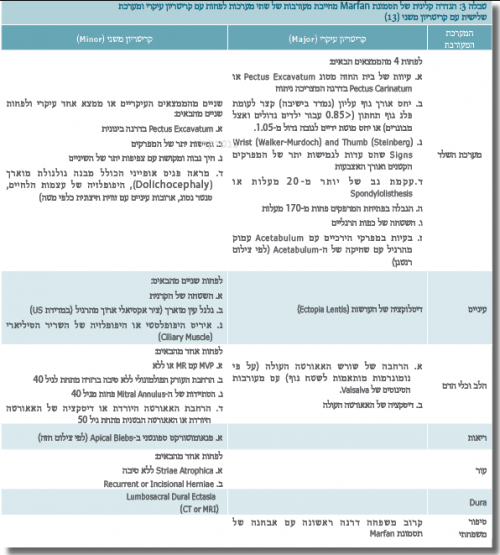
תסמונת Marfan (MIM 154700) היא תסמונת גנטית המועברת בתורשה אוטוזומלית דומיננטית (AD). שכיחותה באוכלוסייה הכללית היא 1:5,000-10,000. רק ברבע מהמקרים (25%) לא קיים סיפור משפחתי ואז מדובר במוטציה חדשה (de novo) שמעתה תעבור הלאה בתורשה האופיינית (AD). הלוקים בתסמונת הם ברוב המקרים בעלי קומה גבוהה עם אורך גפיים חריג ביחס לשלד (Dolichostenomelia). במעקבי גדילה רובם הגדול יימצא סביב אחוזון 95 ואילך. כיום, מתבצעת האבחנה הקלינית לפי הקריטריונים שנקבעו ע"י הקבוצה הבלגית, De Paepe et al., בשנת 1996 (טבלה 3). הקריטריונים נקבעו כדי להגיע לדיוק באבחון הקליני, כך שלא כל פרט גבוה בעל מבנה פנים מוארך ו/או מוטת ידיים גדולה (Marfan Habitus) יקבל את האבחון הקליני כלוקה בתסמונת. הגן לתסמונת מופה והוא נמצא על כרומוזום 15, סימונו FBN1 והוא מקודד לחלבון 1 Fibrillin. במצב תקין החלבון נמצא בחומר החוץ-תאי, והוא מהווה מרכיב חשוב במבנה המכונה Microfibrils.
מבנה זה נמצא ברקמות שונות בגוף ולו תפקידים חשובים ביצירה ובהומאוסטזיס (Homeostasis) של החומר האלסטי, בחיבור בין התא לחומר החוץ-תאי וברגולציה של פקטורי גדילה (Growth Factors) שונים. מוטציות בגן גורמות ליצירת תוצר (=חלבון) לא תקין אשר מתערב עם התוצר (=חלבון) התקין שנוצר בהשראת הגן השני התקין, ובמנגנון המכונה Dominant Negative מפריע ליצירה תקינה של ה-Microfibrils. עבודות שונות הראו במקביל כי לחולי מרפן גם כמות מופחתת של רקמת חיבור, ויש הטוענים כי הדבר נובע מחשיפת יתר של הרקמה הלא תקינה לפרוטאוליזה. יש לציין כי הדבר לא מסביר את מנגנון גדילת היתר בחולי מרפן. לאחרונה דווח על אינטראקציה בין פיברילין לפקטור הגדילה TGF-β, ומוטציות בגן המקודד לרצפטור של TGF-β TGFBR2 נמצאו כגורמות לתסמונת Marfan Type II) MFS II), תסמונת הדומה למרפן ללא Ectopia Lentis ומינימום או היעדר עירוב של מבנה השלד החריג ביחס לגפיים - Dolichostenomelia.
תסמונת ע"ש Loeys-Dietz
תסמונת נדירה אשר כיום מוכרים בה 2 סוגים עיקריים: LDS (Loeys-Dietz) Type I, II, המועברים בתורשה אוטוזומלית דומיננטית (AD). המערכות העיקריות המעורבות בחולי LDS הן:
- המערכת הווסקולרית - הרחבה או דיסקציה של שורש האאורטה (95% מהמקרים). אנוריזמות או פיתול (Tortuosity) של כלי הדם העורקיים באזורי גוף שונים.
- מערכת השלד, כגון: עקמת, מבנה לא תקין של בית החזה, ארכנודקטלי וכד'.# גולגולת/פנים - היפרטלוריזם, חייך שסוע או ענבל מפוצל (Bifid Uvula), תפרים לא תקינים בגולגולת (Craniosynostosis).
- העור - עור דק/שקוף, ניזוק בקלות, צלקות לא תקינות.
ב-2 הסוגים אופייני למצוא פגיעה במערכת הווסקולרית ובשלד. ב-LDS1 אופייני נוסף על כל אלה, עירוב של גולגולת/פנים, ואילו ב-LDS2 עירוב של העור.
בשנים האחרונות התברר כי הסיבה לתסמונות הן מוטציות בגנים TGFBR2 ו-1 TGFBR (Transforming Growth Factor ß Receptor) הנמצאים על כרומוזום 9q ו-3p בהתאמה.
תסמונת LDS2 דומה בחלק מהמאפיינים הקליניים שלה לתסמונת Marfan ונקראת גם Marfan Type II. בספרות קיימים דיווחים על חולים שענו לקריטריונים של תסמונת מרפן, אולם לא נמצאו נושאים מוטציה בגן FBN1, ובבדיקה נמצאה אצלם מוטציה בגן TGFBR2.
תסמונת CCA (Congenital contractural arachnodactyly) (Beals Syndrome)
תסמונת CCA (MIM 121050) העוברת בתורשה אוטוזומלית דומיננטית, מתאפיינת בקומה גבוהה, קונטרוקטורות מהלידה (בברכיים, במרפקים ובאצבעות) אצבעות ארוכות, היפוטוניה, קיפוסקוליוזיס מתקדמת ומבנה לא תקין של אפרכסות האוזניים (Crumpled Ears). בצורתה הקלסית התסמונת אינה כוללת מעורבת של המערכת הקרדיו-וסקולרית, אולם תוארו מספר מקרים של חולים עם CCA אשר נמצאה אצלם הרחבה של שורש האאורטה.
הגן המעורב בתסמונת זו הוא FBN2 המקודד לחלבון Fibrillin 2 אשר נמצא על הזרוע הארוכה של כרומוזום 5. מנגנון הפגיעה ברקמת החיבור דומה לזה של FBN1. ההנחה היא כי הביטוי הפנוטיפי שונה בשל עיתוי שונה של התבטאות הגן בעת התפתחות העובר והתבטאותו ברקמות שונות מאלה של FBN1.
הומוציסטינוריה
הומוציסטינוריה (MIM 236200) היא תסמונת נדירה העוברת בתורשה אוטוזומלית רצסיבית. היא מאופיינת בקומה גבוהה מעל אחוזון 95, אוסטאופורוזיס, סקוליוזיס, מעורבות של העיניים Ectopia Lentis) וקוצר ראייה) מעורבות של כלי דם (Livido Reticularis) וכן מעורבות נוירולוגית הכוללת פיגור שכלי ומחלות פסיכיאטריות.
התסמונת נגרמת ממוטציות בגן המקודד לאנזים Cystathionine Beta-Synthase. בשל ירידה בפעילות האנזים, נמצא בבדיקת דם רמות גבוהות מאוד של הומוציסטאין ומתיונין ורמות נמוכות של Cysteine ו-Cystathinine. כפי שכבר תיארנו, ניתן לטפל בחלק מהתופעות של המחלה באמצעות תרופות. גם במחלה זו נמצא קשר לתסמונת Marfan - הרמות הגבוהות של הומוציסטאין גורמות חיזור של גשרי דיסולפיד על החלבון פיברילין ומשנה את המבנה שלו, ובשל כך משנות גם את תפקודו.
תסמונות נדירות יותר
תסמונת LFS (Lujan-Fryns)
תסמונת LFS (MIM 309520) היא נדירה המועברת בתאחיזה לכרומוזום X. התסמונת כוללת קומה גבוהה, אצבעות ארוכות וגמישות יתר של המפרקים הקטנים ומבנה מרפנואידי המופיע לאחר גיל ההתבגרות. בשונה מתסמונת Marfan לחולים אלו פיגור שכלי. לאחרונה ידוע על שני גנים הקשורים בתסמונת: MED12 ו-UPF3B. ביטוי יתר של הגן NPPC (Natriuretic Peptide Precursor C) מדובר במצב נדיר אשר תואר בחולים בודדים בעולם. הביטוי כולל גדילת יתר לאחר הלידה מעבר לשתי סטיות תקן בגובה, Marfanoid Habitus, סקוליוזיס, אגודלים ארוכים וMetaphyseal-Epiphyseal Dysplasia. הגן מקודד לחלבון שלו תפקיד בבקרה על גדילה של העצמות, ולכן מוטציה בו גורמת לגדילת יתר.
תסמונת CATSHL
תסמונת CATSHL (MIM 610474) מועברת בתורשה אוטוזומלית דומיננטית. התסמונת כוללת קמפטודקטיליה, קומה גבוהה וליקוי שמיעה סנסורינאורלי. נוסף על כך, לחלק מהחולים פיגור שכלי, מיקרוצפליה ושינוי במבנה בית החזה (Pectus Excavatum). הגורם לתסמונת הוא מוטציה בגן FGFR3 באזור הטירוזין קינז של הרצפטור במנגנון Negative Dominant (הסבר לגבי מנגנון זה ראה בפרק הדן בתסמונת Marfan). מעניין לציין כי לגן זה תפקיד ידוע בגדילה של השלד, ומוטציות שונות באלל זה נותנות תמונה קלינית של גמדות או קומה נמוכה.
RNF135
תסמונת זו (MIM 611358) נדירה ותוארה עד כה בשישה חולים. הגן נמצא על כרומוזום 17. לחולים קומה והיקף ראש מעל הנורמה בשתי סטיות תקן. נוסף על כך, סימנים דיסמורפיים הכוללים מצח רחב, קצה אף רחב, פילטרום ארוך, ארובות עיניים Downslanting, שפה עליונה צרה ושפה תחתונה מלאה. לחלק החולים פיגור שכלי, גיל עצמות מתקדם, בעיות שמיעה וראייה. קיימת חפיפה פנוטיפית עם תסמונת Sotos ועם תסמונת Weaver, אולם לא נמצאה מוטציה בגן NSD1 בחולים אלו. תפקיד הגן אינו ידוע.
סיכום
דגלים אדומים
ביבליוגרפיה
קישורים חיצוניים
- תסמונות של גדילת יתר, מדיקל מדיה
המידע שבדף זה נכתב על ידי ד"ר חנה וינקלר, ד"ר עמיהוד זינגר


 כניסה
כניסה  עקבו אחרינו בפייסבוק
עקבו אחרינו בפייסבוק